Генетический код – ключ к созданию вакцины от рака
«Ученые нашли лекарство против рака, которое оказалось смертельным вирусом и привело к вымиранию человечества», «в гигантской подземной лаборатории на волю вырывается опаснейший вирус, мгновенно превращая своих жертв в прожорливых зомби» – к счастью, это не заголовки новостных лент, а сюжеты знакомых всем фантастических фильмов – «Война миров Z», «Обитель зла», «Я легенда». Но чтобы фантастика не стала реальностью, человечество должно быть готово к любому развитию событий и работать над технологиями создания вакцин от любого нового, неизвестного науке вируса.
Заведующая лабораторией структурной биоинформатики и молекулярного моделирования Новосибирского государственного университета, к.б.н. Анастасия Бакулина рассказала о том, как создать вакцину, не зная ничего про вирус; почему российские ученые работают над вакциной против вируса Эбола, если она в России никому не нужна; и как в будущем будут лечить рак
Моделирование процессов, приводящих к развитию болезни Альцгеймера; разработка вакцин против рака, лихорадки Эбола и других опасных инфекций – эти глобальные задачи, стоящие перед мировой наукой, являются предметом исследования лаборатории структурной биоинформатики и молекулярного моделирования НГУ
Вакцина от вируса без вируса
Вероятность эпидемии, от которой погибнет все человечество, очень мала. Она сравнима с вероятностью уничтожения Земли метеоритом, – говорит Анастасия Бакулина, – но, тем не менее, создание противометеоритной системы планеты сегодня считается серьезным вызовом. Разработка платформ для оперативного получения вакцин против любых вирусов – не менее актуальная задача, стоящая перед человечеством. Например, российские ученые работают над созданием вакцины против лихорадки Эбола несмотря на отсутствие прямой угрозы эпидемии этого заболевания в нашей стране.

При стандартном способе получения вакцин, например, против гриппа, вирус размножают в искусственных условиях и потом убивают. В ответ на введенный мертвый вирус в организме человека вырабатываются антитела, которые в случае заражения узнают живой вирус и нейтрализуют его. Те части вируса, которые вызывают выработку антител, называются антигенами. В случае с гриппом в создании универсальной вакцины нет необходимости – при появлении новой модификации того же вируса для него быстро сделают и новую «сезонную» вакцину.
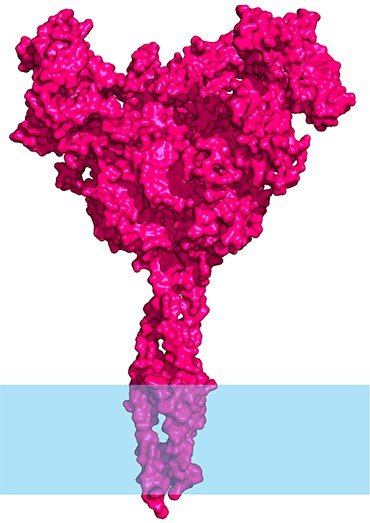 Многочисленные попытки сделать вакцину против вируса Эбола стандартным способом не привели к успеху. Поэтому пришлось использовать другой подход: создавать «гибридные» неопасные вирусы или вирусоподобные частицы, несущие на своей оболочке поверхностный белок вируса Эбола. В такой конструкции поверхностные белки можно менять в случае необходимости – например, белки вируса Эбола на белки вируса Марбург. Поэтому, это не вакцина, а платформа для разработки вакцин.
Многочисленные попытки сделать вакцину против вируса Эбола стандартным способом не привели к успеху. Поэтому пришлось использовать другой подход: создавать «гибридные» неопасные вирусы или вирусоподобные частицы, несущие на своей оболочке поверхностный белок вируса Эбола. В такой конструкции поверхностные белки можно менять в случае необходимости – например, белки вируса Эбола на белки вируса Марбург. Поэтому, это не вакцина, а платформа для разработки вакцин.
Важно, что такая технология безопасна, так как работы проводятся с искусственной конструкцией без участия живого вируса. Только на этапе доклинических исследований, когда вакцины проверяют на лабораторных животных, ученые работают с соблюдением всех мер безопасности, в специальных «скафандрах».
Для разных типов вирусов нужны свои платформы: например, вирус Зика отличается от вируса Эбола по способу «упаковки» поверхностных молекул-антигенов, и для них нужны разные носители. Основной вклад в такие работы вносят вирусологи, но для большей эффективности антител биоинформатики модифицируют белки, которые находятся на поверхности конструкций.
Очень важный момент – скорость получения нужной вакцины. Сейчас каждая инфекция вызывает не всегда обоснованную панику, у которой есть свои «побочные эффекты»: неправильное, нерациональное поведение как пациентов, так и врачей. Но если будет известно, что вакцина появится быстро, паники будет меньше. К сожалению, даже в этом случае вакцина не спасет тех, кто уже заболел – для того, чтобы выработался иммунитет, необходимо время.

В России зарегистрированы и представлены Всемирной организации здравоохранения две вакцины от лихорадки Эбола ("Гам-Эвак" и "Гам-Эвак Комби"). Но вирусы эволюционируют, и неизвестно, какая из вакцин будет более эффективна при появлении измененного вируса. Например, вирус лихорадки Эбола, вызвавший эпидемию 2014 г., отличается от обнаруженного в Африке в 1976 г. Будет ли современная вакцина работать для будущих эпидемий? Биоинформатика помогает анализировать эволюцию вируса и с учетом этого модифицировать старую вакцину.
Необязательно знать врага в лицо
Создавать вакцины нового поколения невозможно без биоинформатики, и, хотя существует множество бесплатных компьютерных программ, которыми уже пользуются ученые, для получения прорывных результатов необходимы новые методы и программы. Одна из проблем создания вакцин – что произвольно выбранный фрагмент белка патогена, взятый за основу для вакцины, в растворе может принимать другую форму, а это означает, что вакцина работать не будет. В разработке научного руководителя нашей лаборатории Андрея Вилховича Каявы реализована идея преодоления этой проблемы с помощью методов биоинформатики на примере возбудителя малярии (простейшие рода Plasmodium – в данном случае P. vivax и P. falciparum).
Метод позволяет выбрать такой фрагмент белка, который в растворе будет иметь ту же форму, что и в целом белке – при этом ничего не зная о функциях того или иного участка генома, о том, какую роль играют различные белки в жизни данного патогена и в развитии болезни. Несколько таких фрагментов Каява выбрал из генома малярийного плазмодия, и, действительно, оказалось, что у переболевших малярией людей на выбранные фрагменты вырабатываются антитела. После этого из фрагментов были выбраны самые перспективные, на основе которых в настоящее время идут работы над созданием вакцины.
То есть, даже если мы не знаем, что за вирус перед нами, каковы симптомы заболевания, которое он вызывает, с высокой вероятностью можно определить, куда будет направлен иммунный ответ.

Вместе с учеными из Монголии мы планируем применить эту методику для создания вакцины против вируса ящура. Для нас – это быстрый, без многолетних клинических испытаний, способ показать высокую эффективность метода. Это необходимо, чтобы заинтересовать серьезных партнеров, к примеру, таких, как Государственный научный центр вирусологии и биотехнологии «Вектор».
ГНЦ «Вектор» – одна из немногих организаций в России, способная провести самостоятельно всю работу по созданию вакцины от начала до конца, включая производство. Перспектива сотрудничества с ними заключается в том, чтобы соединить наш метод выбора фрагментов белков с созданными на базе центра платформами для универсальных вакцин.
Пока метод не полностью автоматизирован, но мы думаем, что со временем напишем программу, которая будет сама предлагать варианты фрагментов белков, закодированных в геноме, на основе которых можно создавать вакцину. Тогда весь процесс будет выглядеть следующим образом: появляется новый инфекционный агент, его «ловят», генетический код расшифровывает и «изучает» программа. Возможно, она сможет даже автоматически выбирать платформу из уже имеющихся, но, как минимум, она выдаст код фрагмента ДНК, который нужно синтезировать и внести в плазмиду – кольцевую молекулу ДНК, на основе которой клетки могут синтезировать белки. Плазмиды, в свою очередь, вносят в культуру клеток, производящих вакцину в виде псевдовирусных частиц, на поверхности которых находятся нужные нам антигены. Клетки вырабатывают вакцину так же, как зараженные вирусом клетки производят новые вирусы, только внутри этих вакцинных частиц не будет полноценного генетического материала для дальнейшего размножения, они будут неопасны.
В фантастических фильмах ученые часто создают вакцину от новой неизвестной болезни за считанные дни, и пока для специалистов это выглядит смешно. Но, имея такую технологию, мы можем сделать это реальностью.
Персонализированные вакцины против рака
Если совместными усилиями мы создадим систему, которая на основе структурной биоинформатики сможет быстро выбирать фрагменты белков и подбирать платформы для создания универсальных вакцин, то ее можно использовать не только для борьбы с инфекционными болезнями, но и против рака – активируя гуморальный иммунный ответ, B-лимфоциты, вырабатывающие антитела. Для рака также очень важен T-клеточный ответ, для вызова которого используются маленькие фрагменты белков, и такие фрагменты современная биоинформатика уже умеет эффективно предсказывать.
Используя те же алгоритмы, как с инфекционными агентами, мы можем выбрать антигены из клеток опухоли больного человека и создать на их основе терапевтическую вакцину. Из многочисленных исследований уже известно, какие антигены, характерные для раковых клеток, наиболее вероятны при разных видах рака. Если секвенировать совокупность РНК клеток опухоли, можно определить, какие в клетке есть белки. Если обнаружатся белки, которых там быть не должно, они, вероятно, и будут раковыми антигенами для опухоли конкретного человека.
Этот путь не гарантирует точности, но попытаться определить правильную мишень с помощью технологий, называемых «анализ генных сетей», можно. Пока это дорого, но, если направление будет развиваться, то и цена снизится. Наша лаборатория работает над теоретической частью – мы предлагаем конструкции, которые могут быть вакциной, а сотрудники Институт клинической иммунологии СО РАМН придумывают, как ввести эту конструкцию в клетки иммунной системы, какие дополнительные молекулы нужны для усиления работы иммунитета.
Раковая опухоль живет потому, что научилась обманывать иммунитет: она выделяет молекулы, которые подавляют клетки иммунной системы. Но можно выделить эти клетки из крови и «обучить» их бороться с опухолью. Такой способ лечения рака, при котором у человека берут кровь, выделяют клетки, отвечающие за иммунитет, и в пробирке, с добавлением стимулирующих иммунитет веществ, «обучают» их бороться с опухолью, а потом вводят обратно в организм – это продолжение развития идеи о том, что рак – это проблема иммунной системы.
Недавно американские ученые (из онкологического научного центра Фреда Хатчинсона в Сиэтле, США) смогли с помощью иммунотерапии вывести в ремиссию безнадежных онкобольных. Это демонстрация результатов развития этого же направления, они работают над активацией Т-клеточного противоопухолевого иммунитета. В данном случае в геном Т-лимфоцитов внесли модификацию – химерную, искусственную конструкцию, состоящую из кусочков существующих в природе молекул, кодирующую фрагменты клеточных рецепторов, помогающих Т-лимфоциту распознавать раковые молекулы и активно атаковать их.
Общая схема такой иммунотерапии давно известна, но новизна разработки в том, что создана конкретная химерная молекула удачной конструкции. Однако молекул, которые регулируют иммунитет, очень много, и, если найдена удачная комбинация, это не значит, что нельзя найти еще более удачную. Думаю, в этом направлении будет много работ, хотя здесь есть две проблемы.
Конечно, опубликованные учеными снимки, на которых опухоль изображена «до» и «после» лечения, очень эффектны, особенно когда опухоль исчезла полностью. Но к сожалению, это не означает, что раковые клетки не возникнут снова – могут оставаться микроскопические метастазы, которые продолжат «свое дело». Очень многие результаты по «суперлечению» рака имеют одно и то же трагическое продолжение: человек полностью выздоровел, начал ходить на работу, в тренажерный зал и так далее, но через пару лет у него случился рецидив, предыдущий вид лечения не помог, человек умер. Вторая проблема – очень дорогое лечение, в десятки раз дороже стандартного, которое тоже не дешево. Есть надежда, что цену удастся понизить за счет удешевления технологий, но, это будет возможным, только если направление будет широко распространено.
Тем не менее, каждый результат – это еще один шаг в борьбе против рака – когда есть высокие шансы вылечить рак, использование иммунотерапии делает эти шансы еще выше. И в случае широкого внедрения многие люди с онкозаболеваниями смогут жить гораздо дольше. Но нужно понимать, что это – пока не прорыв и не панацея.
Мне думается, что в будущем лечение рака будет полностью автоматизированным процессом: из крови онкобольного аппарат забирает клетки иммунной системы и клетки опухоли, – которые там есть, если уже началось метастазирование. Через достаточно короткое время человеку вводят его же клетки иммунной системы, но уже обученные распознавать и атаковать его опухоль. Возможно, эту процедуру необходимо будет повторять несколько месяцев, а, может, всю жизнь, но она увеличит продолжительность и качество этой жизни. Сложно сказать, когда это будущее наступит, но если сравнивать, скажем, с полетом человека на Марс, то оно более реально. Технологии, которые для этого нужны, развиваются уже сейчас.
Подготовили Татьяна Морозова, Мария Перепечаева