Бактериофаги – враги наших врагов
Бактериофаги – это вирусы, способные уничтожать бактерии. Основная роль в природе этих «пожирателей» наиболее многочисленных клеточных организмов на Земле заключается в существенном ускорении разложения органического вещества. Тем самым фаги, влияя на глобальные геохимические процессы, поддерживают круговорот вещества и энергии в биосфере Земли. Что касается человека, то поскольку многие из бактерий являются нашими врагами, кажется естественным использовать фаги в качестве эффективного и безопасного «биологического оружия» для уничтожения или контроля численности вредных и болезнетворных микроорганизмов.
Наша страна была пионером фаготерапии, ставшей сегодня актуальным биомедицинским направлением. Первые отечественные фаговые препараты были разработаны в Тбилиси еще в 1930-е гг., а в настоящие дни они выпускаются в широком ассортименте. В отличие от обычных антибиотиков они обладают высокой избирательностью, не приводят к возникновению лекарственной устойчивости у патогенов и не имеют негативного побочного действия на организм больного. Однако их применение в клинической практике до сих пор ограничено в силу ряда объективных и субъективных причин, от противодействия крупных фармацевтических компаний до отсутствия квалифицированных специалистов и хорошо оборудованных микробиологических центров
Бактериофаги (с древнегреч. – «пожирающие бактерии»), или просто фаги, – это вирусы, способные поражать бактерии. Согласно современным данным, основная роль в природе этих «убийц» бактерий, которые являются наиболее многочисленными клеточными организмами на Земле, заключается в существенном ускорении разложения органического вещества (в конечном счете до углекислого газа и воды). Тем самым фаги, влияя на глобальные геохимические процессы, поддерживают круговорот вещества и энергии в биосфере Земли. Что касается человека, то поскольку многие бактерии являются нашими врагами, кажется естественным использовать фаги в качестве эффективного и безопасного «биологического оружия» для уничтожения или контроля численности вредных и болезнетворных бактерий
Еще несколько цифр: если предположить, что средний диаметр фаговой частицы составляет 50 нм, то все бактериофаги планеты, построенные «в одну шеренгу», составят линию протяженностью 5*1020 км или 5*107 световых лет! Именно на таком расстоянии расположено ближайшее к нам скопление галактик в созвездии Девы, а до ближайшей звезды Проксима Центавра всего 4,2 световых года
Как и все вирусы, бактериофаги находятся на границе между живым и неживым. Вне клеток-хозяев большинство фагов существует в виде вирионов – объектов, напоминающих сложные молекулярные кристаллы. А «живут» фаги, т. е. размножаются, только внутри бактериальных клеток, поскольку их генома недостаточно для автономного существования.
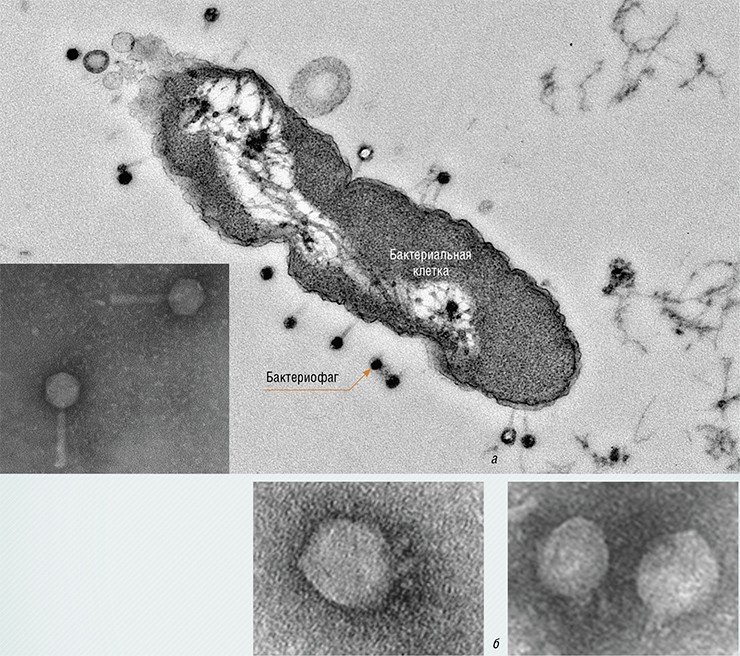
В 1915 г. англичанину В. Туорту и французу Ф. д’Эрелю удалось выделить эти агенты (впоследствии д’Эрелю пришлось многие годы бороться за свой приоритет с Туортом). Именно д’Эрель назвал вновь открытые частицы «бактериофагами». Он сразу понял, что они могут найти применение в качестве противобактериальных препаратов, и в 1919 г. впервые применил фаговый препарат для лечения дизентерии у детей
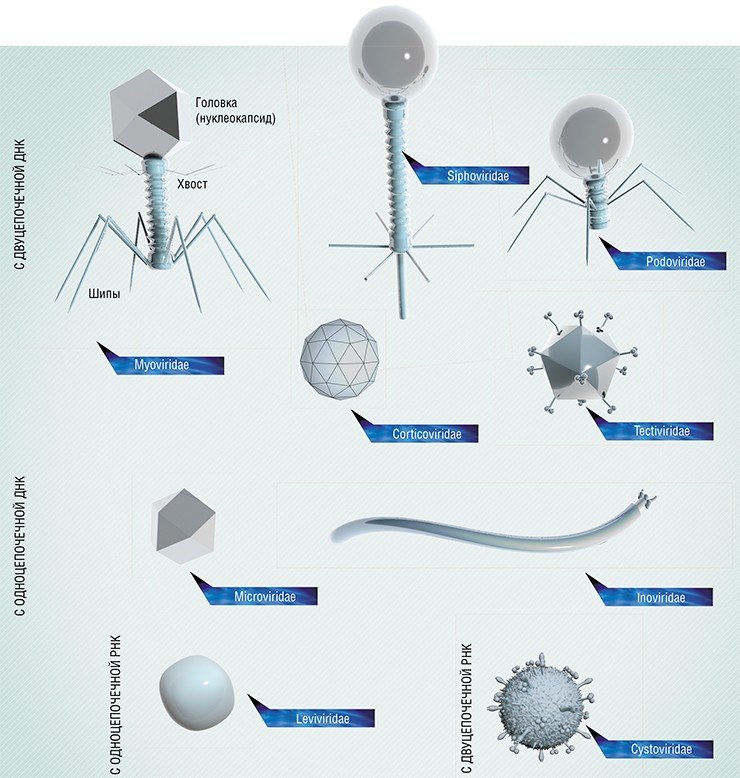
Мир бактериофагов весьма разнообразен: на сегодня известно более 500 разных видов фагов, отличающихся формой и строением. По отношению к бактериям фаги делятся на умеренные и литические. Умеренные фаги встраивают свой геном в геном бактерии, но проявляют свою «убийственную» активность не сразу: затаившись в нем, они размножаются вместе с бактериями и затем уничтожают их расплодившееся потомство. Лизирующие же фаги, заражая бактерию, сразу убивают ее. Именно такие простые фаги являются на сегодня наиболее привлекательными, с точки зрения использования в биотехнологиях и для терапевтических целей.
Боевые «машины»
Бактериофаги, эти настоящие природные боевые машины, устроены крайне просто: их генетический материал, ДНК или РНК, упакован в белковую оболочку, снабженную «орудиями» – специальными устройствами для нападения на бактерии.
Размер генома у разных фагов может различаться. У некоторых он очень мал – (от 3,5 тыс. пар нуклеотидов), в таком геноме хранится информация всего лишь о 3—4 белках. Более того, гены, кодирующие эти белки, вынуждены перекрываться (накладываться друг на друга). Размер геномов у других фагов сопоставим с размером геномов крупных, сложно организованных вирусов многоклеточных животных, достигая 170 тыс. пар нуклеотидов (самый крупный из известных фагов содержит около 480 тыс. пар оснований!). Такой геном может кодировать уже до двухсот различных белков. Именно такие фаги обычно имеют большие размеры и сложно организованы.
ЧУДЕСА БАКТЕРИОФАГОВ Люди издавна сталкивались с чудесными случаями исцелений от инфекционных заболеваний. Сегодня мы имеем право считать, что зачастую их можно объяснить неосознанным использованием бактериофагов. Ведь эти бактерицидные агенты встречаются на Земле повсеместно – в почве и в воде, а для лечения воспалений и ран с древнейших времен применяли грязи и смеси на основе природных продуктов. Не исключено, что подобные случаи чудесного исцеления вызвали к жизни такие обряды, как омывание в священных водах Ганга и крещение в Иордане.
Люди издавна сталкивались с чудесными случаями исцелений от инфекционных заболеваний. Сегодня мы имеем право считать, что зачастую их можно объяснить неосознанным использованием бактериофагов. Ведь эти бактерицидные агенты встречаются на Земле повсеместно – в почве и в воде, а для лечения воспалений и ран с древнейших времен применяли грязи и смеси на основе природных продуктов. Не исключено, что подобные случаи чудесного исцеления вызвали к жизни такие обряды, как омывание в священных водах Ганга и крещение в Иордане.
Антибактериальную активность природных продуктов пытались использовать и не в столь далекие времена. В 1920-х гг. великий хирург-архиепископ Святитель Лука (Войно-Ясенецкий), находясь в ссылке в глухой деревне, узнал о местной знахарке, умеющей излечивать гнойные раны и чирьи с помощью смеси из земли, кислого молока и золы. Лука попытался разобраться в природе этого явления, экспериментируя с составом композиции. Однако результаты лечения плохо воспроизводились (впрочем, как и у всех работавших в то время с бактериофагами). Иногда оно приводило к фантастически быстрому излечению больных, иногда вовсе не помогало. Не имея необходимых условий для работы и возможности ознакомиться с медицинской литературой, Лука вынужден был оставить свои исследования. Сейчас мы знаем, что эффективность фагового препарата будет зависеть от того, имеются ли в его составе бактериофаги, «специализирующиеся» на патогенных бактериях конкретного пациента
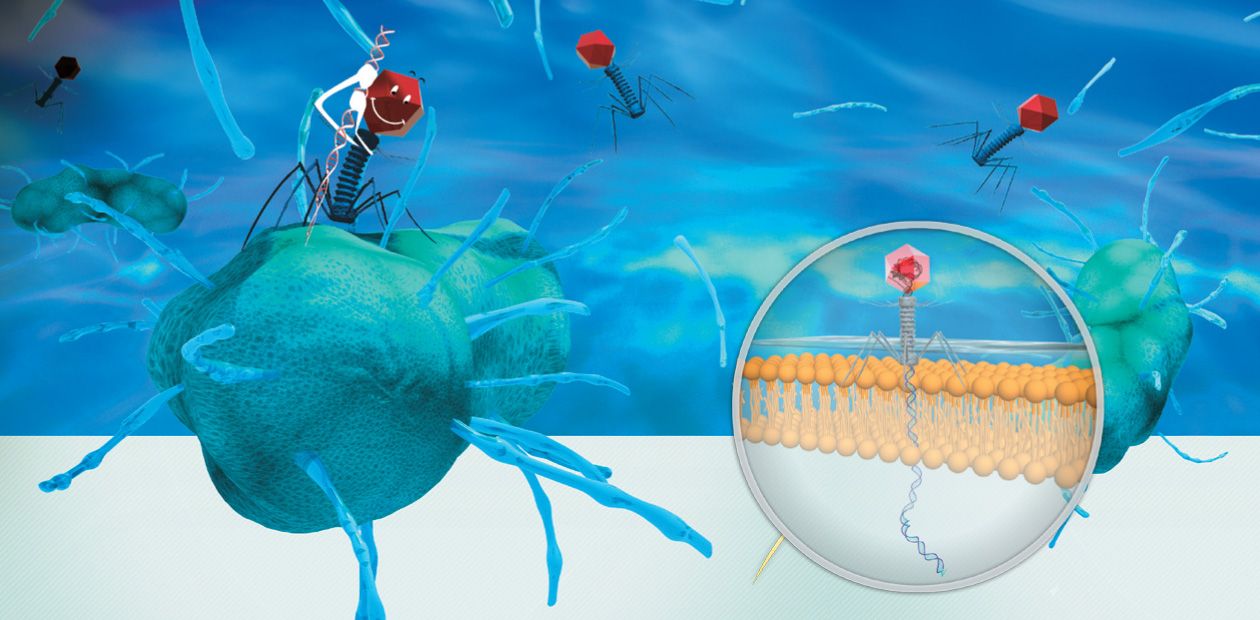
Лизирующий фаг своим видом больше всего напоминает космический корабль-робот, способный стыковаться с заданным объектом. К головке фага, представляющей собой белковый резервуар с упакованной в ней ДНК, присоединен «хвост» − белковая структура наподобие щупалец, на которых расположены так называемые узнающие элементы, способные прочно связываться с рецепторами (особыми белками или полисахаридами) на поверхности бактерии.
После такой «стыковки» с бактерией-мишенью фаг прочно прилипает к ее поверхности. На одну бактериальную клетку могут одновременно напасть сотни бактериофагов, но чтобы убить ее, достаточно и одного. При этом взаимодействие фаг-клетка очень специфично: конкретный фаг может взаимодействовать лишь с определенными (целевыми) видами бактерий и не способен присоединяться к клеткам человека.
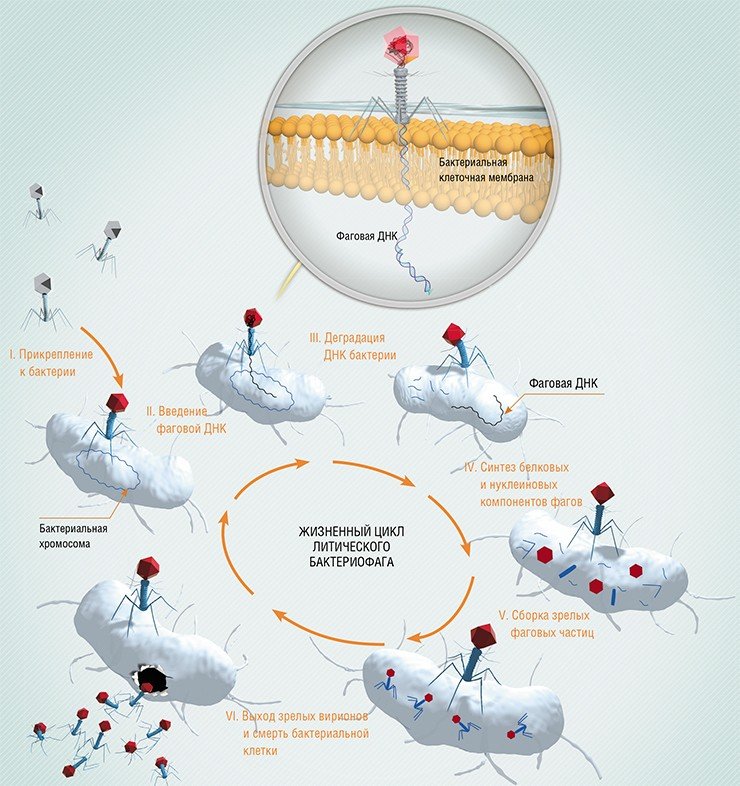
Когда фаг закрепится на поверхности бактерии, его «хвост» с помощью специальных белков внедряется в бактериальную стенку, протыкая ее. Сквозь хвостовой канал генетический материал фага вбрасывается в клетку. Генетические программы фага берут под контроль все жизнеобеспечение клетки: с этого момента все ее материальные и энергетические ресурсы, все молекулярные «машины» переключаются на синтез белков и копий генома фага.
Бактерия обречена. В течение следующего получаса в клетке синтезируются сотни и тысячи новых фаговых частиц, после чего она разрушается, высвобождая очередной отряд бактериальных «убийц».
Гонка вооружений
По оценке специалистов, каждые двое суток бактериофаги уничтожают половину мировой популяции бактерий. Вот почему эти быстро размножающиеся организмы не покрыли толстым слоем всю поверхность нашей планеты – в отсутствии фагов они сделали бы это за несколько дней.
Но несмотря на такую высочайшую антибактериальную эффективность фагов, бактерии все же не исчезли с лица планеты. Дело в том, что в течение многих миллионов лет шла совместная эволюция этих организмов, которую было бы точнее назвать «гонкой вооружений». Благодаря мутациям фаги «изобретали» все новые средства и приемы ведения войны, а бактерии, в свою очередь, хитроумные средства защиты.
Например, ДНК всех бактерий несет на себе особые метки (метилированные основания), и специальные бактериальные ферменты рестрикции расщепляют любую ДНК, на которой таких меток нет, в том числе и фаговую. Однако некоторые фаги научились имитировать такие метки и таким способом обходить защиту.
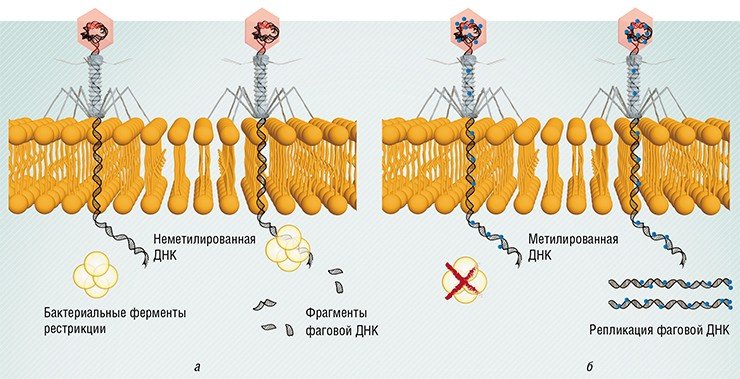
Еще один защитный механизм бактерий – изменение поверхностных рецепторов: в этом случае фаг просто не может узнать «свою» бактерию. В ответ на это появляются фаги, несущие измененные узнающие элементы, которые способны связываться с новыми бактериальными рецепторами. Имеется несколько механизмов подобной модификации генетических программ у фагов и бактерий. Мутации могут возникать случайно, в ходе генетического копирования. Кроме того, с помощью рекомбинации (генетического перераспределения) разные виды фагов могут обмениваться фрагментами своего генома и даже захватывать фрагменты генома бактерий.
К слову сказать, с точки зрения медицины, изменение рецепторов болезнетворной бактерии может быть благом для человека, поскольку именно бактериальные рецепторы служат факторами вирулентности, определяющими выживание и размножение возбудителя в организме-хозяине. И устойчивые к фагу мутанты обычно являются менее патогенными по сравнению со своими предшественниками.
Фаготерапия: сквозь тернии
Открытие вирусов, убивающих бактерии, дало начало новому способу контроля за численностью бактерий. Самое очевидное приложение – фаготерапия, применение бактериофагов для лечения бактериальных инфекций человека. Ее преимуществом является крайняя специфичность фагов, поражающих только «избранные» болезнетворные агенты.
В медицинских целях бактериофаги были впервые применены в 1915 г., когда один из их первооткрывателей, Ф. д’Эрель, использовал такой препарат для лечения дизентерии у детей. Однако дальнейшая история развития фаговой терапии была непростой. Дело в том, что предложения д’Эреля намного опередили свое время, и долгие годы ему пришлось бороться за признание своего открытия. В том числе со знаменитыми французскими коллегами, которые не признавали точку зрения д’Эреля на природу этих бактерицидных агентов, считая их ферментами. Истина восторжествовала лишь в 1940-х гг., но задолго до этого, устав от борьбы, д’Эрель уехал работать в США.
В 1934 г. он приехал в Грузию, в Тбилиси, где к тому времени сложились уникальные возможности для развития фаговой терапии. Еще с 1918 г. там существовала лаборатория (впоследствии − институт) микробиологии, руководитель которой, Г. Элиава, был командирован в знаменитый Институт Пастера для освоения методик и приобретения оборудования. Именно там он и познакомился с д’Эрелем и его удивительным открытием.
Так у Элиавы родилась мечта создать в Тбилиси мировой центр исследования бактериофагов. Эта идея заинтересовала И. В. Сталина, и в 1930 г. было построено и оснащено здание будущего Института бактериофагов, микробиологии и вирусологии, который сейчас носит имя его основателя. Однако далее события развивались по сценарию, характерному для СССР тех лет: в 1937 г. Элиава вместе с женой был арестован и расстрелян как «враг народа», а д’Эрель вернулся в Париж. Однако сам институт не погиб и продолжал успешно функционировать.
С начала 1940-х гг. фаговая терапия начала применяться в странах Европы и США. Такие препараты получили миллионы пациентов, однако результаты лечения оказались противоречивы и невоспроизводимы. Реклама обещала чудеса, но их не было – сама идея фаготерапии была скомпрометирована. Причина заключалась в том, что в то время не только производители препаратов, но и сами ученые не располагали необходимыми знаниями о свойствах фагов и о механизме их действия, да к тому же не имелось и надежных технологий работы с вирусами.
Неудачи следовали за неудачами, поэтому неудивительно, что аптекари и врачи вздохнули с облегчением с появлением антибиотиков. Эти относительно дешевые, с широким спектром антибактериальной активности, хорошо хранящиеся химические вещества, казалось, радикально решили проблему лечения инфекционных заболеваний. Бактериофаги на Западе были забыты на много лет. Основанная д’Эрелем французская компания по выпуску коммерческих фаговых препаратов переключилась на другие проекты (на ее основе выросла знаменитая косметическая компания L’Oreal).
Исследования фагов продолжались только в СССР, Польше и Чехословакии. Самым большим производителем фаговых препаратов был грузинский институт, созданный Элиавой: к 1980-х гг. там работало около 1200 человек, а препараты рассылались для испытаний в клиниках по всему СССР. Производство бактериофагов было организовано также в Уфе и Горьком.
Кстати сказать, в прекращении работ с бактериофагами за рубежом, помимо успеха антибиотиков, большую роль сыграл и политический аспект. Ведь фаговая терапия развивалась в СССР, и западным ученым было политически «неправильным» работать по тематике, связанной с именем Сталина. К тому же это были времена лысенковщины, когда западная наука воспринимала со скептицизмом все, что делалось советскими биологами.
Коктейли из фагов
Новый виток интереса к фаговой терапии пришелся на последние годы. Дело в том, что антибиотики тоже не стали панацеей при лечении бактериальных инфекций: в наши дни разработка новых препаратов не поспевает за ростом числа бактерий с приобретенной устойчивостью к существующим антибиотикам. Уже сегодня в госпиталях Англии около 40 % стафилококковых инфекций вызвано такими штаммами, а в США от госпитальных инфекций, вызванных лекарственно устойчивыми бактериями, ежегодно умирает около 90 тыс. пациентов. При пересчете на население Земли это число составляет 3—5 млн смертей в год!
ВОЗ предупреждает, что мир вскоре вступит в «постантибиотиковую» эру, когда лечить обычные бактериальные инфекции будет нечем. И на этом фоне фаготерапия выглядит весьма перспективным направлением, развитие которого может привести к созданию эффективных персонализированных методов лечения заболеваний. Для этого есть как необходимые знания о фагах и механизмах их взаимодействия с бактериальными клетками, так и технологии работы с вирусными агентами.
Для фаговой терапии сегодня используют только вирулентные лизирующие фаги, в основном «хвостатые» фаги порядка Caudovirales, а также нитчатые фаги семейств Leviviridae (с одноцепочечным РНК-геномом) и Inoviridae (с одноцепочечным кольцевым ДНК-геномом).
Как говорилось выше, спектры активности фагов обычно очень узки и ограничены одним или несколькими близкородственными видами бактерий. С одной стороны, такая узкая специфичность хороша для терапии, поскольку позволяет устранить конкретный микроорганизм, не нарушая всего бактериального сообщества человеческого организма. С другой стороны, при необходимости экстренного лечения (когда нет времени для выявления конкретной бактерии, вызывающей развитие болезнетворного процесса в ране или на обожженной поверхности) необходимо иметь препарат, поражающий сразу несколько видов бактерий, возможных возбудителей инфекции. Для решения этой проблемы обычно используют коктейли фагов – препараты, содержащие несколько фагов, отличающихся по специфичности.
Такой подход использовал еще д’Эрель. Коктейль д’Эреля, привезенный им из Парижа еще в 1930 г., до сих пор является одним из основных фаговых препаратов: он лежит в основе грузинского пиофага и российского интестифага. В Тбилиси на основе фаговых коктейлей разрабатывались препараты для лечения желудочно-кишечных заболеваний и гнойных ран для массового применения в случае возникновения эпидемий или военных действий. Результаты армейских испытаний и широкого эксперимента по предотвращению детских желудочно-кишечных расстройств, проведенного в Тбилиси, показали хорошую эффективность таких препаратов.
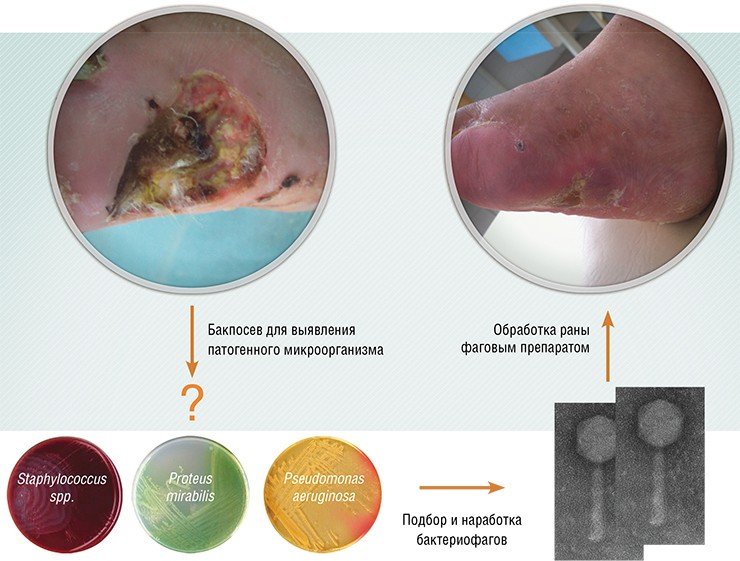
Фаговые коктейли производятся стандартными, и ориентированы они на сообщества бактерий, часто встречающиеся при конкретных заболеваниях. Конечно, более эффективные коктейли получаются в том случае, когда их компоненты подбирают к бактериальному сообществу конкретного пациента. Для получения такого коктейля необходимо протестировать бактерии пациента на чувствительность к фагам из коллекции, чтобы подобрать наиболее эффективные фаговые штаммы. Если нужных фагов в коллекции не окажется, специфичные для бактерий фаги ищут в природных субстратах.
Вообще поиск бактериофагов довольно прост: на бактериальную культуру воздействуют образцами из различных источников: водоемов, почвы, канализационных стоков и т. п. Если бактерии погибают, их отделяют от раствора центрифугированием, а оставшийся раствор тестируют на активность. Затем фаг размножают, выращивая на соответствующей бактериальной культуре. Более того, фаги можно лиофилизировать (высушить в вакууме) и непосредственно использовать в капсулах. В таком виде препарат сохраняют стабильность в течение 14 месяцев при температуре до 55 °С.
Современная история
К настоящему времени самый большой опыт фаготерапии имеют специалисты из Тбилиси и специализированного центра Института иммунологии и экспериментальной терапии им. Л. Хиршфельда (Вроцлав, Польша), где в небольших количествах производятся препараты бактериофагов для испытаний.
Польские исследователи изначально делали акцент на персонализированную терапию. Они использовали фаготерапию для экспериментального лечения пациентов с хроническими заболеваниями, которым не помогают антибиотики. Через центр прошли уже тысячи пациентов, многие из которых были полностью излечены.
Результаты этих клинических испытаний доказали высокую эффективность фагов при лечении инфекционных легочных заболеваний: для подавления инфекции в горле, носу и в легких достаточно однократного интраназального введения препарата. Не менее эффективно фаги элиминируют патогенные бактерии из желудочно-кишечного тракта. Высокая эффективность бактериофагов была также продемонстрирована практически во всех случаях гноеродной язвы диабетической стопы, заболеваний легких, мастита, урогенитальных инфекциях. Список таких заболеваний можно продолжить, при этом важно отметить, что ни в одном из испытаний не наблюдалось каких-либо побочных эффектов, вызванных бактериофагами.
Так, в 2006 г. FDA разрешила применение бактериофаговых коктейлей для обработки мясных и других сельскохозяйственных продуктов. В этом случае фаги получили статус пищевых добавок. Они также были разрешены к применению в качестве средства дезинфекции.
Препараты фагов (в виде аэрозолей) были успешно испытаны в экспериментах по защите сельскохозяйственных птиц на крупных фермах, а также в рыбоводческих хозяйствах
В Англии фаговые препараты были успешно испытаны для лечения хронического отита, трудно излечимого заболевания вследствие образования так называемых бактериальных биофильмов – лекарственно-устойчивых микробных пленок. Во Франции –колыбели фаговой терапии – исследования в этой области сейчас почти не ведутся, хотя до последнего времени Институт Пастера делал фаговые коктейли на заказ.
В промышленных масштабах фаговые препараты сегодня производит российская компания Микроген. Подобные лекарства можно купить в аптеках в России, Белоруссии и на Украине. Фаговые препараты производства Микроген и Тбилисского центра для лечения ожоговых инфекций были успешно испытаны и в Бельгии.
Тем не менее до сих пор в большинстве стран применение бактериофагов в терапии официально не разрешено: это касается как FDA, американского Управления по контролю качества пищевых продуктов и лекарственных препаратов, так и аналогичных европейских агентств. На территории Евросоюза фаги для лечения больных используют только в вышеупомянутом польском Институте иммунологии и экспериментальной терапии.
Поэтому лечение заинтересованных больных проводится в режиме медицинского туризма. Компания «Phage international» (Калифорния, США) направляет пациентов из разных стран, страдающих от хронических заболеваний, вызванных лекарственно устойчивыми бактериями, либо в Центр фаговой терапии в Тбилиси, либо в свою клинику в Мексике.
Выбираем фаги
Почему же фаговая терапия до сих пор не нашла широкого применения? Ведь очевидно, что антибиотики должны быть препаратом выбора при остром, угрожающем жизни заболевании, когда нет времени для подбора специфичного агента. Зато при хронических инфекциях предпочтение следует отдать бактериофагам, как более дружественным агентам.
Среди причин, сдерживающих применения фагов в медицине, в первую очередь следует отметить скептическое отношение многих специалистов, особенно зарубежных. По сложившейся недоброй традиции западные исследователи, несмотря на свое отставание в этой области, до сих пор выражают недоверие к результатам исследований, в свое время успешно проводимых в СССР.
Но есть и более весомые причины, связанные с тем, что в бактериофагах не заинтересованы большие фармацевтические компании. Им нужны исключительные права на изобретения, но фаги – природные агенты, поэтому запатентовать их не так просто, а сама идея фаговой терапии опубликована давно. Кроме того, эти компании вложили огромные средства в производство антибиотиков, поэтому им не нужна конкуренция с дешевыми фаговыми препаратами.
Что касается самих врачей, то они стандартно обучены применять для достижения максимального эффекта антибиотики широкого спектра действия. При фаговой же терапии нужно иметь большой арсенал препаратов, каждый из которых нужно тестировать и подбирать индивидуально для каждого больного. Это в конечном счете приводит к значительному удорожанию такого персонализированного лечения. К тому же хотя люди продолжают умирать от заражения лекарственно устойчивыми бактериями, однако с экономической точки зрения, этот рынок не слишком велик, а лече-ние таких тяжелых больных чревато юридическими проблемами.
Вместе с тем та же FDA сегодня признает, что благодаря своей высокоспецифичности и нетоксичности фаги помогают там, где альтернативные методы оказываются неэффективными. Поэтому FDA планирует выработать практические рекомендации по использованию литических фагов в терапии. Для этого необходимо секвенировать их геномы, определить безопасные условия культивирования, провести современное стандартное тестирование токсичности на животных. В случае использования фаговых коктейлей каждый их компонент должен быть охарактеризован. И, наконец, для доказательства эффективности этих препаратов необходимы контролируемые клинические испытания.
Кстати сказать, применение фагов в медицине может оказаться шире, чем это сегодня представляется. Так, современные технологии позволяют создавать фаги, производящие антибактериальные токсины, которые фаги будут доставлять непосредственно в бактериальную клетку. С помощью генетической инженерии сегодня можно заниматься настоящим дизайном фагов, например, получить фаги с измененной и расширенной специфичностью. Совершенно реалистичной задачей является и полный синтез фаговых геномов.
АНТИБИОТИКИ Достоинства:широкий спектр действия;
простота патентования
Недостатки:
разрушают собственную микрофлору организма,
что создает угрозу вторичных инфекций;
не способны концентрироваться в области
инфекционного поражения;
вызывают побочные эффекты: аллергии, кишечные
расстройства и т. д.;
приводят к возникновению бактериальных штаммов с лекарственной устойчивостью;
создание новых антибиотиков – длительный
и дорогостоящий процесс БАКТЕРИОФАГИ Достоинства:
специфичность действия, для любой бактерии можно найти убивающий ее бактериофаг;
поиск нового фага занимает несколько дней или недель;
производство недорогое и экологически чистое;
не вызывают дисбактериоза;
не токсичны и не вызывают побочных эффектов;
после уничтожения патогенного агента элиминируются из организма
Недостатки:
слишком высокая избирательность – для гарантии
успеха лечения нужно идентифицировать патоген;
патентование затруднено из-за многообразия агентов
Уже испытываются в качестве противобактериальных средств отдельные компоненты фагов и вещества, используемые ими для поражения бактерий. Например, бактериоцины, фрагменты хвостовой структуры фагов, которые повреждают клеточную стенку бактерий, образуя в ней поры, что приводит к быстрой потере важных для клетки ионов и ее гибели.
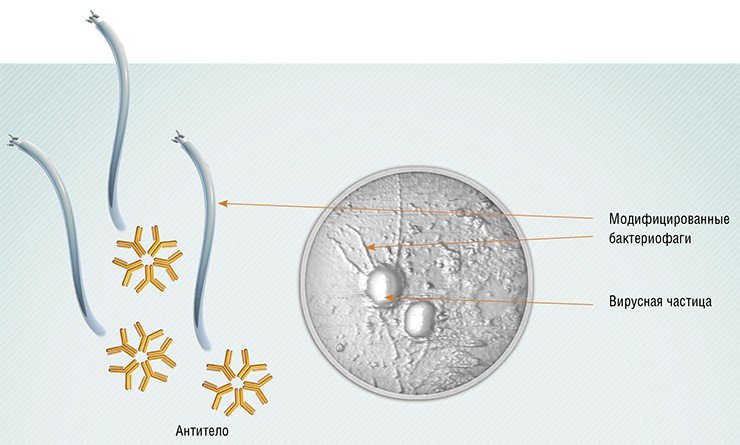
Также разрабатываются подходы к применению фагов в качестве носителей лекарств – антител или химических терапевтических препаратов. На одну фаговую частицу можно присоединить до тысячи молекул антител и до нескольких тысяч молекул антибиотика. А благодаря присоединению к поверхности бактериофагов молекул полиэтиленгликоля удается получать фаги, способные долгое время циркулировать в кровотоке. Кроме того, фаги, несущие на поверхности определенные пептидные антигены, можно использовать в качестве вакцин.
Очевидно, что в XXI в. стимуляция дальнейшего развития фаготерапии должна стать делом государственным. Необходимо создать все условия для создания и поддержания коллекции фагов против устойчивых к антибиотикам патогенов. Что касается всевозможных разрешительных документов, то есть простое решение проблемы: рассматривать фаговые препараты наравне с вакцинами от гриппа. Ведь каждый год готовятся живые противогриппозные вакцины, представляющие собой коктейли нескольких вирусных штаммов, при этом их состав постоянно меняется. И разрешение распространяется на все эти вирусные коктейли, – а чем хуже фаги?
В России сегодня сложилась уникальная ситуация: фаговая терапия у нас разрешена, производится широкий ассортимент «индивидуальных» фаговых препаратов и фаговых коктейлей. Почему же их так редко применяют? Главным образом по причине уже упоминавшейся необходимости персонализированного подхода при фаготерапии. Ведь стандартные фаговые препараты не гарантируют результата, а если препарат не срабатывает, то это не только разочаровывает лечащего врача, но и в случае острого заболевания создает рискованную ситуацию для пациента.
Выход в данной ситуации очевиден: нужно обязательно тестировать бактерии пациента на восприимчивость к фаговому препарату. Это можно делать лишь в хорошо оборудованных центрах, располагающих коллекциями фагов и лабораториями для микробиологического тестирования. Если сеть таких центров будет создаваться в рамках планируемого развития персонализированной медицины, то у нашей страны будут все шансы попасть в лидеры этого важнейшего биомедицинского направления.
Литература
Козлова Ю. Н., Репин В. Е., Анищенко и др. Штамм бактериофага Pseudomonas aeruginosa, используемый в качестве основы для приготовления асептического средства против синегнойной палочки // Патент RU 2455355 C1. 2011.
Тикунова Н. В., Морозова В. В. Фаговый дисплей на основе нитчатых бактериофагов: применение для отбора рекомбинантных антител // Acte Naturae. 2009. № 3б. С. 6—15.
Kropinski A., Lingohr E., Moyles D. et al. Endemic bacteriophages: a cautionary tale for evaluation of bacteriophage therapy and other interventions for infection control in animals // Virology J. 2012. V.9. P. 207—215.
Miedzybrodzki R., Borysowski J., Weber-Dabrowska B. et al. Clinical aspects of phage therapy //Advances in virus res. 2012. V. 83. P. 73—121.
Summers W. Bacteriophage therapy // Annu. Rev. Microbiol. 2001. V. 55. P. 437—451.
Работа была поддержана АНО «Центром Новых Медицинских Технологий» в Академгородке (Новосибирск)