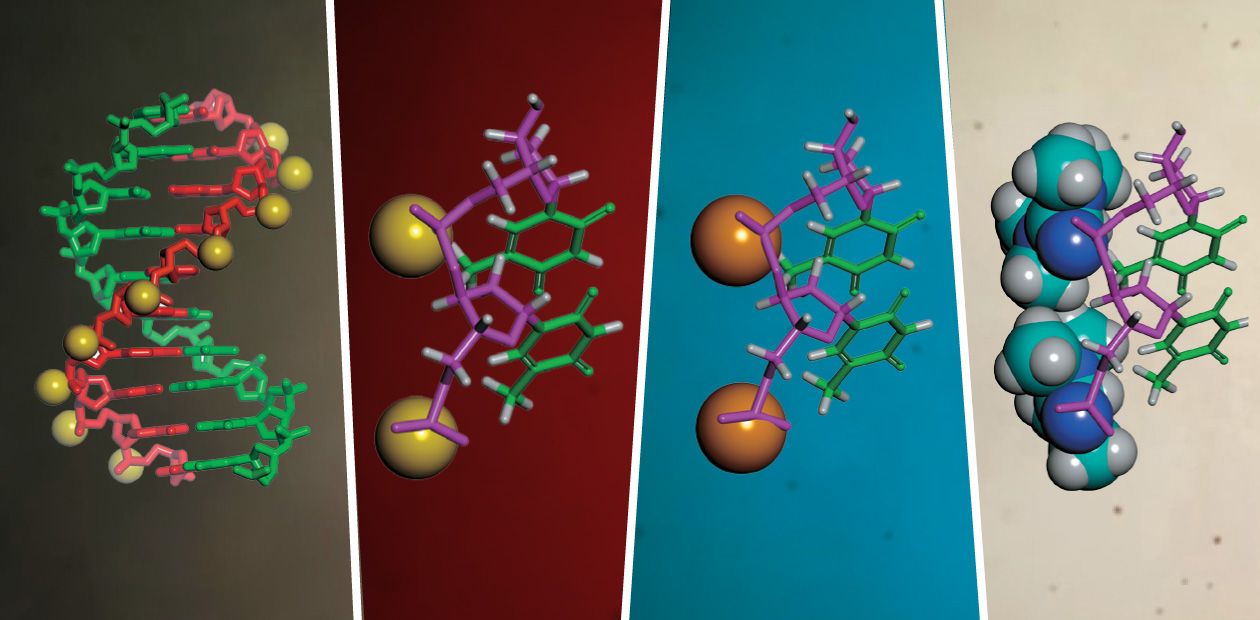
Фосфорилгуанидины – новые химические аналоги нуклеиновых кислот
Новосибирским химикам из Института химической биологии и фундаментальной медицины СО РАН выпала редкая в научном мире удача – им удалось открыть новый класс соединений, не встречающихся в живой природе. Речь идет о фосфорилгуанидинах – аналогах нуклеиновых кислот. Это исследование является прямым продолжением работ новосибирских ученых Н. И. Гриневой и Д. Г. Кнорре, в 1967 г. выдвинувших революционную концепцию терапевтических препаратов на основе олигонуклеотидов (коротких фрагментов нуклеиновых кислот), способных комплементарно связываться с клеточными нуклеиновыми кислотами и направленно влиять на работу генов и перенос генетической информации с ДНК и РНК.
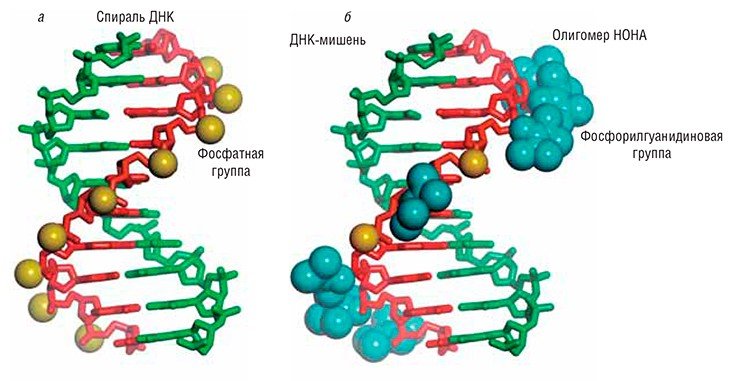
В отличие от обычных нуклеиновых кислот, в новых соединениях «мостиками» между звеньями-нуклеотидами служат не отрицательно заряженные фосфатные, а «нейтральные» фосфорилгуанидиновые группы. Подобная химическая трансформация позволяет им беспрепятственно проникать сквозь липидные мембраны живых клеток, придает устойчивость к разрушающему действию ферментов-нуклеаз и, главное, способность образовывать прочные комплексы в виде двойной спирали с клеточными ДНК и РНК. Благодаря этим свойствам фосфорилгуанидиновые олигонуклеотиды могут стать основой средств медицинской диагностики и лекарственных препаратов нового поколения, способных бросить вызов целому ряду тяжелейших болезней, от которых страдает современное человечество
Сотрудники Института химической биологии и фундаментальной медицины СО РАН (Ноовосибирск) открыли новый класс соединений, которые могут стать основой новых эффективных ген-направленных терапевтических средств
Ex Siberia semper novi – так перефразировал выдающийся русский писатель, ученый и мыслитель советской эпохи Иван Ефремов в своем романе «Лезвие Бритвы» почти забытое в наши дни изречение древнеримского естествоиспытателя Плиния Старшего: ex Africa semper aliquid novi. Переведенное со звонкой латыни на великий и могучий, оно означает: из Африки всегда что-то новое. Вероятно, граждане Древнего Рима в свое время относились к лежащей за морем Африке примерно так, как современные европейцы относятся к Сибири – как к чему-то далекому, таинственному, постоянному источнику неожиданного.
В наше время ефремовское выражение приобретает особый смысл. Ведь Сибирь – это не только кладовая природных ресурсов, источник нефти, газа, золота и алмазов. Главное ее богатство – люди. Люди, которые добывают нефть и газ, моют золото, строят мосты, электростанции и дороги. И отдельное место в созидании окружающего нас рукотворного мира занимают люди науки – по сути, профессиональные первооткрыватели.
Один из важнейших сегментов познания мира занят науками о жизни – биологией и медициной. В этой области ученым надолго хватит работы, ведь человечество все еще остается уязвимым по отношению к целому ряду заболеваний. Причем – глобально уязвимым, о чем жестоко напомнила недавно вспыхнувшая в Африке эпидемия геморрагической лихорадки Эбола.
Можно без ложной скромности сказать, что в сфере биомедицины сибирская наука стоит далеко не на последнем месте. Так было и во время СССР. В 1967 г. в лаборатории химии нуклеиновых кислот Новосибирского института органической химии СО АН СССР (со временем выросшего в нынешний Институт химической биологии и фундаментальной медицины СО РАН), руководимой будущим академиком Д. Г. Кнорре, научный сотрудник Н. И. Гринева выдвинула новую концепцию лечения заболеваний при помощи производных нуклеиновых кислот – олигонуклеотидов.
Эстафету этих открытий приняли нынешние новосибирские химики. Продолжателям дела Гриневой и Кнорре недавно выпала редкая в научном мире удача – им удалось открыть и синтезировать новый класс аналогов нуклеиновых кислот – фосфорилгуанидины (Купрюшкин, Пышный, Стеценко, 2014).
Когда стреляет «незаряженное» ружье
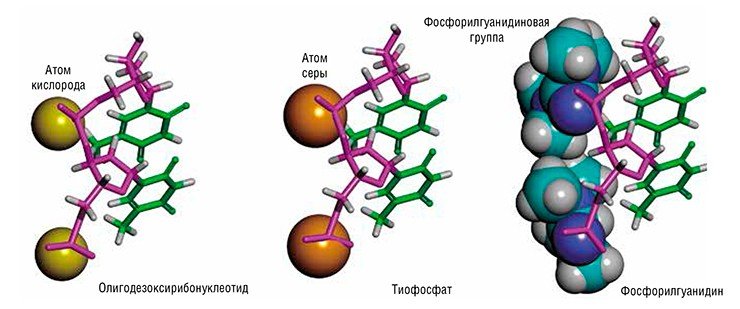
В чем же состоит сходство и различие между обычными нуклеиновыми кислотами и фосфорилгуанидинами? Обычная молекула ДНК или РНК включает в себя отрицательно заряженные фосфатные группы (PO2–), соединяющие между собой соседние нуклеотиды. У аналогов же ДНК, впервые полученных в ИХБФМ СО РАН, место фосфатных групп занимают незаряженные фосфорилгуанидиновые группировки. Низкомолекулярные химические соединения подобной структуры встречаются в живой природе и были впервые синтезированы (кстати, тоже отечественными химиками) еще в 1960-е гг. (Алимов, Левкова, 1964). Однако макромолекулы на основе фосфорилгуанидинов, в частности, производные ДНК или РНК, до сих пор получены не были, и свойства их оставались неизвестными.
Но зачем нам замещать в ДНК отрицательно заряженные фосфаты незаряженными группами? Здесь нужно снова вернуться к природным олигонуклеотидам – относительно коротким цепочкам нуклеиновых кислот, производные которых новосибирские исследователи полвека назад предложили использовать в качестве ген-направленных лекарственных препаратов.
Во-первых, известно, что при попадании в живой организм обычные олигонуклеотиды быстро распознаются и атакуются ферментами, в результате чего распадаются на составляющие звенья за считанные минуты. Поэтому лекарственные средства на основе нуклеиновых кислот должны быть устойчивы к действию ферментов. Во-вторых, чтобы попасть внутрь живой клетки, олигонуклеотиды должны миновать барьер – клеточную мембрану, состоящую преимущественно из липидов. И здесь отрицательный заряд нуклеиновых кислот является скорее помехой, поскольку незаряженным химическим соединениям было бы проще взаимодействовать с неполярными липидными молекулами, составляющими клеточную мембрану.
Так как новые фосфорилгуанидиновые аналоги нуклеиновых кислот не несут отрицательного заряда, то, теоретически, им должно быть проще проникнуть сквозь мембрану в клетку. Что касается их устойчивости к действию ферментов, то и здесь у новых олигомеров все в порядке.
Известно, что в организме за расщепление нуклеиновых кислот отвечают ферменты-нуклеазы. Новые аналоги нуклеиновых кислот сначала прошли испытание на устойчивость к действию одной из наиболее активных нуклеаз – фосфодиэстеразы змеиного яда. Оказалось, что включения в состав олигонуклеотида одной-единственной фосфорилгуанидиновой группы достаточно, чтобы затормозить его расщепление более чем на час, в то время как природный олигонуклеотид полностью расщеплялся менее чем за пять минут. Позднее выяснилось, что олигонуклеотиды, в которых фосфатные группы полностью замещены фосфорилгуанидиновыми, остаются неизменными в среде с высоким содержанием сыворотки в течение как минимум трех суток.
Растворимость в воде у фосфорилгуанидинов, несмотря на их нейтральный характер, достаточно хорошая, что опять-таки немаловажно для лекарственных препаратов.
Будущее с НОНА
Но самое удивительное свойство фосфорилгуанидинов открылось, когда стали искать ответ на, пожалуй, главный вопрос: какова способность новых олигонуклеотидов связываться с целевыми участками нуклеиновых кислот?
Известно, что клеточная молекула ДНК, ответственная за передачу наследственных признаков организма, существует в виде двух цепей, образующих знаменитую двойную спираль. При этом каждый кирпичик ДНК – нуклеотид, связывается только с определенным, подходящим ему нуклеотидом-партнером, образуя комплементарную пару (из четырех нуклеотидов А, С, G и T, входящих в ДНК, «правильными» являются только комплементарные пары А:Т и G:C).
Основой комплементарного связывания служат водородные связи между атомами водорода, азота и кислорода азотистых оснований, входящих в состав нуклеотидов. И в этом смысле комплементарный комплекс олигонуклеотида с участком нуклеиновой кислоты-мишени является как бы уменьшенной моделью двойной спирали ДНК.
Как упоминалось выше, чтобы быть активными в живом организме, олигонуклеотиды нуждаются в защите от действия ферментов-нуклеаз. Для этого природную структуру олигонуклеотидов модифицируют различными химическими группами, которые затрудняют их расщепление ферментами.
В качестве примера подобной химической модификации можно привести замещение одного из атомов кислорода в фосфатной группе на атом серы с образованием тиофосфата. Тиофосфатные олигонуклеотиды проявляют гораздо более высокую устойчивость к действию нуклеаз, чем природные. Однако такие серусодержащие производные, выражаясь языком химиков, при этом проявляют меньшее «желание» (сродство) к образованию комплементарного комплекса с нуклеиновыми кислотами-мишенями. Другими словами, образующиеся в этом случае двойные спирали менее устойчивы, чем такая же по числу нуклеотидов обычная двойная спираль ДНК. Химики связывают это явяление с большим, по сравнению с атомом кислорода, радиусом атома серы.
Интересным является еще одно «приложение» этого названия: НОНА – такое имя было дано универсальной артиллерийской системе, совмещающей в себе функции пушки, гаубицы и миномета. Предположительно, это название является аббревиатурным сокращением от «нового орудия наземной артиллерии». Не правда ли, весьма символично, если учесть, что новые соединения могут стать эффективными и «прицельными» препаратами в нашей извечной борьбе с недугами?
Зато выяснилось, что фосфорилгуанидиновые двойные спирали весьма мало отличаются по стабильности от природной двуцепочечной ДНК. Этот результат можно счесть удивительным, если сравнить размеры фосфорилгуанидиновой группы с размерами атомов серы и кислорода. Поразительно, но фосфорилгуанидиновая группа, несмотря на свой значительный размер, в целом неплохо вписывается в параметры двойной спирали ДНК, не вызывая существенного возмущения ее структуры. Среди множества известных на сегодняшний день химических модификаций фосфатной группы фосфорилгуанидиновая группировка представляет собой, пожалуй, уникальное явление.
Стоит обратить внимание еще на одно полезное свойство фосфорилгуанидинов. Так как замещению гуанидиновой группой подвергается всегда лишь один из атомов кислорода фосфатной группы, остальная часть молекулы нуклеотида остается в полной неприкосновенности и, в свою очередь, может быть подвергнута независимой химической модификации.
Это открывает огромные перспективы получения модифицированных производных олигонуклеотидов с разнообразным набором свойств. В частности, есть возможность сочетать в составе одного олигонуклеотида заряженные участки, содержащие фосфатные или тиофосфатные группы, и незаряженные – с фосфорилгуанидиновыми группами, желаемой протяженности. Это позволило новосибирским химикам сформулировать новую концепцию конструирования олигонуклеотидов НОНА (не полностью заряженные олигонуклеотидные аналоги – non-uniformly charged nucleic acids, NONA). В олигомерах НОНА участки с отрицательным зарядом, несущие, например, фосфатные или тиофосфатные группы, сочетаются с электронейтральными участками, несущими фосфорилгуанидиновые группы.
Как упоминалось выше, частичная или полная нейтрализация отрицательного заряда может пригодиться, в частности, для разработки олигонуклеотидных производных, способных свободно проникать в клетки. Олигомеры НОНА расширяют арсенал научных методов конструирования синтетических нуклеиновых кислот как возможных лекарственных препаратов нового поколения и средств медицинской диагностики.
Сейчас мы находимся еще в самом начале пути к будущим лекарственным препаратам, основой которых могут стать олигонуклеотиды с фосфорилгуанидиновыми группами. Их первооткрыватели надеются, что новые лекарства смогут бросить вызов целому ряду болезней, от которых страдает современное человечество.
Конечно, пока получены только самые первые представители обширного класса фосфорилгуанидиновых производных нуклеиновых кислот, полным ходом идет работа по изучению их биологической активности, в частности, антибактериальных и противовирусных свойств. Хочется пожелать всей команде ИХБФМ СО РАН, занятых этими исследованиями, и дальше поддерживать хорошую традицию: из Сибири – всегда новое!
Литература
Алимов П. И., Левкова Л. Н. // Изд. Акад. Наук СССР. Сер. Хим. 1964. С. 1889.
Власов В. В. Лекарство для генов // НАУКА из первых рук. 2007. № 2(14). С. 56—59.
Власов В. В., Д. В. Пышный, М. А. Зенкова и др. Комплементарные здоровью // НАУКА из первых рук. 2014. № 1 (55). С. 39–49.
Купрюшкин М. С., Пышный Д. В., Стеценко Д. А. Фосфорилгуанидины. Новый класс аналогов нуклеиновых кислот // Acta Naturae. 2014. V. 6. N. 4(23), Р. 53—55.
Belikova A. M., Zarytova V. F., Grineva N. I. Synthesis of ribonucleosides and diribonucleoside phosphates containing 2-chloroethylamine and nitrogen mustard residues. // Tetrahedron Lett. 1967. V. 8. N. 37. P. 3557–3562. doi: 10.1016/S0040-4039(01)89794-X.
Работа поддержана грантом Правительства РФ для научных работ, выполненных под руководством ведущих мировых ученых (№ 14.В25.31.0028)