Конструируем рибонуклеазы. Ножницы-ферменты
В клетках нашего организма – сложно устроенных «химических фабриках» – постоянно происходит бесчисленное множество самых разнообразных биохимических реакций. Причем процессы деструкции, разрушения ненужных или чужеродных для клетки веществ не менее значимы для нее, чем процессы синтеза. Осуществляются они, как правило, с помощью ферментов - природных катализаторов белковой природы...
Рибонуклеиновые кислоты, которые служат матрицами для синтеза белков, являются важнейшим компонентом клеточного биохимического «производства». Однако в некоторых случаях, при инфекциях или других патологических состояниях организма, необходимо остановить процессы синтеза того или иного белка. И один из способов сделать это – разрушить соответствующую РНК с помощью специальных ферментов.
Неудивительно, что ученые начали задумываться о возможности создания на их основе принципиально новых лекарственных препаратов, способных избирательно уничтожать, например, вирусные РНК, не затрагивая при этом жизненно важные рибонуклеиновые кислоты клеток организма.
Все гениальное – просто
Рибонуклеазы – ферменты класса гидролаз, расщепляющие РНК, – широко распространены в клетках всех организмов. Самый известный из них – панкреатическая рибонуклеаза (или РНКаза А), выделенная из поджелудочной железы быка.
Говоря об этом ферменте, постоянно приходится добавлять слово «впервые». РНКаза А – первый ферментный белок, для которого в начале 60-х гг. прошлого века была полностью определена последовательность входящих в его состав аминокислот. А когда в 1969 г. был осуществлен первый химический синтез фермента, им оказалась все та же панкреатическая рибонуклеаза. Более того, она же стала и первым ферментом, вошедшим в медицинскую практику (его используют в качестве противовирусного средства). В качестве отступления заметим что фермент онконаза – аналог РНКазы А, выделенный из ооцитов лягушки Rana pipiens, сегодня является абсолютно новым противораковым препаратом, явный успех клинических испытаний которого позволяет говорить о зарождении нового класса противоопухолевых препаратов – серьезной альтернативе классической химиотерапии.
Природные рибонуклеазы – ферменты, разрушающие ненужную или чужеродную (вирусную) РНК – присутствуют в клетках всех живых организмовСледующей вехой на пути превращения рибонуклеаз в лекарства можно считать 1980-е гг., когда американский биохимик Р. Бреслоу обнаружил, что небольшие молекулы гетероциклического вещества имидазола способны расщеплять РНК подобно природной панкреатической рибонуклеазе. Ему пришла мысль, что можно создать искусственные аналоги ферментов – низкомолекулярные соединения с функциями природных катализаторов. Эта идея была гениальна в своей простоте: для достижения результата достаточно взять каталитически активные группы, встречающиеся в активных центрах природных ферментов, зафиксировать их определенным образом в пространстве – и синтетический аналог фермента готов!
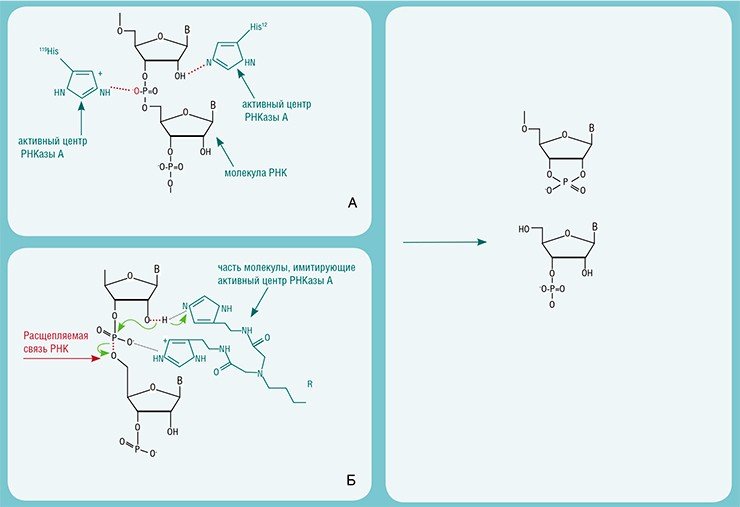
Через несколько лет Р. Бреслоу удалось реализовать высказанную им идею на практике. И хотя полученные им «искусственные» рибонуклеазы были способны расщеплять фосфодиэфирные связи лишь в специально синтезированном для этих целей субстрате, а не в природных РНК, начало было положено.
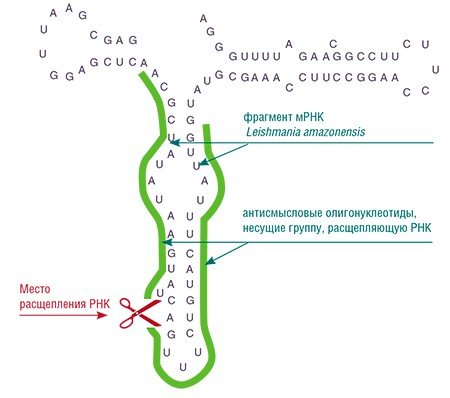
Появление первых работ по искусственным рибонуклеазам совпало с пиком исследований по другой очень интересной тематике – так называемым антисмысловым олигонуклеотидам, работы по которым велись велись в отделе биохимии Института общей химии СО РАН (Новосибирск), возглавляемого академиком Д.Г. Кнорре. Здесь следует пояснить, что более менее протяженные последовательности нуклеиновых кислот являются уникальными по своей структуре. Поэтому на них можно направленно воздействовать комплементарными (антисмысловыми) олигонуклеотидами, которые могут специфично «узнавать» и присоединяться лишь к определенным участкам конкретной нуклеиновой кислоты.
Объединение этих двух технологий – «антисмысловой» и низкомолекулярных искусственных рибонуклеаз – сулило прорыв в производстве синтетических ферментов для медицинских целей. А поскольку хорошие идеи зачастую приходят в голову многим людям одновременно, неудивительно, что работы в этом направлении в 90-х гг. прошлого века начались практически одновременно по всему миру – в Японии, Европе, Соединенных Штатах и России.
Не хуже природных
 К сожалению, в ходе реализации антисмысловой технологии в ее первоначальном варианте обнаружился ряд проблем, в результате чего создание реальных лекарственных препаратов на основе таких соединений отодвинулось на неопределенное время. Эти проблемы касались в первую очередь проникновения синтетических олигонуклеотидных производных сквозь клеточные мембраны, а также их стабильности в живых системах.
К сожалению, в ходе реализации антисмысловой технологии в ее первоначальном варианте обнаружился ряд проблем, в результате чего создание реальных лекарственных препаратов на основе таких соединений отодвинулось на неопределенное время. Эти проблемы касались в первую очередь проникновения синтетических олигонуклеотидных производных сквозь клеточные мембраны, а также их стабильности в живых системах.
Кроме того, на свертывание работ в этом направлении повлияла причина «нетехнологического» характера. Антисмысловая технология на начальном этапе своего становления казалась настолько легко реализуемой, что во всем мире как грибы стали появляться коммерческие фирмы, обещающие создать «панацею» уже в ближайшие годы. В эту область были инвестированы огромные средства; когда же обещанной быстрой отдачи не последовало, компании стали быстро разоряться, произошло и значительное сокращение финансирование фундаментальных исследований. Для российских ученых этот период совпал с общим развалом российской экономики, значительным сокращением финансирования науки в целом.
Аналоги природных ферментов – удобный инструмент для молекулярной биологии и генной инженерииКогда новосибирские ученые из Института химической биологии и фундаментальной медицины СО РАН начинали свою работу в области конструирования искусственных рибонуклеаз на основе олигонуклеотидных конъюгатов, они знали о всех трудностиях, хотя, как и многие в то время, считали их временными. К сожалению, идеальные носители для наших рибонуклеаз – синтетические аналоги нуклеиновых кислот, легко проникающие внутрь клеток и не разрушающиеся под действием природных ферментов, – не созданы до сих пор.
Однако, несмотря на все трудности, работу по созданию искусственных рибонуклеаз ученые не прекратили, начав с моделирования той самой РНКазы А. В лаборатории органического синтеза были синтезированы десятки потенциальных искусственных ферментов. Все они в той или иной степени расщепляли фосфодиэфирные связи в различных молекулах природной РНК, при этом совершенно не затрагивая ДНК. Каждая молекула этих синтетических ферментов была способна катализировать разрушение десятков и сотен связей в РНК.
Искусственные рибонуклеазы могут стать высокоизбирательными малотоксичными лекарственными препаратами для лечения вирусных, онкологических и наследственных заболеванийОкончательно сказать, что структурно-функциональные аналоги РНКазы А созданы, ученые смогли после того, как детально исследовали особенности разрушения РНК в присутствии как природного, так и синтетических ферментов. Дело в том, что помимо высокой эффективности природным ферментам свойственна еще и высокая избирательность действия. Например, РНКаза А наиболее эффективно расщепляет связи в цепочке РНК между нуклеотидами аденином (А) и цитозином (С) и несколько хуже – между аденином и уридином (U). Так вот, оказалось, что искусственные ферменты работали практически также, как и природный.
Конечно, даже самые активные из созданных рибонуклеаз уступают по активности природному ферменту в сотни и даже тысячи раз. Однако если учесть, что РНКаза А ускоряет разрушение РНК в 1014 раз, то и полученные результаты выглядят впечатляюще. В то же время искусственные рибонуклеазы обладают рядом преимуществ: в первую очередь, они очень дешевы по сравнению с природными ферментами. Кроме того, эти соединения очень стабильны и могут работать в широком диапазоне условий.
Универсальные «солдаты»
Где могут найти применение искусственные рибонуклеазы? В первую очередь там, где сейчас используют природные ферменты. Например, в современной биотехнологии – при выделении геномной ДНК, при подготовке ее для ПЦР-анализа, который широко используется в самых различных областях, от медицинской диагностики до криминалистики.

Искусственные рибонуклеазы совершенно инертны по отношению к другим биомолекулам, в частности, белкам. Это их свойство оказалось незаменимым при создании вакцин. Ведь чтобы получить безопасные противовирусные вакцины, вирусные частицы надо «обезоружить», т. е. разрушить их генетический материал. Наиболее часто для этой цели в настоящее время используется формальдегид, сочетающий высокую активность с низкой стоимостью. Однако формальдегид также частично разрушает вирусные белки, а именно: на них в организме при вакцинации вырабатывается иммунный ответ. В результате эффективность вакцинации снижается. Искусственные рибонуклеазы лишены этого недостатка, что подтвердили предварительные эксперименты, проведенные на лабораторных мышах, зараженных вирусом гриппа. Выживаемость животных, получавших подобную вакцину, оказалась существенно выше по сравнению с контрольной группой, вакцинированной стандартным образом.
И наконец, искусственные ферменты могут с успехом заменить природные в исследованиях различных РНК-белковых комплексов. Например, при решении вопроса о том, чем на заре становления жизни определялась специфичность протоферментов – их РНК-связывающим центром, «узнающим» определенные связи в цепочке РНК (как это наблюдается у современных рибонуклеаз) или эту функцию первоначально исполняли их каталитически активные центры? Подобные работы напрямую связаны с одой из важнейших фундаментальных эволюционных проблем – проблемой становления белковой жизни.
Выстрел в десятку
Исследования расщепления протяженных фрагментов РНК (в частности фрагментов генома вируса гриппа) привели к важному открытию: оказалось, что некоторые искусственные рибонуклеазы расщепляют не все принципиально доступные им фосфодиэфирные связи, но лишь те, что находятся в определенных пространственных элементах РНК. Это означало возможность вновь вернуться к идее создания избирательных противовирусных препаратов, но уже на основе низкомолекулярных соединений, без привлечения «антисмысловой» технологии: ферменты сами, без помощников, могли теперь «распознавать» и уничтожать «нужную» РНК!
ГЛОССАРИЙАнтигены – высокомолекулярные коллоидные вещества, которые при введении в организм животных или человека вызывают образование специфических, реагирующих с ними антител.
Антисмысловой олигонуклеотид – молекула РНК или ДНК, полученная в лаборатории и комплементарная по последовательности своей мРНК-мишени. Антисмысловой подход использует такие олигонуклеотиды для подавления экспрессии специфических генов.
Аутоиммунные заболевания – заболевания, при которых иммунная система организма начинает атаковать клетки своего организма.
Вектор – в современной биологии так называют средство доставки чужеродного генетического материала в клетку-мишень. Также вектором называют организм – переносчик болезни.
Гликопротеин – белок, содержащий олигосахаридные цепи, ковалентно присоединенные к полипептидной цепи.
Интерфероны и цитокины – это белки, продуцируемые клетками иммунной системы для регуляции иммунного ответа. Интерфероны принадлежат к классу цитокинов.
Множественная лекарственная устойчивость – состояние, позволяющее болезнетворному организму сопротивляться лечению широким спектром лекарственных препаратов. Такими организмами, проявляющими множественную лекарственную устойчивость могут быть патологические клетки, в том числе бактериальные или раковые.
Моноклональные антитела – это моноспецифические антитела, идентичные между собой в силу того, что они производятся иммунными клетками, являющимися клонами одной родительской клетки. Создание технологии моноклональных антител позволило, в частности, начать применение терапевтических методик на их основе в клинике. Это стало революцией в ряде областей медицины, включая онкологию.
Нокаут гена/cайленсинг – совокупность экспериментальных подходов, позволяющих подавить экспрессию специфического гена-мишени.
Онкоген – ген, участвующий в злокачественной трансформации клетки.
Протоонкоген – это нормальный клеточный ген, который может стать онкогеном из-за мутации или гиперэкспрессии. Обычно протоонкогены кодируют белки, участвующие в росте и дифференцировке клетки.
ПЦР-анализ (ПЦР, полимеразная цепная реакция) – метод современной молекулярной биологии
РНКазомиметик – исскуственный низкомолекулярный аналог фермента РНКаза
Рибозим – олигорибонуклеотид, обладающий ферментативной активностью.
АнтагомикроРНК (antagomiRNA) – антисмысловой олигонуклеотид, антагонист микроРНК, который связывается с регуляторной микроРНК по принципу комплементарности и снимает контролирующее влияние микроРНК на ген-мишень
мРНК – матричная РНК, на которой происходит синтез белков рибосомами
миРНК (microRNA) – микроРНК, малая регуляторная антисмысловая РНК, подавляющая трансляцию гомологичной молекулы мРНК
siРНК (small interfering RNA) – малая интерферирующая РНК. Это малая антисмысловая РНК, которая образуется из специфической двуцепочечной РНК, запускающей механизм РНК-интерференции.
РНК-интерференция – процесс, посредством которого двуцепочечная РНК специфически подавляет экспрессию гомологичного гена
Триплексная технология – наиболее современный из антисмысловых подходов, в котором антисмысловой олигонуклеотид связывается с двуцепочечной ДНК не по принципу комплементарности оснований Уотсона-Крика, а на основе так называемого спаривания Хугстина. Эта технология позволяет регулировать экспрессию гена не на уровне трансляции, как другие антисмысловые технологии, но на уровне транскрипции. Она также позволяет навсегда подавить экспрессию гена или вносить в него мутации.
К сожалению, в успех этого мероприятия мало кто верил, да и сами полномасштабные испытания противирусной активности — дорогое удовольствие. Помог случай: на одной из научных конференций новосибирские ученые встретились с вирусологами из Одесского противочумного института, которые согласились провести испытания пятнадцати новых соединений. И это был, что называется, выстрел в десятку: десять из испытанных соединений показали четко выраженную противогриппозную активность. Более того, эффективность четырех из них была сопоставима или даже превышала эффективность таких известных лекарственных препаратов, как ремантадин и дейтефорин в 50—100 раз! Это был безусловный успех, учитывая низкую токсичность испытанных рибонуклеаз.
Эти работы вызвали живой интерес со стороны не только украинских, но и белорусских, и итальянских коллег, а также некоторых фармацевтических компаний. Заинтересованность проявили и региональные власти. Но самой высокой оценкой своей работы сами ученые считают слова легендарного «отца-основателя» искусственных ферментов Р. Бреслоу, высказанные им на недавнем международном симпозиуме: «Я восхищен новосибирскими химиками, сумевшими получить такие результаты!»
Литература
Зенков М. А., Сильников В. Н., Власов В. В. Химические рибонуклеазы // Молекулярная биология. 1998. Т. 32. № 1. С. 62—70.
Гарипова И. Ю., Сильников В. Н. Сайт-специфичные синтетические рибонуклеазы на основе конъюгатов олигонуклеотидов с металлонезависимыми органическими катализаторами гидролиза фосфодиэфирных связей // Известия АН. Серия химическая. 2002. № 7. С. 1025—1030
Сильников В. Н., Власов В. В. Конструирование реагентов для направленного расщепления рибонуклеиновых кислот // Успехи химии. 2001. Т. 70. № 6. С. 562—580.
Kuznetsova I. L., Silnikov V. N. Small ribonuclease mimics. Ed. Marina A. Zenkova «Artificial Nucleases» in Nucleic Acids and Molecular Biology. 2004. V. 13. P. 111—128, Springer Verlag Berlin.





