Кошки и гены: 30 лет спустя
Некоторые ученые всю жизнь занимаются одним-единственным объектом и одной-единственной проблемой. Меня же все время носило из стороны в сторону. Одним из таких «заносов» было увлечение кошками. Не могу сказать, что я их страстный любитель... Но я посвятил этим домашним хищникам изрядную часть своего свободного времени, потому что их генетика оказалась безумно интересной. Да и знакомиться с наукой о наследственности намного увлекательнее на таком обаятельном объекте, чем на классической мушке-дрозофиле
Все началось много лет назад, еще в бытность мою студентом НГУ. В качестве домашнего задания по английскому языку нужно было приготовить пересказ научной статьи, причем такой, что была бы интересной моим согруппникам. При просмотре журналов мне бросилось в глаза фото на обложке Journal of Heredity с изображением фонтана на городской площади. Там, вокруг фонтана и на нем самом сидели, стояли и гуляли 94 кошки! Фотография отсылала к статье под названием «Некоторые коты из Сан-Паулу, Бразилия» – одной из цикла статей, посвященных геногеографии кошек.
Кошки оказались идеальным объектом для подобных исследований благодаря тому, что в их популяциях с высокой частотой встречаются мутанты по разным генам окраски (серые, черные, белые, рыжие, пятнистые и т. д.). Еще в конце 1940-х гг. на это явление обратил внимание великий английский генетик Дж. Б. С. Холдейн, и по его инициативе по всему миру генетики начали считать кошек. В итоге стала прорисовываться всемирная кошачья геногеографическая карта. Сравнение разных популяций по частотам генов окраски проливало свет на эволюцию кошки и факторы, которые ее определяли: естественный и искусственный отбор, миграции, изоляция, дрейф генов.
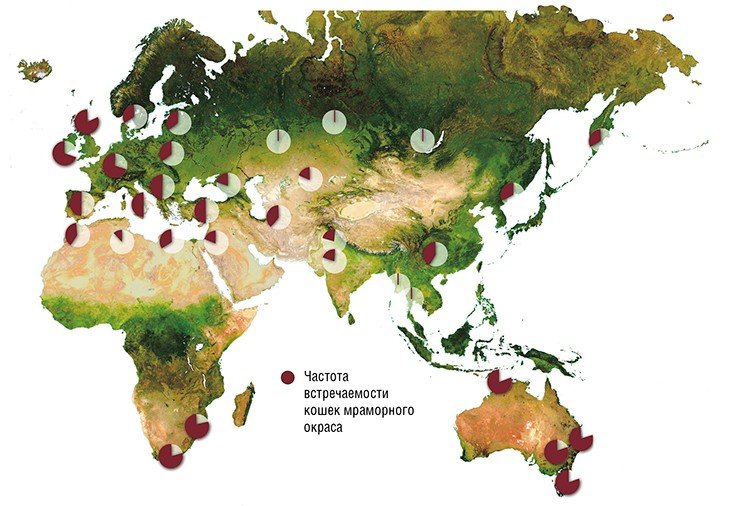
У этой карты был один недостаток: вся наша страна (тогда СССР) была изображена сплошным белым пятном. Естественно, я взялся этот недостаток восполнить. Сначала я пересчитал кошек в Академгородке, а затем во всех городах нашей необъятной Родины, куда меня заносила судьба.
Сам подсчет кошек был страшно увлекательным, азартным и даже в некотором роде опасным занятием. Приходилось считаться не только с самими зверями, но и общественным мнением – ведь человек, что-то высматривающий и вынюхивающий во дворах и подворотнях, вызывает обоснованные подозрения. В лучшем случае его принимают за налогового инспектора, в худшем – за иностранного агента. А когда этот человек потом достает записную книжку и что-то в нее записывает, то крепнущие подозрения могут привести к крайне нежелательным последствиям.
Поэтому котов мне приходилось наблюдать и регистрировать незаметно, по возможности – на ходу, и не замедляя шаг. Когда в моей памяти «накапливалось» более пяти котов, я заходил в телефон-автомат, снимал трубку и просил мифическую Марью Ивановну продиктовать телефон не менее мифического Ивана Ивановича. После этого я спокойно записывал информацию в книжку, благодарил Марью Ивановну и вешал трубку.
Затем я попытался расширить масштаб своих геногеографических операций, завербовав многомиллионные массы советских школьников. Для этого сделал учебный фильм на Центральном телевидении, где с самой красивой дикторшей телевидения Инной Ермиловой гулял по Москве и якобы случайно встречал кошек. Я диагностировал их по генотипам, а Инна регистрировала.

На самом деле вся операция была построена по принципу «рояль в кустах». Усилиями нашего режиссера были мобилизованы учителя биологии из нескольких московских школ. В свою очередь, они мобилизовали своих учеников, выдали каждому по пузырьку валерьянки и послали на отлов бродячих кошек. Нас с Инной на казенном микроавтобусе привозили «на точку». Мы становились в задумчивые позы (я – весь в белом, она – в красном), режиссер командовал «Мотор!», и в этот момент очередной школьник выпускал на нас очередного кота.
После этого школьники со всех концов нашей Родины прислали мне три мешка писем с описаниями локальных популяций кошек. Письма были замечательными, но научно малоинформативными. Пришлось рекрутировать специалистов – коллег-генетиков.
Плодом всех трудов стали две научные статьи в тот же Journal of Heredity и монография «Генетика кошки». Увлекшись, я написал и две научно-популярные книжки – «Этюды о мутантах» (1983) и «Кошки и гены» (1995).
Кроме всего прочего, я написал еще две научно-популярные статьи для журнала «Химия и жизнь». Первая из них под названием «Кошки, гены и география» вышла в 1979 г., вторая – «Кошки и гены: 10 лет спустя» – в 1989 г. Так что нынешнюю поневоле пришлось назвать «Кошки и гены: 30 лет спустя».
Кошачьи хромосомы
 Что же произошло в генетике домашней кошки за последние 20 лет? С одной стороны, ситуация с геногеографией практически не изменилась. Глобальные карты стали достаточно информативными уже 20 лет назад, и добавление новых данных перестало влиять на интерпретацию. Поэтому публикации по этой теме постепенно сошли на нет. С другой стороны, за истекшее десятилетие в генетике кошки произошли важные события, связанные в том числе и развитием методов секвенирования геномов.
Что же произошло в генетике домашней кошки за последние 20 лет? С одной стороны, ситуация с геногеографией практически не изменилась. Глобальные карты стали достаточно информативными уже 20 лет назад, и добавление новых данных перестало влиять на интерпретацию. Поэтому публикации по этой теме постепенно сошли на нет. С другой стороны, за истекшее десятилетие в генетике кошки произошли важные события, связанные в том числе и развитием методов секвенирования геномов.
Первые результаты расшифровки генома кошки появились в 2007 г. Пока расшифровано примерно 65 % кошачьих генов. Сравнение генома кошки с хорошо исследованными геномами человека, шимпанзе, собаки, коровы, мыши и крысы позволило идентифицировать у нее 20 285 генов. Следовательно, общее число генов кошки, по-видимому, близко к количеству генов человека, т. е. тридцати тысячам.
Очень интересные и неожиданные результаты дало сравнение генетического состава хромосом кошки и других млекопитающих. Оказалось, что кошка, как и человек, довольно незначительно перестроила свои хромосомы за 80—90 млн лет эволюции от общего предка.
При этом, несмотря на то, что хромосомы кошки выглядят крайне консервативными в макроэволюционном контексте, они оказались чемпионами среди хромосом млекопитающих по частоте генетической рекомбинации – перераспределения генов путем обмена участками парных хромосом. А, как известно, рекомбинация является главным поставщиком новых сочетаний генов, которые являются базой для естественного отбора, микро- и макроэволюционных процессов.
Оказалось, что по плотности рекомбинационных событий, т. е. обменов отдельными фрагментами цепочек ДНК на единицу длины хромосомы, кошка занимает первое место среди всех изученных млекопитающих. Среднее расстояние между точками рекомбинации у кошки равно 3,7 мкм (для сравнения: у мыши – 7,1 мкм, у человека – 6,0 мкм). При этом нижний предел этого расстояния составляет всего 0,05 мкм, т. е. на грани разрешения микроскопа.
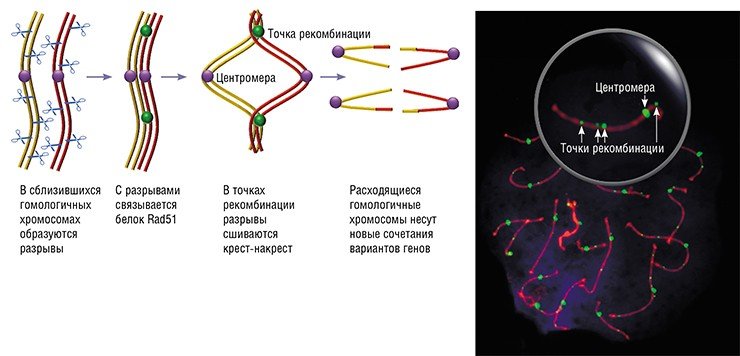
При подготовке к первому делению гомологичные (парные) хромосомы сближаются и выравниваются по длине. В это время в их ДНК возникают множественные двунитевые разрывы. В воссоединении разорванных нитей ДНК активно участвует белок Rad51, который связывается со свободными концами разорванных ДНК и внедряет их в ДНК гомологичных хромосом, одновременно расплетая ДНК-мишень.
Найдя комплементарный участок, внедрившаяся нить ДНК с ним спаривается. Однако большая часть связок между ДНК разрезается и сшивается так, что восстанавливается исходное состояние цепей ДНК (безобменный путь). У всех исследованных млекопитающих (кроме кошки!) лишь менее десяти процентов связок сшивается крест-накрест (обменный путь). При этом ДНК одного из гомологов в пунктах обмена соединяется с ДНК другого. Это и есть точки рекомбинации.
Опознавательным знаком для точек рекомбинации служит белок MLH1, принадлежащий к семейству белков репарации, чья функция – исправлять ошибки спаривания ДНК, т. е. устранять неспаренные нуклеотиды. С помощью антител к MLH1, меченных флуоресцентными красителями, можно проанализировать частоту и распределение рекомбинационных событий по геному
Высокая плотность рекомбинации у кошки сопряжена с высокой эффективностью этого процесса. У всех других исследованных млекопитающих только небольшая (меньше 10 %) часть первичных связок между ДНК гомологичных хромосом сшивается крест-накрест, приводя к образованию рекомбинантных хромосом. У кошки доля связок, разрешаемых по рекомбинантному пути, составляет 25 %. То есть процесс рекомбинации у кошки организован более экономично, чем у других млекопитающих: при меньшем числе двунитевых разрывов ДНК он обеспечивает достаточно высокий уровень рекомбинации.
Сиамская замена
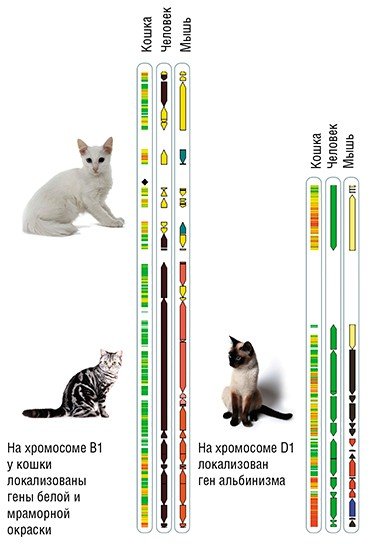
Двадцать лет назад генетическая карта хромосом кошки содержала всего несколько десятков генов; сейчас их число приближается к двум тысячам. В том числе картированы и расшифрованы гены окраски и выявлены критические точки, мутации в которых приводят к ее изменениям.
Так, на одной из соматических (неполовых) хромосом локализованы две мутации по окраске. Мутация доминантной белой окраски, находящаяся в протоонкогене с-kit, нарушает способность к миграции у меланобластов – предшественников пигментных клеток эмбриона. И поскольку меланобласты не успевают достигнуть вовремя кожи, пигмент не попадает в волоски. В результате шерсть вырастает совершенно белой. Если же иногда меланобластам все же удается внедриться в волосяные фолликулы, расположенные на голове кошки, то там появляются небольшие окрашенные участки. У носителей этой мутации количество меланобластов, достигших сетчатки глаза, может различаться. Если их много, то глаза будут иметь нормальный желтый цвет, если очень мало – голубой.

В той же хромосоме находится ген, задающий рисунок окраса. Нормальный аллель (структурная форма) этого гена дает полосатую, тигровую окраску. Иногда эти полосы сплошные, иногда – разорванные. Известна полудоминантная мутация абиссинский тэбби. У гомозигот (т. е. у особей, имеющих пару ¬одинаковых аллелей) по этой мутации никаких полос на теле не обнаруживается: звери имеют однородную окраску. А вот у гетерозигот по этой мутации полосы располагаются на хвосте, морде и лапах. Рецессивная мутация в том же гене – мраморный тэбби – превращает поперечные полосы в завитки или разводы неправильной формы. Часто у таких котов по спине тянется широкая черная полоса.
При альбинизме – явлении, широко встречающемся у разных видов млекопитающих, – имеются мутации в гене, кодирующем фермент тирозиназу. При этом синтез фермента либо полностью блокируется, либо синтезируется дефектный фермент с измененной активностью.
У кошек описано несколько таких мутаций. У гомозигот по мутации бирманского альбинизма активность тирозиназы несколько снижена по сравнению с нормой. Причем степень подавления активности фермента зависит от температуры тела: при более низкой по сравнению с нормальной температурой он более активен. Именно поэтому у бирманских кошек более интенсивно окрашены участки шерсти на кончиках лап, хвоста, ушей, на носу, то есть в тех районах тела, где температура понижена.
То же самое можно сказать и относительно мутации сиамского альбинизма. Однако уровень депигментации при этом гораздо выше: у сиамских кошек шерсть на туловище, как правило, не имеет пигмента, а окраска сохраняется лишь на кончиках лап, хвоста, на ушах и на носу. Но даже и эти участки пигментированы слабее, чем у бирманских кошек. Глаза, как правило, голубые из-за снижения количества пигмента в сетчатке.

Сейчас мы точно знаем молекулярную природу этих мутаций: они получаются благодаря замене в генной последовательности одного-единственного нуклеотида! У сиамских кошек в гене, ответственном за синтез тирозиназы, заменяется нуклеотид, стоящий в 422-й позиции от начала гена. У нормальных кошек там находится гуанин, у сиамских – аденин. В результате последовательность нуклеотидов, кодирующая аминокислоту аргинин, превратилась в последовательность, кодирующую глицин. Замена аргинина на глицин в белке тирозиназе привела к снижению его ферментативной активности при нормальной температуре тела.
У бирманских кошек аналогичное ослабление окраски на теле обусловлено заменой нуклеотида в 227-й позиции.
Родственница лошади
Детальный анализ геномов кошки и других млекопитающих привел к радикальному пересмотру всего родословного древа млекопитающих. До этого филогенетическое древо выглядело вовсе даже не как древо, а как куст, у котором все ветви – отряды – отходили от одного корня. Сейчас на нашем общем родословном древе мы можем различать последовательные ветвления.
Выделяются три главные ветви: афротерии (слоны, сирены, даманы, трубкозубы, златокроты и др.), неполнозубые (эндемики Южной Америки – броненосцы, ленивцы и муравьеды) и лавразиотерии (все остальные плацентарные млекопитающие). Эти три ствола образовались из-за раскола древнего мегаматерика Пангеи на Гондвану (современные Африка, Индия, Южная Америка, Антарктида и Австралия) и Лавразию (соответственно Евразия и Северная Америка). Гондвана затем раскололась на составляющие материки, причем первой отделилась Африка. На этом изолированном континенте и появился надотряд афротериев.
Интересующие нас кошки входят в отряд хищных, который принадлежит к ветви лавразиотериев, включающей наибольшее число видов. Дальнейшее ветвление приводит, в числе прочего, к хищно-копытно-рукокрылым млекопитающим. И как бы ни безумно выглядела эта группа, ее общее происхождение убедительно подтверждается молекулярным данными. Более того, эти же данные показывают, что дальнейшее ветвление внутри этой группы происходило вовсе не так, как можно было бы заключить из внешнего облика животных, ее составляющих.
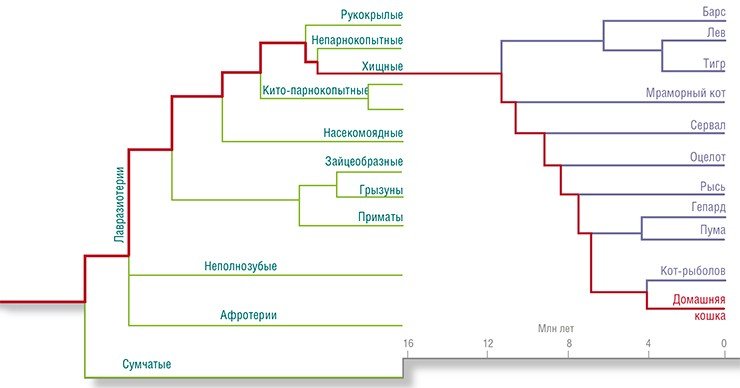
Первыми отделились кито-парнокопытные. (Это не опечатка: именно так – кито-парнокопытные. В старом, «домолекулярном» древе китов выводили прямо от корня куста млекопитающих. Сейчас оказалось, что ближайшим родственником китов является бегемот). Другая ветвь – пегасохищные – ветвится на непарнокопытных (лошади, тапиры, носороги), хищных (кошки, собаки, медведи, моржи и др.) и рукокрылых (летучие мыши).
Порядок ветвления в пределах надотряда пегасохищных пока не вполне понятен, но есть указания на то, что первыми выделились рукокрылые, а уже потом произошло разделение непарнокопытных и хищных. Но что совершенно определенно, так это то, что последний общий предок лошади и кошки существовал позже (т. е. ближе к нашему времени), чем последний общий предок лошади и коровы.
Родословное древо самих кошачьих было также существенно пересмотрено за последние 20 лет. Выяснилось, что первое разделение этого семейства произошло около 11 млн лет назад в Азии, когда от него отделилась линия больших рычащих кошек (лев, тигр, леопард, ягуар и снежный барс). Многие виды, принадлежащие к этой группе, имеют практически идентичные хромосомные наборы. В природе они сохраняются как отдельные виды, но в неволе от них легко получить гибридное потомство. Многие зоопарки имеют тигрольвиц, лигров и т. д. И хотя большинство из них стерильно, сама возможность получения жизнеспособных гибридов между этими видами указывает на большое генетическое сходство рычащих кошек друг с другом.
Почему у Копирки Нет Рыжих Пятен?В зиготе – клетке, образующейся при слиянии яйцеклетки и сперматозоида, – активны обе Х-хромосомы. В ходе клеточных делений и последующей дифференцировки во всех клетках тела, в том числе в будущих пигментных клетках, одна из Х-хромосом инактивируется. Если кошка гетерозиготна по гену окраски, то в одних клетках может инактивироваться хромосома, несущая аллель рыжей окраски, в других – несущая аллель черной окраски. Дочерние клетки строго наследуют состояние Х-хромосомы. В результате формируется черепаховая окраска.
Очевидно, что при клонировании в ядре реконструированной яйцеклетки, взятом из обычной соматической клетки трехцветной кошки, не произошла полная реактивация выключенной Х-хромосомы
Вторая группа, выделившаяся тоже в Азии, состоит из мраморного кота и азиатской золотистой кошки, ныне обитающих в Юго-Восточной Азии. От этой линии отделилась и мигрировала в Африку ветвь, к которой относится сервал, каракал и африканская золотистая кошка. Это произошло 6–10 млн лет назад, когда уровень мирового океана был довольно низким, и между Африкой и Азией существовала перемычка в районе современного Красного моря.
В это же время остальные кошки широко расселились по Азии, а часть их перешла по Берингийскому мосту в Северную Америку. Именно там находят самые древние останки рыси, оцелота и пумы. Затем потомки североамериканцев мигрировали назад в Азию и затем в Африку, где дали начало евроазиатской рыси и африканскому гепарду. В конце плиоцена (2–3 млн лет назад) образовался Панамский перешеек между Северной и Южной Америкой. В Южную Америку проникла линия оцелота и дала начало семи новым видам кошек. Туда же перебрались из Северной Америки пума и ягуар.

Разделение остальных азиатских кошек на отдельные роды и виды произошло в Евразии в течение последних 5 млн лет. Именно к этой группе принадлежит домашняя кошка.
Сколько жизней у кошки?
Как известно, первым клонированным животным стала овца: знаменитая Долли родилась в 1996 г. Через пять лет на свет появилась первая клонированная кошка, метко названная CC (Carbon Copy) или, по-русски, Копиркой.
Оригиналом для копирования выбрали черепаховую (серо-рыжую) кошку с белым пятном по имени Радуга. Из ее яичника были выделены яйцеклетки и обычные соматические клетки. Из каждой яйцеклетки удалили ядро и заместили его ядром, выделенным из соматической клетки. После стимуляции электрошоком реконструированные яйцеклетки трансплантировали в матку серой полосатой кошки. От этой суррогатной матери и родилась Копирка (Shin et al., 2002).
По генотипу Копирка была точной копией Радуги, но вот по внешнему виду она отличалась от оригинала: у нее не было рыжих пятен. Авторы статьи в Nature довольно уклончиво объясняли это различие: «Характер пигментации у многоцветных животных определяется не только генетическими факторами, но факторами развития, не контролируемыми генотипом».
Такое высказывание можно понимать как угодно. Я это понимаю так. В соматической клетке, из которой взято ядро для создания Копирки, была инактивирована одна из двух половых Х-хромосом – та, которая как раз и несла аллель рыжей окраски. А, как известно, состояние Х-хромосомы стойко передается в поколениях соматических клеток.
В случае с Копиркой поразительно то, что перенос ядра соматической клетки в яйцеклетку не привел к реактивации Х-хромосомы. Следовательно, процедура клонирования не приводит к полному репрограммированию ядра. Может быть, с этим явлением связаны и проблемы со здоровьем и размножением у клонированных животных. Правда, Копирка на здоровье не жалуется. Ей сейчас уже 8 лет, а три года назад она стала счастливой матерью трех котят.
Компания Genetic Savings & Clone, финансировавшая создание Копирки, попыталась сделать на этом бизнес. К сожалению, клиент не пошел: удалось продать только двух клонированных домашних любимцев (за 50 и 32 тыс. долл.), и на этом дело закончилось.
Однако эстафету подхватили в Южной Корее: первая кошка была клонирована там в 2004 г. Корейские исследователи рассматривали ее клонирование не как самоцель, а как промежуточный этап в решении другой, гораздо более амбициозной задачи.
Их интересовало получение GM (генетически модифицированных) кошек. Для этого они выделили клетки соединительной ткани – фибробласты – из уха белого ангорского кота. Фибробласты культивировали в питательной среде, в которую был добавлен ¬мобильный генетический элемент, содержащий ген, который кодировал красный флуоресцентный белок.
После того как мобильный элемент проник в ядра фибробластов и встроился в хозяйскую ДНК, эти ядра выделили и перенесли в яйцеклетки, из которых предварительно удалили собственные ядра. Из этих реконструированных яйцеклеток развились два GM котенка, у которых красный флуоресцентный белок синтезируется практически во всех клетках тела. В результате под ультрафиолетовым излучением эти коты светятся мистическим красным светом (Yin et al., 2008). В статье, опубликованной в 2008 г. в журнале Biology of Reproduction, особенно интригует последняя фраза: «Данная технология будет полезна для направленного создания дизайнерских котов».
Трудно представить, сколько будут стоить подобные дизайнерские GM коты и кому они могут понадобиться. При этом меня ничуть не пугают генетически модифицированные кошки. Ведь если подумать хорошенько, то все кошки в мире были генетически модифицированы за долгие поколения естественного и искусственного отбора, которому подвергались их предки.
P.S. Памятуя о последствиях своей научно-популярной деятельности, сообщаю, что котов не клонирую, генетически не модифицирую, рекомендаций по случке не даю и котенка в мои руки прошу не предлагать.
Литература
Бородин П. М. Этюды о мутантах. М.: Знание, 1983
Бородин П. М., Рувинский А. О. Генетика кошки. Новосибирск: Наука, 1992
Бородин П. М. Кошки и гены. ЗАО Зоосалон, 1995.
Бородин П. М. Кошки, гены и география. // Химия и жизнь. 1979. № 4. С. 40—46
Бородин П. М. Кошки и гены: десять лет спустя. // Химия и жизнь. 1989. № 4. С. 40—45
Shin T, Kraemer D, Pryor J, Liu L, Rugila J, Howe L et al. A cat cloned by nuclear transplantation. // Nature. – 2002. V. 415(6874). – P. 859.
Работа по анализу рекомбинации у кошек выполнена при поддержке гранта РФФИ № 04-04-48024-a
Автор и редакция благодарят И. Бодунова (Клуб любителей кошек «Азия», Новосибирск), М. Вестузина и Л. Вэдсворта (Texas A&M College of Veterinary Medicine, College-Station) за помощь в подготовке иллюстраций