Легко ли Быть Создателем? Реалии трансгенеза растений
Беспрецедентный в человеческой истории научно-технический и технологический взрыв, ознаменовавший конец второго тысячелетия, не обошел и такую традиционную область знания, как биология. Это произошло благодаря рождению новых дисциплин – генетики и ее «дочери» – молекулярной биологии, что позволило манипулировать с носителями наследственной информации, молекулами ДНК, вне живой клетки. Ученые стали генными инженерами и биотехнологами. Используя методы генетической трансформации и культивирования клеток и тканей, они научились создавать «новые» организмы, взяв на себя роль если не бога, то эволюционного процесса
Голубые розы, золотой рис…
Достижения в области генной инженерии растений достаточно быстро нашли применение в практике. Так, первые трансгенные растения были созданы в начале 1980-х годов, а через десять лет в Китае уже промышленно выращивали трансгенный табак, устойчивый к гербицидам. В настоящее время мы наблюдаем крупномасштабный выход новых сортов, созданных на основе генетически модифицированных растений; число же видов, на основе которых они были получены, приближается к двумстам!
Использование генно-инженерных методов для переноса генов, определяющих потребительски ценные признаки, открыло большие перспективы для улучшения главных сельскохозяйственных культур. Созданы трансгенные растения, устойчивые к гербицидам, к насекомым-вредителям, вирусам и болезням; растения со сбалансированным составом аминокислот и измененным составом жирных кислот; декоративные сорта с измененной окраской цветов (например, гвоздики, розы и хризантемы голубого цвета).

Можно привести и совершенно потрясающие примеры. В частности, у африканских деревьев (Dioscoreophyllum cumminisii и Thaumatococcus danielli) были обнаружены удивительные белки – монеллин и таутаматин – которые в тысячу раз слаще сахара. Гены, контролирующие синтез этих белков, при переносе в другие виды растений (например, клубнику или яблоню) обеспечивают их плодам необычную сладость. А поскольку сладкая компонента представлена здесь не углеводами, а белком, такие растения будут настоящей находкой для больных диабетом, не говоря уж о людях, страдающих избыточным весом.
Крупнейшим успехом генной инженерии явилось создание под руководством швейцарского профессора И. Потрикуса нового сорта риса с повышенным содержанием провитамина А, железа и фолиевой кислоты. Употребление такого «золотого риса» позволит компенсировать нехватку витамина А в повседневном рационе, особенно в странах, испытывающих его дефицит. Еще один сорт риса – высокопродуктивный, устойчивый к засухе и засолению почв – создали американские ученые из Корнельского университета. Они перенесли в растительный геном от обычной кишечной палочки (Echerihia coli) два гена, контролирующих синтез углевода трегалозы, который и обеспечивает высокую устойчивость растений, как к высоким, так и низким температурам.
Пищевые и декоративные трансгенные растения уже пользуются широкой известностью. Кроме того, растет интерес к трансгенным растениям как биопродуцентам новых материалов, биологически активных веществ и лекарственных препаратов. Они могли бы стать более дешевым и безопасным источником различных белков медицинского назначения по сравнению с традиционными системами с использованием бактерий, дрожжей, клеточных культур насекомых и млекопитающих. Одно из перспективных направлений – создание трансгенных «съедобных вакцин» для повышения иммунитета у животных и человека.
Потенциальная сфера применения трансгенных растений необычайно широка. Например, уже созданы растения для очищения окружающей среды от различного рода загрязнений, в том числе тяжелых металлов, для биодеградации полимеров и т. д. Сейчас в научно-исследовательских лабораториях мира разрабатываются все новые и новые проекты, поражающие дерзостью замыслов.
Трансгены наступают!
Но перейдем от слов к цифрам – оценим долю генетически модифицированных растений в общемировом «пироге» основных сельскохозяйственных культур.
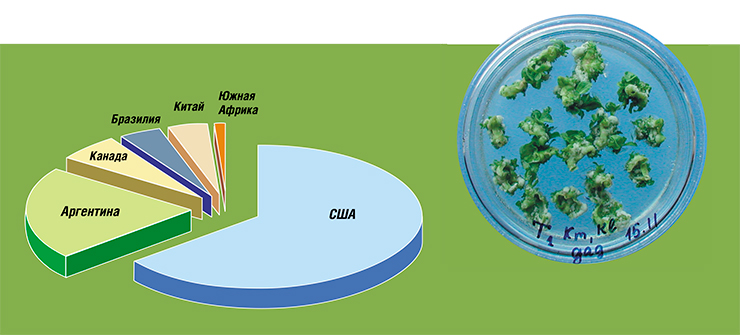
Сухие статистические сводки отчетливо демонстрируют наступление трансгенных растений на поля производителей. Так, за 8-летний период (1996–2003 гг.) мировые площади под этими культурами возросли в 40 раз, составив более 67 млн га. К 2003 году уже около 7 млн фермеров в 18 странах размещали трансгенные растения на своих полях.

ГМ-культуры выращиваются для коммерческих целей в Южной Африке и Австралии, Индии и Румынии, Уругвае и Испании, в Мексике и на Филиппинах, в Колумбии, Болгарии, Гондурасе, Германии и Индонезии. Главными производителями таких культур в мире считаются США, Аргентина, Канада, Бразилия и Китай. Кстати, обратите внимание, – нашего отечества в этом списке нет!
Среди стран, выращивающих трансгенные растения – 7 индустриальных и 11 развивающихся, причем на долю последних приходится около одной трети всех площадей (20 млн га), занятых трансгенными культурами. Доминируют сорта, устойчивые к гербицидам (соя, кукуруза, рапс и хлопок) и к насекомым-вредителям.
Приведенные данные свидетельствуют о безусловной востребованности и широком выходе в практику достижений генетической инженерии растений. Тем не менее, ее методы и приемы для широкой общественности до сих пор остаются своего рода «черным ящиком», что в значительной мере и обуславливает настороженность многих в отношении ГМ-продуктов. Такого рода опасения носят эмоциональный, психологический характер, поскольку основаны на отсутствии реальных представлений о существе вопроса. Поэтому остановимся более подробно на основных этапах и методах создания трансгенных растений, сравнивая это направление с традиционными методами селекции.
Фантастическая явь
В чем суть генной инженерии? – В целенаправленной экспериментальной модификации генома организма за счет внесения отдельных новых генов. Сразу же зададим себе вопрос: а чем, собственно, эти методы принципиально отличаются от давно существующих методов селекции, на которых до недавнего времени была основана вся технология получения новых сортов растений?
Первое, что необходимо подчеркнуть: как в том, так и в другом случае, в геном будущего сорта переносятся новые, желаемые гены, существенно различаются лишь способы их «доставки».
Традиционные методы селекции основаны на объединении желаемых генов в геноме гибридного растения, что происходит в результате переопыления растений – «доноров» необходимых для селекционера признаков. Методами же генной инженерии нужные гены изолируют (клонируют) и целенаправленно переносят в клетки организма-реципиента. Таким образом, изменяется лишь «внешняя форма», но не сама суть методов.
 Однако в результатах есть существенное различие: традиционные методы селекции позволяют объединять в геноме гибридов генетическую информацию только близкородственных, скрещивающихся между собой видов. В то время как генно-инженерный подход дает уникальную возможность перестраивать геном растения с использованием наследственной информации из совершенно других систем – вирусов, бактерий, насекомых, животных. Само собой разумеется, что при этом существенно расширяются возможности модификации генома и внутри самого растительного царства, снимаются естественные барьеры между систематически удаленными видами, например, – однодольными и двудольными растениями.
Однако в результатах есть существенное различие: традиционные методы селекции позволяют объединять в геноме гибридов генетическую информацию только близкородственных, скрещивающихся между собой видов. В то время как генно-инженерный подход дает уникальную возможность перестраивать геном растения с использованием наследственной информации из совершенно других систем – вирусов, бактерий, насекомых, животных. Само собой разумеется, что при этом существенно расширяются возможности модификации генома и внутри самого растительного царства, снимаются естественные барьеры между систематически удаленными видами, например, – однодольными и двудольными растениями.
Таким образом, методы генной инженерии являются очень «логичным» дополнением к традиционным селекционно-генетическим методам. Они позволяют до таких размеров раздвинуть границы формообразовательного процесса при создании исходного материала, о каких селекционер раньше не мог и мечтать.
Генная инженерия против «любителя картошки»
В современных технологиях создания трансгенных растений можно выделить несколько основных этапов:
а) клонирование «нужных» генов и создание генетических конструкций, которые могут экспрессироваться (работать) в растительных геномах;
б) перенос созданных генетических конструкций в геном растения;
в) оценка трансгенных растений по стабильности экспрессии перенесенных генов и отбор отдельных растений-трансформантов для дальнейшей селекционной доработки;
г) оценка биобезопасности трансгенов.

Картофель – одна из основных сельскохозяйственных культур в России. Стабильность в снабжении этим питательным и доступным продуктом существенна для продовольственной безопасности страны. Однако урожайность картофеля остается достаточно низкой, а производители сталкиваются с постоянной проблемой защиты его от вредителей и болезней.
Главным незаконным «едоком картофеля» является колорадский жук (Leptinotarsa decemlineata), который уже к 1992 году «завоевал» площадь около 2,5 млн га. Потенциальные потери урожая от жука оцениваются в 4,1 млн тонн на сумму 19,4 млрд рублей. Поскольку более 90% картофеля выращивается в частном секторе (где без соответствующих обработок может погибнуть до 100% урожая), некоторые эксперты оценивают реальные потери в 2–3 млрд долларов ежегодно!
В рамках традиционной селекции не удается получить сорта картофеля, устойчивые к колорадскому жуку. Поэтому существует острая необходимость создания новых сортов методами современной биотехнологии, в частности – генетической инженерии. Новые сорта помогут не только снизить потери урожая, но и уменьшить пестицидную нагрузку на сельхозугодья, что положительно скажется на здоровье населения.
Общепризнанной стратегией создания ГМ-растений, устойчивых к насекомым-вредителям, является использование естественных природных инсектицидов – белков ( -эндотоксинов), гены которых были клонированы из бактерии Bacillus thuringiensis. Такие Bt-защищенные кукуруза, хлопок и картофель были внедрены в сельскохозяйственную практику в США в 1995–1996 гг. Широкомасштабные испытания и длительный опыт использования в сельском хозяйстве разных стран подтвердили безопасность продукции из Bt-культур для человека и окружающей среды.
Эти аргументы и стали предпосылкой для начала и успешной реализации одного из самых крупномасштабных проектов в области биотехнологии сельскохозяйственных растений в Российской -Федерации – создания Bt-защищенного картофеля на основе сортов российской селекции, о котором мы расскажем в одном из будущих номеров журнала.
К настоящему времени уровень развития генно-инженерных методов позволяет клонировать самые разнообразные гены в зависимости от поставленных в конкретном биотехнологическом проекте целей и задач. Рассмотрим отдельные этапы этого процесса на конкретном примере, а именно – на любимой нами картошке, заслуженно считающейся в России «вторым хлебом».
Несмотря на то, что в нашей стране возделывается много высокопродуктивных сортов картофеля, адапти-рованных к широкому спектру природных условий, около трети всего урожая теряется из-за болезней и вредителей. Врагом № 1 заслуженно считается колорадский жук, впервые появившейся на территории России около 50 лет назад. Для борьбы с ним ранее широко применялись химические методы, небезопасные и загрязнявшие окружающую среду. В качестве экологически безопасной альтернативы был разработан целый арсенал биологических методов, один из которых основан на использовании специфического белка, синтезируемого энтомопатогенными бактериями Bacillus thuringiensis.
Данный белок при попадании в кишечник вредителя расщепляется, образуя активизированный токсин, что приводит к гибели насекомого. В ряде стран уже в течение многих лет с помощью различных штаммов B. thuringiensis в промышленных условиях нарабатываются нужные количества инсектицидного белкового препарата. Полученный инсектицид распыляется на листья и проникает в организм «любителя картофеля» вместе с пищей. Нетрудно себе представить, что при распылении препарата он легко попадает также и в окружающую среду, тем более что при таком способе нанесения его невозможно точно дозировать.
Что же предлагает генная инженерия для того, чтобы уберечь картофель от прожорливого насекомого? А предлагает она тот же самый метод защиты с одной лишь разницей – растение само должно накапливать нужный белок в листьях. Достигается это тем, что ген CryA из бактерии B. thuringiensis переносится в ДНК картофеля и становится неотъемлемой частью его генома. Более того, перенесенный ген «заставляют» работать только в определенных частях растения, например, в листьях, а не в клубнях, которые попадают к нам на стол.
Колечки из ДНК
Как же происходит создание генетической конструкции для переноса выделенного гена в наш «модельный» объект – растение картофеля?
 Первый этап – сбор насекомых (колорадских жуков), погибших в естественных условиях от бактериального энтомотоксина. Бактерии с тела жука переносят на специальные чашки Петри и размножают на питательных средах, а выросшие колонии отбирают под микроскопом. Затем из бактерий выделяют ДНК.
Первый этап – сбор насекомых (колорадских жуков), погибших в естественных условиях от бактериального энтомотоксина. Бактерии с тела жука переносят на специальные чашки Петри и размножают на питательных средах, а выросшие колонии отбирают под микроскопом. Затем из бактерий выделяют ДНК.
Известно, что у бактерий гены располагаются не только в хромосомах, как у высших организмов, но и в плазмидах – небольших кольцевых молекулах ДНК. В частности, нужный нам ген CryA локализован именно на одной из таких плазмид. Выделенные плазмиды обрабатываются специальными ферментами, представляющими собой «молекулярные ножницы», разрезающие плазмидную ДНК на отдельные фрагменты.
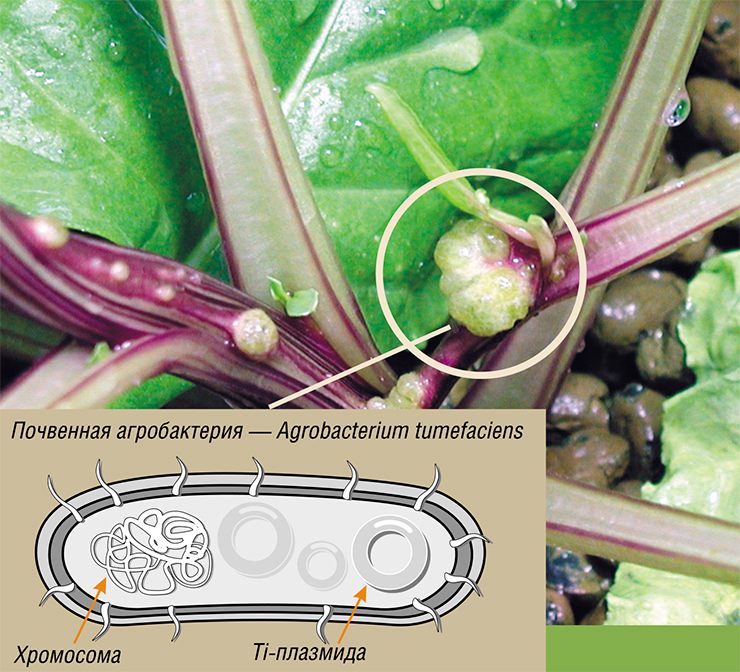
Фрагмент с искомым геном переносится в плазмиду кишечной палочки, которая в данном случае служит «копировальной машиной», так как именно в ней достаточно быстро образуется много копий нужного гена. Затем гены вновь переносятся в плазмиду, но уже другой бактерии – почвенной агробактерии Agrobacterium tumefaciens. И вот о ней стоит поговорить особо.
Агробактерия – «перевозчик» для генов
В настоящее время наиболее распространенным методом переноса чужеродных генов в клетки растений (в особенности представителей класса двудольных) является использование почвенных бактерий рода Agrobacterium, чаще всего – A. tumefaciens, вызывающих у растений болезнь корончатые галлы.
 Корончатые галлы образуются в результате проникновения агробактерий в местах поранения или повреждения поверхности растений грызущими насекомыми. При этом сама почвенная бактерия в растительные клетки не проникает, а «посылает» туда только небольшой фрагмент ДНК, который располагается на плазмиде между двумя сигнальными районами. Эти районы представляют собой повторы из 25 пар нуклеотидов, которые «распознаются» специальными ферментами в тот самый момент, когда почвенная бактерия присоединяется к пораненной растительной клетке. Фермент разрезает нить ДНК между двумя сигнальными районами. Затем к ней присоединяются различные белки, защищающие и переносящие нить ДНК в цитоплазму и далее – в ядро растительной клетки. Фрагмент ДНК бактерии встраивается непосредственно в ДНК растения, и бактериальные гены начинают функционировать наравне с собственными генами растения. В результате метаболизм растительной клетки меняется и в ней начинается синтез веществ, служащих источниками питания для агробактерий.
Корончатые галлы образуются в результате проникновения агробактерий в местах поранения или повреждения поверхности растений грызущими насекомыми. При этом сама почвенная бактерия в растительные клетки не проникает, а «посылает» туда только небольшой фрагмент ДНК, который располагается на плазмиде между двумя сигнальными районами. Эти районы представляют собой повторы из 25 пар нуклеотидов, которые «распознаются» специальными ферментами в тот самый момент, когда почвенная бактерия присоединяется к пораненной растительной клетке. Фермент разрезает нить ДНК между двумя сигнальными районами. Затем к ней присоединяются различные белки, защищающие и переносящие нить ДНК в цитоплазму и далее – в ядро растительной клетки. Фрагмент ДНК бактерии встраивается непосредственно в ДНК растения, и бактериальные гены начинают функционировать наравне с собственными генами растения. В результате метаболизм растительной клетки меняется и в ней начинается синтез веществ, служащих источниками питания для агробактерий.
Фрагмент ДНК плазмиды A. tumefaciens получил специальное название – тДНК (от анг. transfer – «перенос»). тДНК сыграла неоценимую роль в развитии стратегий генно-инженерной модификации растений: взяв за основу эту уникальную природную особенность бактерии, генные инженеры заменяют бактериальные гены на те, которые представляют интерес для исследователя. Тем не менее, эта удобная система для переноса чужеродных генов не является универсальной, поскольку подходит в основном для двудольных растений. Что касается большой группы однодольных, куда относятся и такие важные для сельского хозяйства культуры, как хлебные злаки, то здесь она малоэффективна, поскольку эти растения устойчивы к заражению агробактериями. В этих случаях используются методы прямого переноса генов, одним из которых является доставка фрагментов ДНК на частичках из золота или вольфрама с помощью «генной пушки».
Нелегкая эта работа…
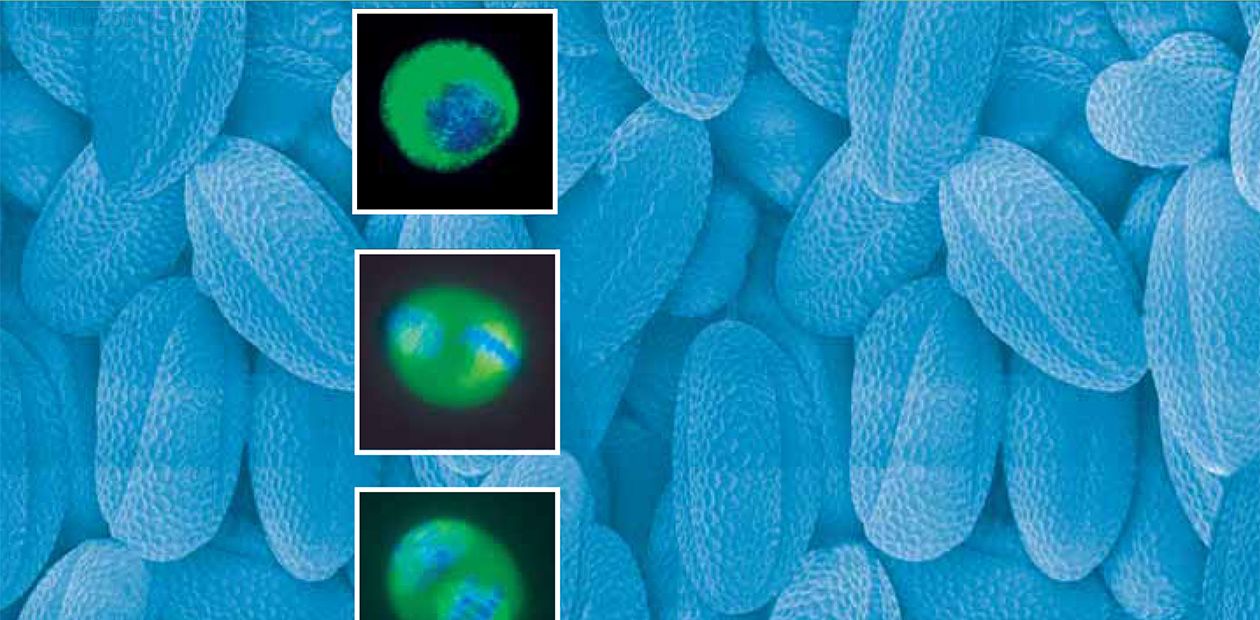
Но вот фрагмент ДНК доставлен в клетку растения и интегрирован в ядерный геном. Клетка получает новый статус – генетически модифицированной. На следующем этапе экспериментатору необходимо отделить трансгенные клетки от нетрансгенных, размножить их и восстановить (регенерировать) из них полноценные растения.
 Для этого вместе с целевыми генами (в нашем «картофельном» примере – геном CryA) одновременно в растения переносят также ген устойчивости к антибиотику, губительному для растительного организма. Присутствие такого гена в растительной клетке дает ей возможность выживать и расти на специальных средах с добавлением антибиотика, а экспериментатору – отобрать трансгенные клетки. Так, например, перенос гена nptII придает растительным клеткам устойчивость к антибиотику канамицину.
Для этого вместе с целевыми генами (в нашем «картофельном» примере – геном CryA) одновременно в растения переносят также ген устойчивости к антибиотику, губительному для растительного организма. Присутствие такого гена в растительной клетке дает ей возможность выживать и расти на специальных средах с добавлением антибиотика, а экспериментатору – отобрать трансгенные клетки. Так, например, перенос гена nptII придает растительным клеткам устойчивость к антибиотику канамицину.
Проведя сортировку клеток в условиях селективной среды и размножив отобранные трансгенные клетки, экспериментатор затем переносит их на среды специального состава с добавлением фитогормонов для восстановления целого растения. В условиях in vitro, т. е. в пробирке, регенерировавшие растения подращивают и переносят в теплицу.
Но работа на этом не заканчивается, а лишь вступает в новую кропотливую фазу. Во-первых, необходимо доказать наличие в геноме данных растений перенесенного фрагмента ДНК с целевым геном. Затем показать, что перенесенные гены не просто «существуют», но и экспрессируются в новом генном окружении. А еще они должны не нарушать работу других генов, т. е. не вызывать мутации, а также сохраняться и передаваться потомкам… В общем, не будем далее останавливаться на деталях генно-инженерной «кухни», чтобы окончательно не утомить читателя.
Россия – трансгенный «оффшор»?
Итак, трансгенные, хорошо «работающие» растения получены. С этого момента и до выхода ГМ-растений в практику начинается большая и трудоемкая работа по санитарно-гигиенической экспертизе: оценивается соответствие химического состава исходных и трансгенных растений; проверяется – не ухудшилась ли биологическая ценность и усвояемость продуктов, приготовленных из генетически модифицированных растений; изучается – не вызывают ли отдельные компоненты аллергических реакций, не являются ли они канцерогенными, токсичными или мутагенными, не окажут ли негативного влияния на репродуктивные функции животных и человека? – В результате трансгенный картофельный клубень может оказаться намного более безопасным для здоровья, нежели картошка с огорода, притулившегося к скоростной магистрали, обильно поливаемая старыми «добрыми» инсектицидами.
Испытания на биобезопасность трансгенных растений включают в себя и оценку возможных путей переноса встроенных трансгенов в другие организмы, в частности – в близкородственные виды путем их естественного переопыления. Кроме того, изучается влияние новых генов на подверженность трансгенных растений болезням и вредителям, а также влияние самих генетически модифицированных растений на почвенную микрофлору и другие составляющие биоценоза.
В странах, где выращивают трансгенные растения, созданы специальные комиссии для их проверки и регистрации. В России регистрацию трансгенных растений координирует Межведомственная комиссия по проблемам генно-инженерной деятельности, созданная Правительством РФ в 1997 году.
Вообще же деятельность в области биотехнологий регулируют более 150 законов, постановлений и нормативных актов. При этом, как уже упоминалось, собственных посевных площадей, занятых ГМ-культурами, в России нет, как практически нет и трансгенных сортов отечественной селекции. И причина этого заключается не в том, что все россияне дружно проголосовали против ГМО, скорее – в отношении нашего государства и общества к генетике, считающейся в развитых странах арьергардом современной науки.