Тритильные радикалы: 111 лет исканий и находок
В наши дни даже люди, весьма далекие от химии, знают, что радикал – это не только бескомпромиссный сторонник глубоких преобразований в обществе, но и химическая частица с высокой реакционной способностью. Термин «свободный радикал» можно очень часто слышать при обсуждении проблем заболеваний и старения и пользы антиоксидантов, поскольку такие активные короткоживущие частицы постоянно генерируются в нашем организме в норме и при патологии. Однако мало кто знает, что за последние несколько десятилетий химикам удалось синтезировать ряд стабильных радикалов с долгим периодом «жизни», которые позволили провести настоящую революцию в инструментальных способах исследования вещества. В частности, «эволюционные потомки» первого тритильного радикала, открытого свыше ста лет назад, сегодня начинают активно использоваться в биомедицинских технологиях
Когда молодой постдокторант М. Гомберг в 1897 г. вернулся в родной Мичиганский университет (Чикаго, США) после стажировки в Германии, он занялся проверкой своих идей в области органической химии, которые появились у него в ходе совместной работы с крупнейшими немецкими химиками того времени.
Гомберг поставил перед собой задачу синтеза неизвестного ранее вещества – гексафенилэтана, симметричного углеводорода, в котором к обоим центральным атомам углерода присоединены по три фенильных группы. Считалось, что цели можно достичь с помощью хорошо известной реакции Вюрца – взаимодействия активного металла с уже полученным к тому времени трифенилметилхлоридом. Однако, к большому удивлению ученого, вместо ожидаемого вещества неизменно получалось нечто иное (впоследствии вещество было идентифицировано как пероксидное соединение – продукт захвата атмосферного кислорода неизвестным участником реакции).
Для обеспечения чистоты эксперимента исследователь полностью устранил «кислородную помеху». Однако опыты, проводимые в инертной атмосфере, принесли новые сюрпризы. Вопреки прогнозу, полученный продукт оказался чрезвычайно реакционноспособным и охотно реагировал с кислородом и галогенами. Так, в реакции с хлором получался исходный трифенилметилхлорид.
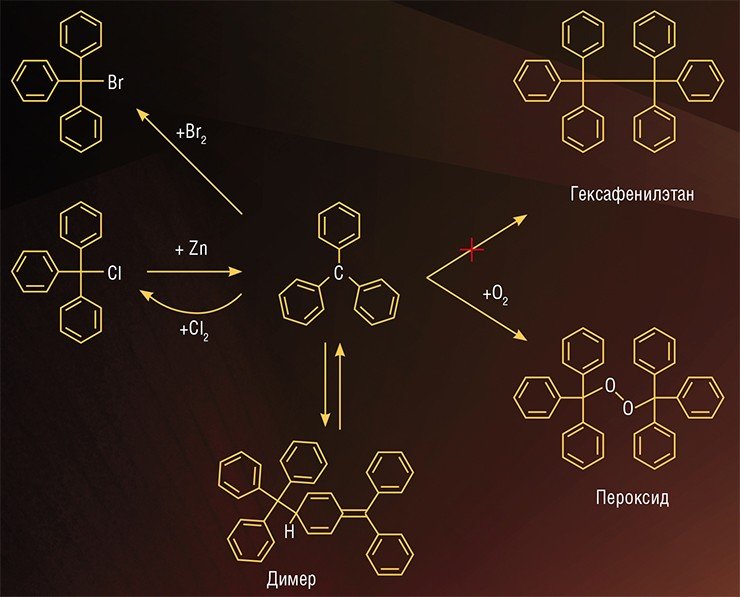
Убедившись в том, что столь странные результаты не являются следствием процедурных ошибок, ученый пришел к парадоксальному выводу: он получил ранее неизвестную форму органического вещества с необычным трехвалентным состоянием углерода. Не «целую» молекулу, а радикал –обломок молекулы с разорванной химической связью и, соответственно, с неспаренным электроном. Это открытие полностью противоречило устоявшимся взглядам на строение органических соединений, согласно которым органический углерод всегда должен быть четырехвалентным, а любые другие формы «не существуют в природе» и поэтому не заслуживают рассмотрения.
Тем не менее Гомберг опубликовал результаты своих исследований в статье (Gomberg, 1900), которая вызвала необычайный интерес и нашла быстрое признание у научного сообщества. Фактически этой работой было заложено новое направление, посвященное химии (и спектроскопии) органических радикалов. Открытый радикал был отнесен к категории тритильных, а автор открытия получил почетный титул «основателя химии органических свободных радикалов».
Казанский приоритет
Дальнейший ход событий показал, что радикалы являются «химической нормой», а отнюдь не редкостью. Они принимают участие в очень многих превращениях, от многотоннажного органического синтеза до метаболитических процессов, лежащих в основе дыхания растений и животных или трансформации лекарственных препаратов внутри организма. Даже молекулярный кислород – вещество, без которого немыслима жизнь, – является радикалом.
Однако увидеть присутствие радикалов совсем непросто. Как правило, свободные радикалы (за рядом исключений, к числу которых относится и кислород) обладают крайне высокой реакционной способностью – и, следовательно, малыми временами жизни. Поэтому традиционные методы химического анализа непригодны для их обнаружения и уж тем более для установления их строения.
Найти свойственный всем свободным радикалам признак помог случай. В июне 1941 г. молодой научный сотрудник Казанского государственного университета Е. К. Завойский в солях некоторых металлов впервые наблюдает явление электронного парамагнитного резонанса (ЭПР). Выяснилось, что все дело в парамагнетизме ионов этих металлов, который обусловлен наличием неспаренных электронов. Если образец поместить в магнитное поле, он обнаруживает способность к резонансному поглощению электромагнитного излучения, что приводит к появлению характерного для него спектра ЭПР.
«Явление электронного парамагнитного резонанса» было внесено в Государственный Реестр научных открытий СССР 12 июля 1944 г. С этой даты и ведется отсчет одного из важнейших событий в физике XX в. – открытие ЭПР как явления и метода спектроскопического анализа. Появление нового метода привело к резкому ускорению научного поиска и способствовало появлению принципиально новых парамагнитных материалов на основе органических радикалов, которым удалось придать необычайно высокую, практически безграничную во времени «живучесть». К их числу в первую очередь нужно отнести стабильные нитроксильные радикалы, традиционно изучаемые в Новосибирском институте органической химии им. Н. Н. Ворожцова СО РАН и являющиеся его своеобразной «визитной карточкой»*.
Просто – о сложном
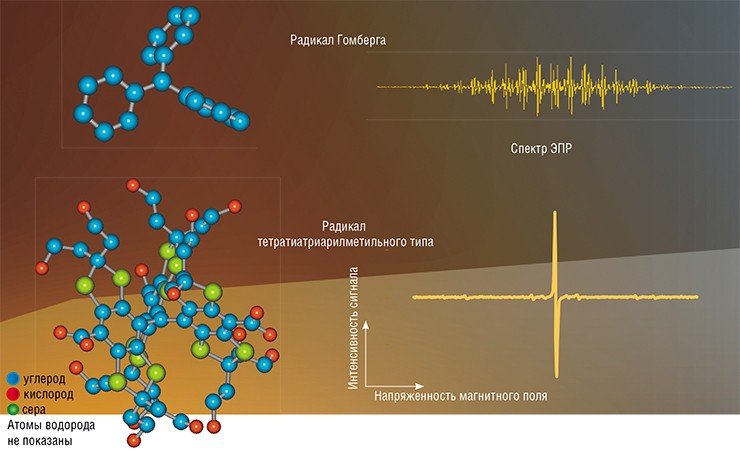
Но какой же оказалась судьба трифенилметила – родоначальника тритильных радикалов? На первый взгляд она весьма завидна, так как на долгое время этот простейший из тритилов стал излюбленным и весьма полезным модельным объектом многочисленных фундаментальных исследований в области спектроскопии и химической физики. Однако до практических приложений долгое время дело не доходило по двум причинам. Радикал этот не очень устойчив: длительность его жизни обычно не превышает секунды. Кроме того, весьма сложная структура его спектра ЭПР препятствует использованию этого радикала в качестве полезного на практике спинового зонда.
Задачу упрощения вида спектра и придания радикалам высокой устойчивости удалось решить химикам норвежской компании Nycomed Imaging, открывшим в конце прошлого века тритилы нового типа, в состав которых входит сера (тетратиатриарилметилы).
 Эти вещества обладают прекрасной растворимостью в воде, устойчивы к действию большинства окислителей и восстановителей, а в спектре ЭПР «демонстрируют» один-единственный, или как принято говорить, синглетный сигнал. Будучи крайне узким и поэтому весьма интенсивным, сигнал от этих радикалов обладает способностью «чувствовать» присутствие других парамагнитных веществ в растворе. Их влияние приводит к уширению линии, что позволяет судить о концентрации примеси. В случае кислорода взаимодействие носит обратимый характер: сигнал сужается при удалении кислорода и вновь расширяется при насыщении раствора кислородом. Сочетание этих качеств имеет особую ценность при использовании тетратиатриарилметильных радикалов в качестве спиновых зондов в биологических и медицинских исследованиях.
Эти вещества обладают прекрасной растворимостью в воде, устойчивы к действию большинства окислителей и восстановителей, а в спектре ЭПР «демонстрируют» один-единственный, или как принято говорить, синглетный сигнал. Будучи крайне узким и поэтому весьма интенсивным, сигнал от этих радикалов обладает способностью «чувствовать» присутствие других парамагнитных веществ в растворе. Их влияние приводит к уширению линии, что позволяет судить о концентрации примеси. В случае кислорода взаимодействие носит обратимый характер: сигнал сужается при удалении кислорода и вновь расширяется при насыщении раствора кислородом. Сочетание этих качеств имеет особую ценность при использовании тетратиатриарилметильных радикалов в качестве спиновых зондов в биологических и медицинских исследованиях.
В списке потенциально возможных приложений особенно выделяются методы регистрации пространственного распределения кислорода в живых организмах и материалах биологического происхождения – трехмерная оксиметрия на основе ЭПР спектроскопии высокого разрешения. Для таких объектов выдвигается дополнительное ограничение: парамагнитные добавки должны быть нетоксичными. Задача эта имеет прямое отношение к диагностике ряда опасных заболеваний, течение которых меняет картину распределения кислорода.
«Трехмерный» кислород
Для реализации этих программ необходимо, чтобы новые парамагнитные материалы были доступны как для фундаментальной науки, так и для прикладных работ. Но это требование не выполнялось, материалы были недоступны. Именно тогда Новосибирский институт органической химии СО РАН приступил к разработке методов синтеза и изучению свойств устойчивых тритильных радикалов разнообразных типов.
Как правило, такой синтез проводится в несколько стадий, каждую из которых можно осуществить разными способами. И за последнее десятилетие новосибирским ученым удалось определить основные пути синтеза радикалов и оптимизировать все стадии химической трансформации. Были разработаны методики, позволяющие получать радикалы в лабораторном масштабе (десятки граммов), которые отличаются простотой проведения и очистки конечных продуктов.
Синтезированные в институте радикалы тетратиатриарилметильного типа демонстрируют высокую устойчивость к большому кругу восстановителей и ферментов. Спектр ЭПР этих радикалов характеризуется синглетным сигналом чрезвычайно малой ширины. Это обстоятельство обеспечивает резкое увеличение чувствительности и разрешения – параметров, играющих ключевую роль в трехмерной оксиметрии биологических объектов.

Будучи полярными и хорошо растворимыми в воде веществами, тритильные радикалы существенно различаются по способности к связыванию с белками и липидами. Так, радикал типа I, впервые синтезированный исследователями Nycomed, обладает сравнительно высокой склонностью к образованию связанных состояний с высокомолекулярными биополимерами и поэтому характеризуется более высокой токсичностью. Это обстоятельство препятствует его широкому применению в экспериментах непосредственно на теплокровных организмах, однако не создает затруднений для исследований в клеточных культурах или применительно к микроорганизмам.
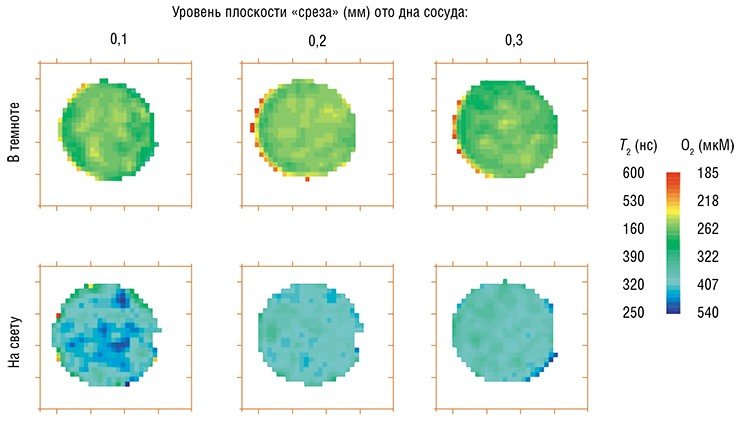
Недавно новосибирские исследователи совместно с биофизиками из института Technion (Хайфа, Израиль) разработали новую методологию построения образа трехмерного распределения кислорода, генерируемого живыми клетками цианобактерий. При этом использовался один из методов импульсной ЭПР-спектроскопии, которым определяется характерное время спин-спиновой релаксации. Такие измерения можно проводить не только для всего образца в целом, но и для любого его участка c высоким пространственным разрешением (не хуже 0,1 мм). Просканировав весь объект, можно получить трехмерную картину распределения в нем растворенного кислорода.
Новый инструментарий, основанный на использовании спектроскопии ЭПР, обладает высокой чувствительностью по отношению к кислороду – порядка 1 мкM. Он является удачным дополнением к ныне существующим методикам, базирующимся на потенциометрических измерениях, эффектах флюоресценции и фосфоресценции.
Тритил для оксиметрии in vivo
В этом месте, замыкая своеобразный круг, наш рассказ возвращается в исходную географическую точку. В стенах Университета Чикаго в рамках многодисциплинарной программы, выполняемой с участием НИОХ СО РАН при поддержке Национального института здоровья США, сегодня проводится блок медико-диагностических исследований при использовании еще одного тритильного радикала – типа II.

В отличие от радикала типа I, этот сильнополярный тритил оказался нетоксичен в опытах с теплокровными животными. Это обстоятельство оказалось очень важным для биомедицинских исследований злокачественных новообразований, характерной чертой которых, как известно, является внутриопухолевая гипоксия (пониженная концентрация кислорода), положительно связанная с ростом опухоли. Поэтому на основе безопасного для живого организма тритила типа II началась разработка инструментального диагностического метода для определения области локализации злокачественных опухолей во время курса лечения средствами химио- и радиотерапии.
В качестве терапевтического средства воздействия на опухоль была выбрана радиационно-индуцируемая генная терапия – новое направление, сочетающее высокую эффективность с направленным воздействием на пораженные участки. Суть этой терапии в том, что генетически модифицированный аденовирусный вектор вызывает в инфицированных клетках экспрессию гена, приводящего к наработке α-фактора некроза раковых тканей. Кроме того, α-фактор обладает ярко выраженным антиваскулярным эффектом, т. е. способностью разрушать кровеносные сосуды, питающие опухоль. А поскольку деятельность вектора «запускается» облучением раковых клеток значительной дозой радиации, эффект радиационной терапии подкрепляется уменьшением кровоснабжения опухолевых участков.
Использование чувствительного к концентрации кислорода тритила II позволяет контролировать ход лечения путем генерации трехмерных образов распределения кислорода и их последующего анализа. Предлагаемая методика может сочетаться с традиционными методами магниторезонансной томографии.
Новый подход был апробирован на лабораторных тимус-эктомированные мышах с раком простаты. Животные были обследованы по «радикальной» методике, после чего половина из них была подвергнута комплексной генно-радиационной терапии. Через три дня были вновь сняты трехмерные картины распределения концентрации кислорода в области простаты у особей из экспериментальной и контрольной групп.
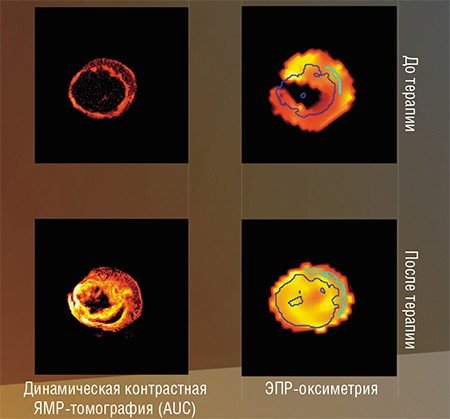 Судя по этим данным, у мышей, подвергавшихся терапевтической процедуре, произошло видимое сокращение размеров опухоли. С помощью ЭПР-контроля удалось заметить и то обстоятельство, что антиваскулярный эффект, первоначально вызываемый действием аденовирусного вектора, по мере уменьшения опухоли исчезает, и кровоснабжение анализируемого участка в конечном итоге заметно усиливается.
Судя по этим данным, у мышей, подвергавшихся терапевтической процедуре, произошло видимое сокращение размеров опухоли. С помощью ЭПР-контроля удалось заметить и то обстоятельство, что антиваскулярный эффект, первоначально вызываемый действием аденовирусного вектора, по мере уменьшения опухоли исчезает, и кровоснабжение анализируемого участка в конечном итоге заметно усиливается.
Тритильные радикалы прошли долгий путь от открытия до применения в качестве кислород-чувствительного зонда в биомедицинской диагностике. И разумеется, круг возможных применений этих уникальных соединений далеко не исчерпывается исследованиями в области 3D-оксиметрии высокого разрешения. Например, они оказались весьма полезными в исследованиях особенностей диффузии в микрогетерогенных системах, определении пространственной структуры биополимеров, выявлении факторов и глубины стресса у культурных и дикорастущих растений.
В программе исследований НИОХ СО РАН особое место занимают радикалы, характеризующиеся отчетливо детектируемым откликом спектра ЭПР на изменение кислотности среды – это так называемые pH-чувствительные спиновые зонды **. В последние годы сотрудниками института разработаны подходы к синтезу радикалов нитроксильного ряда, способных обеспечить надежное и высокочувствительное зондирование кислотности среды в широком диапазоне. Накопленный в институте опыт по дизайну нитроксильных pH-зондов разумно перенести на тритилы.
Важность этих работ в том, что с помощью подобных соединений можно будет регистрировать очень малые изменения кислотности среды в значимом для медицины и биологии диапазоне (pH 6,5—7,5). Возможность локализации в живом организме участков с аномальными параметрами кислотности даст основу для надежного выявления разнообразных патологий.
Литература
Григорьев И. А., Полиенко Ю. Ф., Войнов М. А. рН-чувствительные нитроксильные радикалы: структурные требования, проблемы молекулярного дизайна и синтетические подходы // Химия ароматических, гетероциклических и природных соединений (НИОХ СО РАН 1958—2008 гг.). Новосибирск, 2009. С. 501—535.
Gomberg M. An instance of trivalent carbon: triphenylmethyl // J. Am. Chem. Soc. 1900. V. 22. № 11. P. 757—771.
Halevy R., Tormyshev V., Blank A. Microimaging of Oxygen Concentration near Live Photosynthetic Cells by Electron Spin Resonance // Biophysical Journal. 2010. V. 99. P. 971—978.
* Подробнее о нитроксильных радикалах – в статье В. А. Резникова
** Подробнее – в статье В. А. Резникова