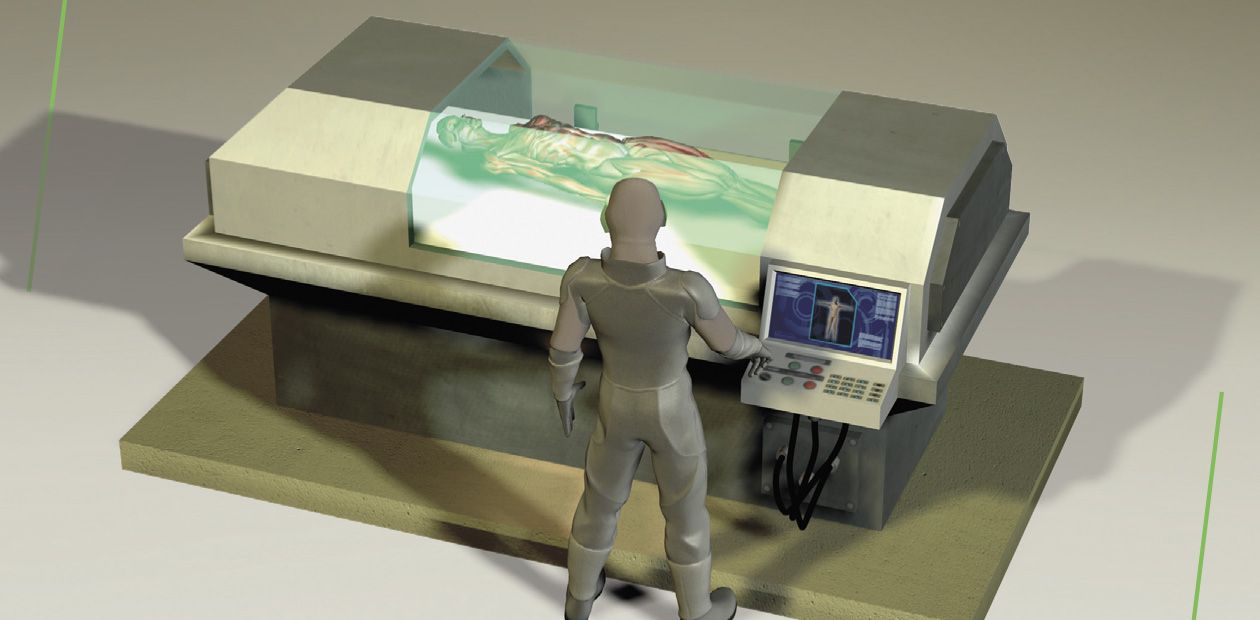
Вслед за Создателем. Технологии биопринтинга
Давняя мечта человечества о возможности замены больных или утраченных частей тела на новые воплотилась в реальность только в середине прошлого века. Но хотя к настоящему времени техническая сторона пересадки органов освоена достаточно хорошо, серьезнейшей и до сих пор нерешенной проблемой остается нехватка органов для трансплантации. Радикально решить эту проблему позволит применение «биопринтинга» – трехмерной пeчaти человеческих органов. Биопечать аналогична известной технологии послойного формирования объектов из металла или полимеров на основе компьютерной модели, только в качестве строительных блоков здесь используются живые клетки самого пациента, выращенные в биореакторе.
Уже сегодня вполне реально «печатать» хрящи и кожу, однако клиническое применение этих технологий пока в мире официально не разрешено. Но при достаточном финансировании исследований уже через 10—15 лет станет возможным производить уже цельные органы со встроенной сосудистой сетью, например, печень и почку. Над этой проблемой сейчас работает и российская компания «3D Bioprinting Solutions», созданная в 2013 г. под научным руководством биопринтинга, профессора В.А. Миронова
Каждый день почти два десятка человек умирает из-за нехватки донорских органов; каждые десять минут в лист ожидания на трансплантацию добавляется новое имя. Только в США более 114 тыс. человек ожидают донорские органы для пересадки, и большая часть из них – пациенты с почечной недостаточностью, которым требуется новая почка. К этому можно добавить, что период ожидания такой операции может достигать 10—15 лет, поэтому неудивительно, что почти четверть ожидающих очереди на трансплантацию умирают, ее не дождавшись.
Ежегодно в мире осуществляется в общей совокупности около 100 тыс. трансплантаций органов. Один только «рынок почки» оценивается специалистами в 25 млрд долларов США.В России сегодня более 20 тыс. человек страдают почечной недостаточностью и буквально прикованы к аппарату искусственной почки, при этом ежегодные затраты на одного пациента, нуждающегося в процедуре гемодиализа, составляют свыше 2 млн руб.
Число пациентов с потребностью в гемодиализе в России ежегодно увеличивается примерно на 6 тыс.человек, тогда как в 2009 г. было осуществлено только 820 трансплантаций донорской почки
Нехватка доноров – серьезнейшая медицинская проблема, причем тенденция такова, что доноров становится все меньше, а пациентов, которым требуются донорские органы, – все больше. Кроме того, пересадка той же почки означает для реципиента пожизненный прием лекарств, подавляющих иммунитет, а это делает людей более восприимчивыми к болезням и может приводить к онкологическим заболеваниям. Существующая альтернатива трансплантации почки – регулярный гемодиализ, очистка крови с помощью искусственных фильтров, процедура неприятная и дорогостоящая.
На сегодня существует несколько путей выхода из этой ситуации, однако практически все они имеют ряд серьезных недостатков.
Инжиниринг органов
Среди технологий создания донорских органов есть технически осуществимые, но откровенно неэтичные и потому неприемлемые. Например, выращивание «на органы» анацефальных (не имеющих мозга) эмбрионов в матке суррогатной матери из стволовых клеток пациента.
 При классических технологиях «инжиниринга органов» сначала изготавливается каркас – основа будущего органа. Это может быть имплантат из искусственных материалов, стойких или разлагающихся со временем, в который врастают клетки и сосуды пациента, образуя с ним единое целое. Однако к таким материалам предъявляются, и небезосновательно, серьезные требования, удовлетворить которым непросто.
При классических технологиях «инжиниринга органов» сначала изготавливается каркас – основа будущего органа. Это может быть имплантат из искусственных материалов, стойких или разлагающихся со временем, в который врастают клетки и сосуды пациента, образуя с ним единое целое. Однако к таким материалам предъявляются, и небезосновательно, серьезные требования, удовлетворить которым непросто.
В качестве основы имплантата можно использовать и «натуральный» соединительнотканный каркас органа человека или животного (например, свиньи). При этом соответствующий орган децеллюляризируют, т. е. убирают все клеточные элементы, чтобы снизить риск отторжения, и только потом на этот каркас наращивают собственные клетки пациента. Принципиальная возможность такого подхода была продемонстрирована на примере сердца (Ott et al., 2010), легкого (Petersen et al., 2010), печени (Uygun et al., 2013). В апреле 2013 г. ученые из Гарвардского университета продемонстрировали успешно работающую почку крысы, которая была выращена в биореакторе и затем пересажена животному (Song et al., 2013).
Но и при такой технологии остается риск иммунного отторжения; кроме того, при использовании органов животных всегда существует опасность передать человеку вирусы этих организмов.
От подобных недостатков избавлен альтернативный подход – так называемый биопринтинг или биопечать (трехмерная пeчaть человеческих органов). Биопринтинг тоже принадлежит к группе технологий «инжиниринга органов», но основывается он на так называемом восходящем модульном бескаркасном подходе, когда нужный орган конструируется из клеток самого пациента, что гарантирует отсутствие реакции отторжения.
Идее самосборки – сто лет
Технология биопринтинга базируется на известном явлении самосборки (направленной самоорганизации) клеточных структур. Этот процесс, управляемый силами поверхностного натяжения и межбелковыми взаимодействиями, повсеместно встречается в живом мире, начиная от формирования клеточных мембран и заканчивая образованием органов у эмбриона.
Технология книгопечатания в современном ее понимании была разработана в середине XV в. немецким ювелиром и гравером Иоганном цум Гутенбергом, прирожденным предпринимателем и изобретателем. Пять наиболее важных элементов технологии книгопечатания Гутенберга включают в себя текст, бумагу, чернила, съемные металлические литеры и печатный пресс. По аналогии с книгопечатанием технология биопечати включает в себя: виртуальную модель органа (аналог текста), тканевые сфероиды (аналог чернил), гидрогель (аналог бумаги), картридж, заправленный тканевыми сфероидами (аналог литер) и, наконец, аналог печатного пресса – биопринтер.Существует два типа биопечати: аналоговая и цифровая. Аналоговая биопечать – это непрерывное распыление биобумаги (гидрогеля) с тканевыми сфероидами. При цифровой печати происходит дискретное или каплеобразное распыление
Идея биопринтига родилась из предположения, что такие процессы самосборки тканей можно воспроизводить in vitro, т. е. вне живого организма. Первооткрывателем этого феномена в конце XIX в. стал немецкий профессор анатомии Г. Борн. Однажды вечером Борн препарировал головастика, но ему пришлось прервать работу из-за ужина, чем профессор был немало раздосадован. Борн вернулся к работе только на следующий день и был очень удивлен, обнаружив, что рассеченные фрагменты головастика срослись. А в 1907 г. американский морской биолог Г. В. Вильсон обнаружил спонтанное сращивание тканей морских губок.
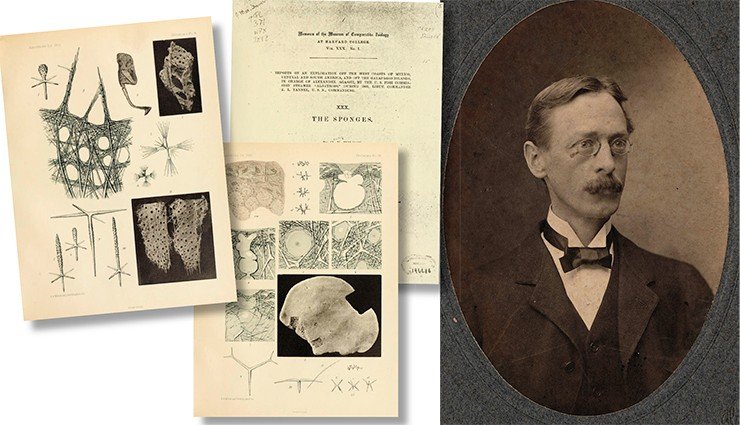
Таким образом, идейная основа биопринтинга была заложена уже более ста лет назад, и в этом смысле эта технология является не гениальным изобретением, а, скорее, практическим результатом многолетних интенсивных исследований в ряде научных областей: биологии моря, эволюционной биологии, молекулярной биологии и биологии стволовых клеток. Здесь как нельзя более уместно привести известное выражение И. Ньютона: «Если я и видел дальше, то лишь потому, что стоял на плечах гигантов».
Базовая методика биопринтинга аналогична уже хорошо отработанной технологии послойного формирования различных трехмерных объектов из металла, керамики или полимеров на основе виртуальной трехмерной компьютерной модели, только в качестве строительных блоков при этом используются живые объекты.
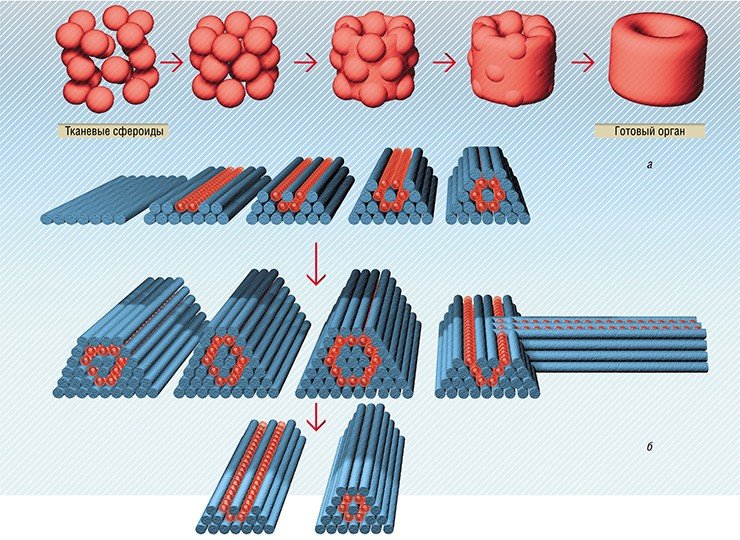
Элементарный живой «кирпичик» создаваемого таким образом тканевого «здания» называют тканевым сфероидом. Это крошечный (200–300 мкм диаметром) шарообразный сгусток из живых клеток. Структура его, скорее, жидкая, чем твердая, недаром ее называют также сложной или мультикомпонентной жидкостью. Это очень важно, потому что более плотные тканевые сфероиды медленнее сращиваются. При сращивании происходит существенное сокращение объема трансплантируемой ткани, что необходимо учитывать при «проектировании» органа.
От клетки – к органу
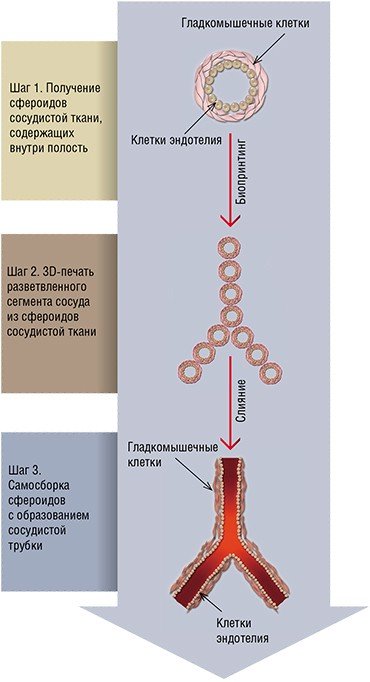
Экспериментальное развитие печати органов началось около десяти лет тому назад. На первом этапе это больше всего походило на создание деталей для конструктора «Лего», когда исследователи могли получать лишь отдельные фрагменты той или иной ткани. Затем появилась возможность создавать сегменты внутреннего органа, уже снабженные сосудистой сетью, что стало определяющим этапом развития новой технологии.
При производстве сфероидов сосудистой ткани используют фактор роста эндотелия сосудов, в результате чего можно получать сосудистые трубки разного диаметра. Так, группе исследователей из Цюрихского центра регенеративной медицины удалось создать сосудистую трубку из тканевых сфероидов с использованием специальной формовки, которую инкубировали в перфузионном биореакторе. По сообщению доктора Дж. М. Келмы, свойства трубчатой конструкции, выращенной из таких сфероидов, вполне сравнимы с природными кровеносными сосудами. А американские исследователи Дж. Дэвис и Б. Вайнштейн (Nature, 2006) доказали, что помещенные в гидрогель клетки эндотелия, сращиваясь и формируя вакуоли (полости), способны формировать сеть капилляров.
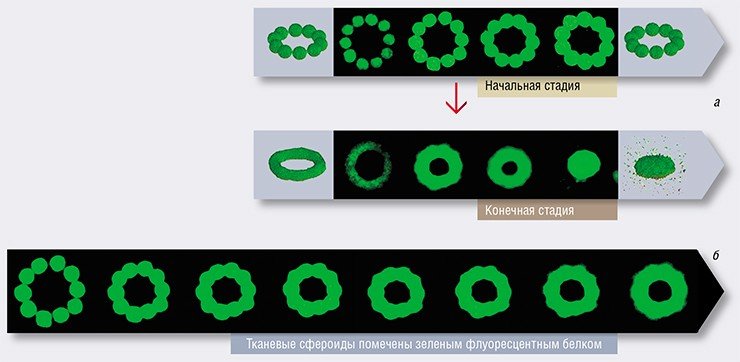
Таким образом, стало технологически возможным производить цельный внутренний орган, снабженный сосудистой сетью. Но для создания полноценного органа, пригодного для трансплантации, требуется усовершенствовать так называемую пост обработку ткани или органа.
В частности, над этой проблемой работает группа В. А. Миронова из российской компании «3D Bioprinting Solutions», которая занимается разработкой технологий биопечати. Исследователи стараются добиться ускоренного развития тканей, используя так называемый «волшебный коктейль», состоящий из определенной комбинации специфических биомолекул – факторов роста и развития.
Клеточные «инкубаторы»
Из чего же состоит «производственная цепочка» биопринтинга?
Как упоминалось выше, основой технологии являются тканевые сфероиды. Простой вариант такой структуры можно получить путем инкубации суспензий различных клеток пациента в небольшом объеме культуральной среды, например, в формах в виде мелких пчелиных сот. Удобным «сырьем» для биопечати являются стволовые клетки жировой ткани пациента, которые можно получить сразу в большом количестве с помощью вакуумной липосакции – малоинвазивной хирургической процедуры. Такие стволовые клетки могут легко дифференцироваться в гладкомышечные клетки, а тканевые сфероиды, произведенные из них, могут сращиваться в кольцо или торус и сокращаться под действием специфических стимулов.

Полученные таким образом клетки выращивают в биореакторах – устройствах, в которых биологические и биохимические процессы развиваются в жестко контролируемых искусственных условиях. Биореактор является своего рода «инкубатором», обеспечивая культуре клеток необходимое ей окружение, питание и кислород и отводя продукты жизнедеятельности. Подобные приборы давно используются для получения антител, вакцин, антибиотиков и ряда пищевых добавок.
Биореакторы для тканевой инженерии устроены гораздо сложнее, ведь клетки в них должны не только расти и нарабатывать какое-то целевое вещество: такие устройства предназначены для формирования полноценной ткани или даже целого органа. Для этого в питательную среду в строго определенном соотношении добавляют вещества, которые стимулируют размножение, дифференцировку и созревание тканей или тканево-инженерных конструкций.
Судя по последним данным, для этого требуется не только конкретное химическое окружение, но и определенное механическое воздействие (вибрации, растяжения и т. п.). По сути, нужно как можно точнее воспроизвести естественные условия, в которых происходят процессы формирования каждой ткани, лишь тогда в биореакторе удастся воспроизвести полноценный орган.
От сортировщика до биореактора
 Полная производственная линия биофабрикации (искусственного производства живых органов) должна включать в себя несколько автоматических установок: cортировщик клеток пациента, биофабрикатор тканевых сфероидов, биопринтер и, наконец, вышеупомянутый биореактор. Все эти установки представляют собой сложные приборы, разработка и совершенствование которых в мире идет полным ходом.
Полная производственная линия биофабрикации (искусственного производства живых органов) должна включать в себя несколько автоматических установок: cортировщик клеток пациента, биофабрикатор тканевых сфероидов, биопринтер и, наконец, вышеупомянутый биореактор. Все эти установки представляют собой сложные приборы, разработка и совершенствование которых в мире идет полным ходом.
Так, современный сортировщик клеток, разработанный компанией «Cytori Therapeutics» (США) в партнерстве с известной компанией «Olympus» (Япония), способен всего за 1—2 часа выделить нужную популяцию стволовых клеток из жировой ткани.
Технологии печатания органов сегодня разработаны, но будут ли они рентабельны? Сколько будет стоить искусственный орган, например, та же почка, произведенная по технологии биопринтинга?Для сравнения: цена искусственного механического сердца в США сегодня составляет около 250 тыс. долларов. Затраты на пациента с почечной недостаточностью, которому требуется процедура гемодиализа, за двенадцать лет составляют 1 млн долларов. Если цена «напечатанной» почки будет также, по ориентировочным оценкам, составлять 250 тыс. долларов плюс дополнительные затраты в 250 тыс. долларов на саму операцию трансплантации, то и в этом случае получается значительная экономия.
К этому стоит добавить, что только в США в очереди на пересадку донорской почки стоит свыше 60 тыс. человек
Сейчас в мире существует, по меньшей мере, шесть коммерческих компаний, занимающихся производством тканевых сфероидов. Так, компания «3D Biomatrix» (США) и «InSphero» (Швейцария) создали автоматическую технологию биофабрикации тканевых сфероидов, основанную на модификации старого микробиологического метода висячей капли, разработанного Р. Кохом еще в конце XIX в. для культивирования бактерий в стерильных условиях.
 Еще одна элегантная технология биофабрикации была создана компанией «Microtissues, Inc.» (США): в качестве среды для формирования сфероидов в ней используется неадгезивный гидрогель, благодаря чему клетки прилипают не к поверхности культуральной посуды, а друг к другу, образуя шарообразную структуру. Автоматизированный вариант этой технологии, разработанный в Медицинском университете Южной Каролины (США) группой В. А. Миронова, позволяет производить до 6 тыс. тканевых сфероидов в стандартных 96-луночных планшетах (Mehesz et al., 2011).
Еще одна элегантная технология биофабрикации была создана компанией «Microtissues, Inc.» (США): в качестве среды для формирования сфероидов в ней используется неадгезивный гидрогель, благодаря чему клетки прилипают не к поверхности культуральной посуды, а друг к другу, образуя шарообразную структуру. Автоматизированный вариант этой технологии, разработанный в Медицинском университете Южной Каролины (США) группой В. А. Миронова, позволяет производить до 6 тыс. тканевых сфероидов в стандартных 96-луночных планшетах (Mehesz et al., 2011).
Однако реальный прорыв в развитии биофабрикации тканевых сфероидов, очевидно, будет связан с применением так называемой цифровой микрофлюидики – совокупности технологий, основанных на микроманипулировании изолированными каплями (так работает, к примеру, обычный струйный принтер). Эта технология позволит генерировать до 10 тыс. тканевых сфероидов в секунду, что даст возможность создавать сложные составные сфероиды. Работы над созданием такого генератора тканевых сфероидов активно ведутся.
Уже разработаны и несколько поколений биопринтеров. К настоящему времени имеется несколько компаний, среди которых «EnvisionTEC» (Германия); «Sciperio-nScript» и «Organovo» (США), «regenHU Ltd» (Швейцария), которые производят коммерческие биопринтеры.
Итак, технология искусственного производства живых органов на сегодня принципиально разработана, создано и выпускается необходимое оборудование. Однако биопринтинг органов до сих пор остается уделом исследователей: применение этих технологий в клинике нигде в мире пока официально не разрешено.
Тем не менее уже сегодня вполне реально «печатать» для медицинских целей такие относительно простые органы, как хрящи и кожу, которым не требуется «встроенных» кровеносных сосудов. Однако, несмотря на все достигнутые успехи, биопечать человеческих почек и печени – самых востребованных и сложно¬организованных внутренних органов, пока недостижима. При достаточном финансировании научно-прикладных исследований это станет возможным через 10—15 лет.
В 2013 г. в Москве была открыта Лаборатория биотехнологических исследований «3D Bioprinting Solutions». Ее научный руководитель – профессор В. А. Миронов, пионер в области технологии печати органов и биофабрикации; заведующий – С.В. Новоселов, эксперт в области молекулярной и клеточной биологии и биомедицины; генеральный директор и председатель Совета директоров группы компаний «ИНВИТРО», ключевого инвестора Лаборатории – А. Ю. Островский. Долгосрочная цель проекта – создание технологии биопринтинга и производства почки, одного из самых востребованных донорских органов человекаНо прежде чем перейти к биопечати больших трехмерных тканевых моделей, необходимо будет решить ряд так называемых «производственных» проблем. Ведь для биопечати только одной человеческой почки требуются миллионы тканевых сфероидов, т. е. речь идет о настоящих промышленных масштабах!
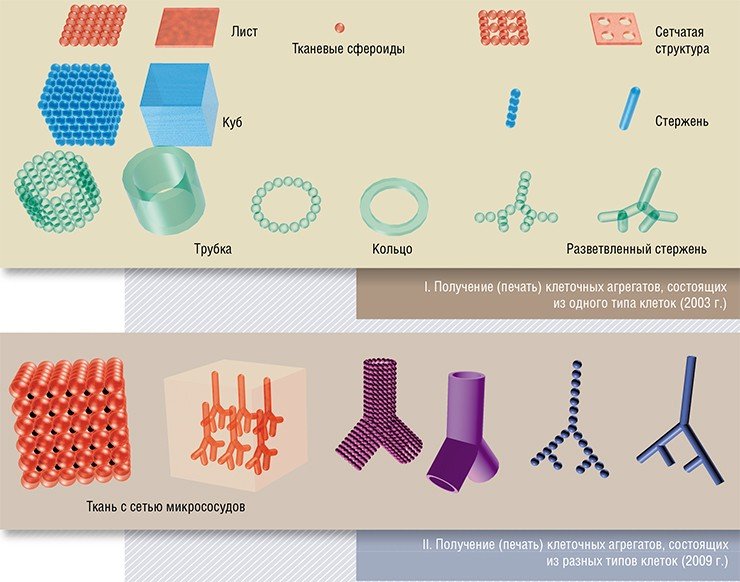
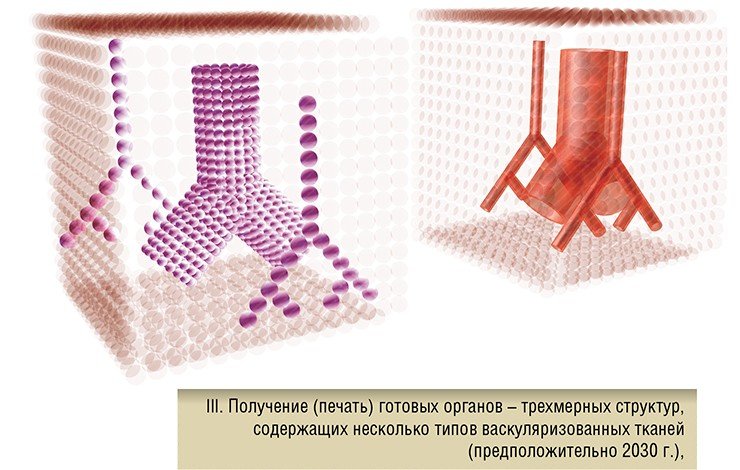
Биопринтинг имеет много схожих характеристик с микропроцессорной и электронной индустрией, которые начали интенсивно развиваться лишь в результате систематического внедрения автоматизации и роботизации в производственные линии. И в этом смысле речь идет о создании не только роботизированного биопринтера, но и целой технологической линии самосборки тканей и органов, чтобы сделать «производство органов» рентабельным и прибыльным.
Для этого сегодня имеются все необходимые предпосылки, и нет сомнений, что именно трехмерной печати органов предстоит в недалеком будущем сделать решающий, революционный прорыв в регенеративной медицине.
Ежегодно в мире осуществляется в общей совокупности около 100 тыс. трансплантаций органов. Один только «рынок почки» оценивается специалистами в 25 млрд долларов США.
В России сегодня более 20 тыс. человек страдают почечной недостаточностью и буквально прикованы к аппарату искусственной почки, при этом ежегодные затраты на одного пациента, нуждающегося в процедуре гемодиализа, составляют свыше 2 млн руб.
Число пациентов с потребностью в гемодиализе в России ежегодно увеличивается примерно на 6 тыс.человек, тогда как в 2009 г. было осуществлено только 820 трансплантаций донорской почки
Литература
Martin I., Wendt D., Heberer M. The role of bioreactors in tissue engineering. Trends Biotechnol. 2004 Feb; 22(2):80–6.
Mehesz, Brown J., Hajdu Z. et al. Scalable robotic biofabrication of tissue spheroids // Biofabrication. 2011 Jun; 3(2):025002. doi: 10.1088/1758–5082/3/2/025002. Epub 2011 May 12.
Song J. J, Guyette J. P., Gilpin S. E et al. Regeneration and experimental orthotopic transplantation of a bioengineered kidney // Nat Med. 2013 May; 19(5):646–51. doi: 10.1038/nm.3154. Epub 2013 Apr 14.