Меж алмазных наковален
Вторая половина 40-х гг. прошлого века была ознаменована появлением принципиально новых устройств для создания высоких давлений в лабораторных условиях — ячеек с алмазными наковальнями. Они произвели настоящую революцию в экспериментальной технике. Такие устройства весом всего 10—30 г позволяют создавать давления до миллиона атмосфер, причем работа с ними не требует приложения особых физических усилий...
Область высоких давлений изначально была епархией физиков и геологов. Физиков привлекала возможность «испытать вещества» в экстремальных условиях, в которых у них могут появиться необычные свойства. Например, при высоком давлении неметаллы превращаются в металлы, кардинально меняются электрические, магнитные и оптические свойства вещества.
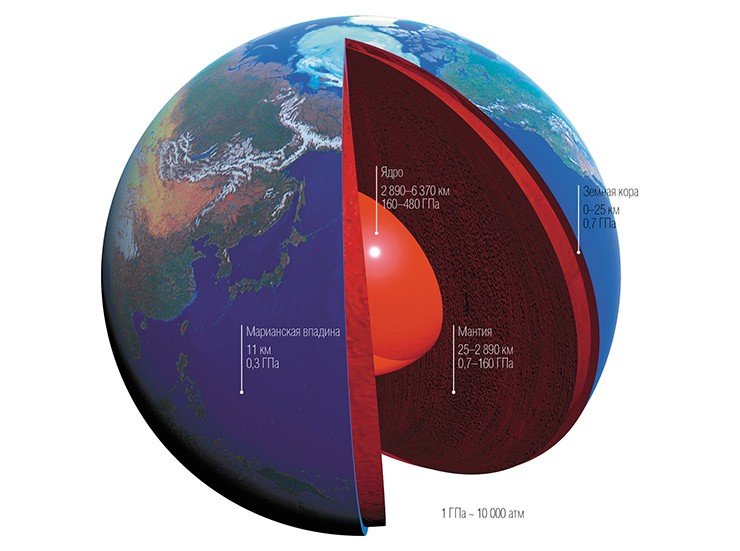
Геологов интересовали процессы, протекающие в веществе в условиях, приближенных к тем, что реально происходят в недрах Земли и других планет; геохимические реакции, приводящие к глобальным геологическим явлениям, а также процессы образования минералов. Одной из частных, но очень заманчивых задач стал синтез алмазов в условиях высоких давлений.
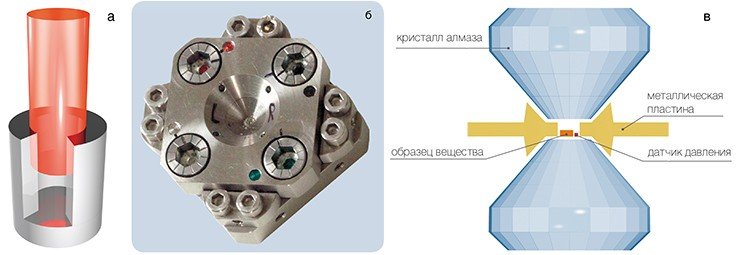
Вторая половина 40-х гг. прошлого века была ознаменована появлением принципиально новых устройств для создания высоких давлений в лабораторных условиях — ячеек с алмазными наковальнями. Они произвели настоящую революцию в экспериментальной технике. Такие устройства весом всего 10—30 г позволяют создавать давления до миллиона атмосфер, причем работа с ними не требует приложения особых физических усилий. Основной принцип работы таких ячеек прост: высокие давления достигаются за счет того, что площадь приложения силы очень маленькая.
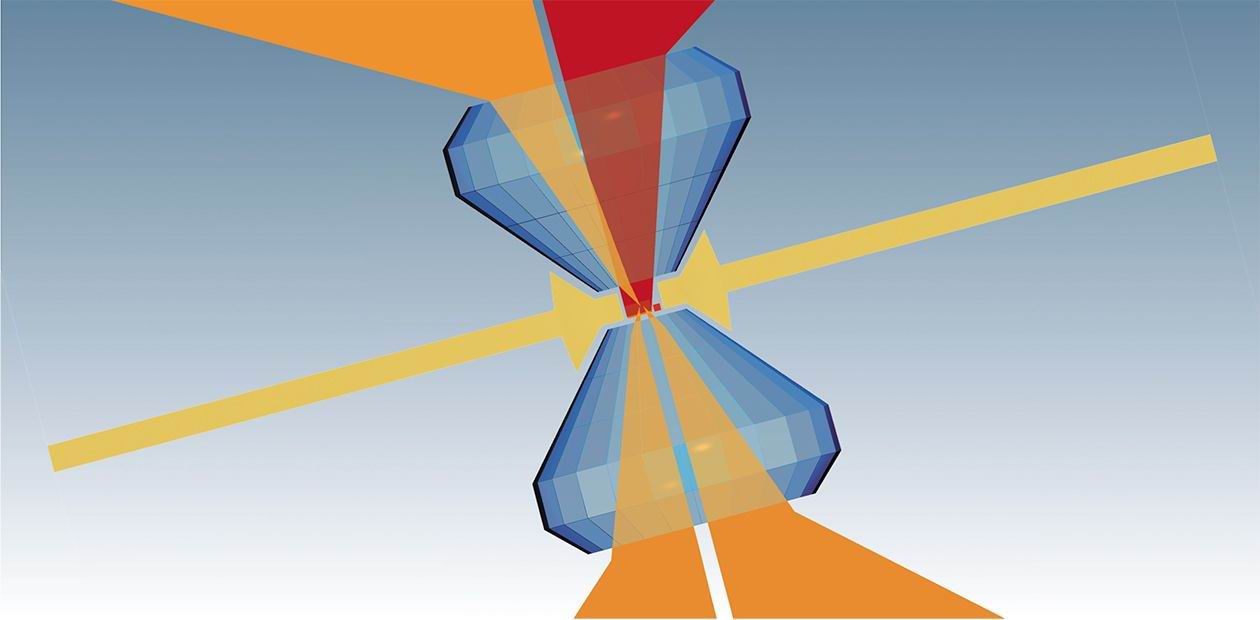
Конкретных реализаций этого принципа множество, но все их можно условно разделить на две группы: ячейки типа «поршень-цилиндр» и типа «наковальня». Благодаря тому что алмаз прозрачен для инфракрасного излучения, видимого и ультрафиолетового света, рентгеновских лучей и нейтронов, появилась возможность изучать колебательные спектры и кристаллические структуры различных веществ, а также наблюдать за их превращениями непосредственно в условиях высоких давлений. При этом исследуемый образец можно одновременно либо нагревать до 700 °С, либо охлаждать вплоть до температуры жидкого гелия.
Неудивительно, что появление столь широких возможностей резко повысило интерес к исследованиям веществ в этих необычных условиях, которые от эксперимента к эксперименту становились все более экстремальными.
Взяли на вооружение
Первые эксперименты по влиянию давления на химические и биологические объекты были проведены еще в начале прошлого века, тогда же, когда стартовали исследования минералов. Например, около века тому назад была обнаружена денатурация куриного белка при повышении давления.
Первые достижения химиков и биологов на фоне захватывающих дух успехов физиков и геологов выглядели достаточно скромно, но это была лишь «проба сил». Химия и биология высоких давлений по-настоящему бурно начали развиваться сравнительно недавно.
Как многочисленных тонких нитей, опутавших Гулливера, хватило лилипутам, чтобы лишить великана подвижности, так и слабых, но многочисленных межмолекулярных взаимодействий в кристаллах достаточно, чтобы повлиять на их строение и функцииДля химиков высокие давления сделались инструментом, используемым для синтеза новых соединений, а также кристаллизации уже известных соединений в виде новых полиморфных модификаций — новых кристаллических структур. Кроме того, с помощью высоких давлений ученые изучают природу химических связей и межмолекулярных взаимодействий, «гибкость» молекул, механизмы химических реакций, в том числе и тех, которые вызываются не увеличением давления, а изменением температуры или облучением светом.
Биологи применяют высокие давления для исследования динамики природных биополимеров — высокомолекулярных соединений, являющихся основой всех живых организмов. Они изучают факторы, отвечающие за вторичную и третичную структуру этих молекул, а также то, как она меняется в ходе биохимических процессов, при генетических заболеваниях и внешних воздействиях.
Эксперименты, проводимые при высоких давлениях, помогают разрешить много проблем. Например, каким образом целому ряду организмов (так называемым пьезофилам) удается выжить в глубинах Мирового океана; какие процессы происходят в живой клетке при взаимодействии «рецептор-субстрат»; как работают мышцы и передаются нервные импульсы; за счет чего так прочны природные волокна — нить паутины и шелковая нить — и как создать искусственные волокна, по прочности не уступающие природным. Сегодня высокие давления все шире используются и в пищевой промышленности для дезактивации патогенных микроорганизмов в качестве альтернативы термической обработке продуктов.
И наконец, проблема устойчивости органических соединений к действию высоких давлений напрямую связана с одним из фундаментальных вопросов естествознания: проблемой происхождения жизни на Земле, в том числе с возможностью ее «импорта» извне.
Что такое молекулярные кристаллы?
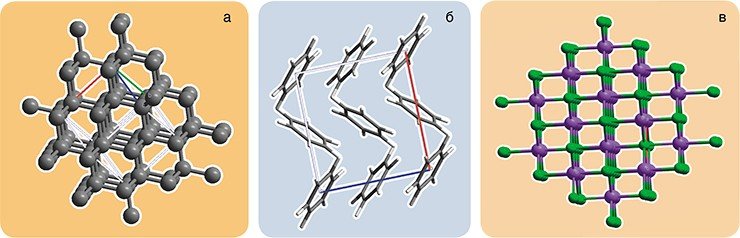
Кристалл — это «ансамбль» атомов, которому присуща так называемая трансляционная симметрия, другими словами — это совокупность атомов, которые, периодически повторяясь в пространстве, образуют трехмерную регулярную структуру. В кристаллах поваренной соли (NaCl) или алмаза (С) все химические связи равноценны: нельзя выделить фрагменты, внутри которых атомы связаны друг с другом сильнее, чем с окружением. В целом подобный кристалл представляет собой, по сути, одну большую «молекулу».
Но гораздо чаще встречаются кристаллы, в которых сосуществуют разные типы связей. К их числу относятся и так называемые молекулярные кристаллы, в которых связи между отдельными молекулами слабее, чем внутри молекул. В подобных кристаллах молекулы не утрачивают своей «индивидуальности», хотя строение и поведение некоторых из них могут видоизменяться в зависимости от состава молекулярного «коллектива». Несмотря на относительную слабость межмолекулярных взаимодействий, именно они определяют разнообразие как трехмерных структур, которые можно «построить» из одних и тех же «кирпичиков»-молекул, так и физико-химических свойств получившихся молекулярных кристаллов.
Молекулярные кристаллы применяются в электронике, фармации, а также используются в качестве модельных объектов, которые имитируют строение и функции отдельных фрагментов биополимеров и биохимических систем.
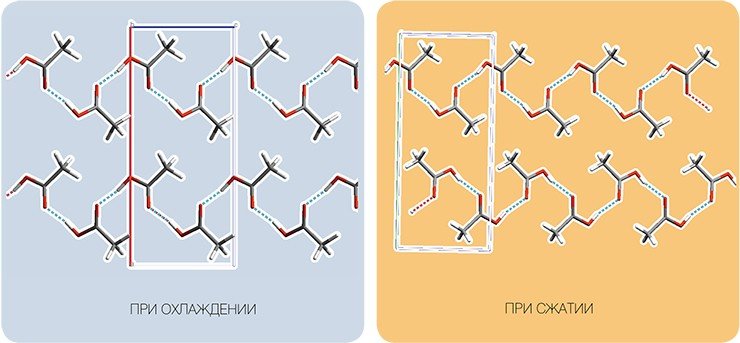
Вещества, которые в нормальных условиях являются жидкостями или газами, способны кристаллизоваться, если взаимодействия между молекулами усилятся. Достичь этого можно, либо понизив температуру (кристаллизация при замораживании), либо повысив давление (кристаллизация при сжатии).
Интересно, что кристаллические структуры, возникающие при замораживании и сжатии одного и того же вещества, часто бывают различны. Яркий пример тому — вода. Лед, образующийся при замораживании, имеет ажурную структуру, поэтому его плотность меньше, чем у жидкой воды. Плотность же льдов высокого давления, множество примеров которых известны, может быть почти в три раза больше, чем плотность жидкой воды. По мере повышения давления атомы водорода все более «обобщаются»: кристаллическая структура уже не содержит индивидуальных молекул воды, связанных между собой водородными связями, но представляет собой кислородный каркас, внутри которого распределяются «общие» атомы водорода.
Разные структуры в зависимости от способа кристаллизации возникают и во многих других веществах: бензоле, уксусной кислоте, метаноле, этаноле, феноле, серной кислоте, ацетоне и др. Сравнение этих структур позволяет лучше понять роль различных типов межмолекулярных взаимодействий в формировании кристаллов, в том числе кооперативных.
Например, в кристаллах уксусной кислоты молекулы образуют не димеры, как в газовой или жидкой фазах, а бесконечные цепочки. В этом случае получается «проигрыш» по энергии индивидуальных водородных связей, зато «выигрыш» — по энергии всего ансамбля как целого. «Интересы» коллектива подчиняют себе «интересы» индивидуумов.
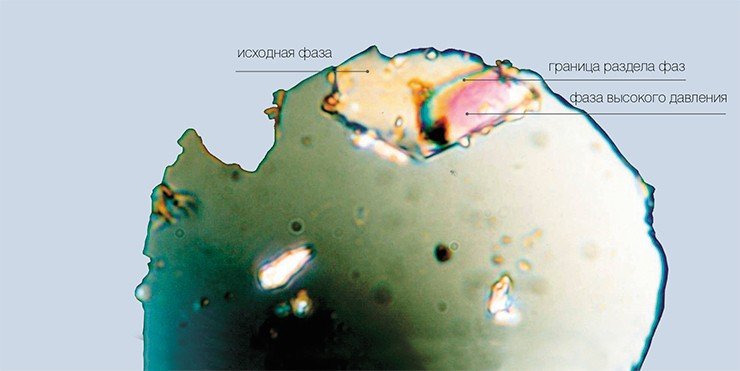
Высокие давления можно использовать не только для получения кристаллов веществ, жидких в нормальных условиях, но также для перекристаллизации твердых веществ. Если такое вещество растворить в жидкости и затем сжать раствор, то по мере повышения давления растворимость вещества будет уменьшаться и начнется процесс кристаллизации.
Таким способом нередко удается получать новые кристаллические структуры, отличные от тех, которые уже известны при нормальных давлениях. Некоторые из фаз вещества, возникших под воздействием высокого давления, удается сохранить даже после снятия нагрузки (так называемая «закалка»). Это необычное явление сегодня находит применение в различных областях, например при разработке новых лекарственных форм.
Кристаллы аминокислот
Аминокислоты, малые органические молекулы, являются «кирпичиками», из которых строятся важнейшие биополимеры — полипептиды и белки. Структура этих биополимеров характеризуется определенной последовательностью аминокислот (первичная структура), а также особой трехмерной «укладкой» молекул благодаря дополнительным взаимодействиям (например, водородным связям) между отдельными фрагментами полипептидных цепочек (вторичная структура).
В то же время аминокислоты способны образовывать особые кристаллические структуры, которые могут служить удобными моделями для исследований на стыке разных наук: физики, химии, биологии, а также в -области техники. Многие из подобных кристаллов являются пьезоэлектриками или обладают нелинейными оптическими свойствами; их применяют как лекарственные вещества или биологически активные добавки.
Наконец, кристаллы аминокислот могут использоваться в качестве имитаций отдельных фрагментов биополимеров. Почти во всех этих кристаллах в качестве строительных единиц используются молекулярные цепочки «голова к хвосту». И хотя в данных структурах молекулы связаны не ковалентными, а более слабыми водородными связями, аминокислотные цепочки обладают высокой степенью устойчивости к различным внеш-ним воздействиям и в течение длительного времени не разрушаются даже после растворения кристаллов.
Цепочки из аминокислот можно рассматривать в качестве простейших моделей биополимеров — пептидов, в которых за счет отщепления молекул воды образовались пептидные C—N связи. Ряд исследователей полагает, что склонность аминокислот к образованию подобных структур имеет прямое отношение к проблеме происхождения жизни. Полиаминокислотные цепочки — основа таких природных полимеров, как нить паутины или шелка, а кроме того искусственных полимеров (нейлон).
Исследования, проводимые при высоких давлениях, позволяют количественно измерить жесткость и прочность цепочек, построенных из разных молекул аминокислот, а также образуемых этими цепочками слоев и трехмерных сеток. При повышении давления может происходить и реорганизация трехмерных структур — так называемые полиморфные превращения. В некоторых структурах подобные полиморфные превращения возможны, в других — нет. Эта «способность» кристаллических структур напрямую связана с процессом фолдинга, т. е. с изменением вторичной структуры биополимеров.
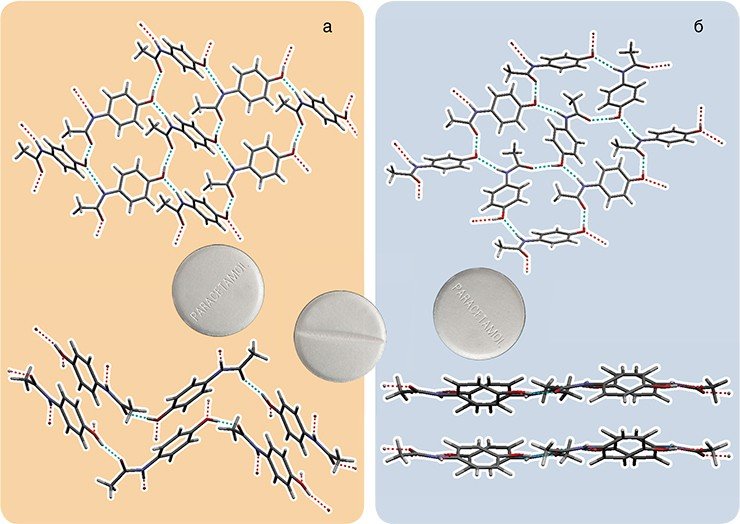
Полиморфные превращения в кристаллах аминокислот имеют аналоги среди процессов, протекающих в природных биополимерах. Например, одно из полиморфных превращений в кристаллах аминокислоты глицина, вызываемых давлением, сопровождается развертыванием тройных спиралей кристаллической решетки в слои. Аналогичный процесс описан для коллагена, белка соединительной ткани, обеспечивающего ее прочность. Можно также найти сходство между полиморфными переходами в кристаллах аминокислот и процессами образования амилоидов — жестких устойчивых структур, связанных с рядом тяжелых заболеваний инфекционной, воспалительной и опухолевой природы.
Исследование полиморфных переходов в кристаллах аминокислот, как и в других молекулярных кристаллах, осложняется тем, что к их описанию плохо применимы традиционные подходы, например построение фазовых диаграмм.
Подобные процессы часто далеки от состояния равновесия. Образование определенных фаз можно наблюдать только в особых режимах, в частности не при повышении давления, а «на обратном пути», при его снижении. На ход полиморфных превращений нередко влияет и скорость подачи нагрузки, и то, как долго вещество находится под высоким давлением. Так, при быстром росте давления может образовываться одна фаза вещества, а при медленном — совершенно другая. На ход превращения могут влиять и присутствующие в системе, даже в малых количествах, жидкости и газы. Отмеченные особенности, безусловно, осложняют работу, но в то же время делают ее более увлекательной.
Исследования молекулярных кристаллов при высоких давлениях еще только начинаются. Эта область науки сулит много интересных открытий и практических приложений, но достигнуть успеха можно лишь при тесном сотрудничестве инженеров, физиков, химиков, биологов, специалистов в области синтеза, кристаллизации, спектральных и дифракционных методов исследования.
И в Сибирском отделении Российской академии наук все предпосылки для этого созданы: в рамках Междисциплинарного интеграционного проекта уже сделаны первые шаги в этом новом и очень перспективном направлении.
Литература
1. Болдырева, Е. В. Высокие давления и изучение супрамолекулярных систем. — Новосибирск: Изд-во МДЭБТ НГУ, 2002.
2. High-Pressure Crystallography / ed. A. Katrusiak & P. F. McMillan. — Dordrecht: Kluwer, 2004.
3. Болдырева, Е. В. Высокие давления и супрамолекулярные системы // Изв. РАН. Сер. хим. наук. — 2004. — Т. 53. — № 7. — С. 1315—1324.
4. Boldyreva, E. V. Crystal of amino acids as a link between chemistry, biology and materials science // Magic, Models and Mysteries of Molecules / ed. J. Boyens. — Berlin, Heidelberg: Springer, 2007.