Менделеев: путь к Закону
Об истории открытия Периодического закона
Первая статья Д. И. Менделеева об этом законе начиналась следующими словами: «Систематическое распределение элементов подвергалось в истории нашей науки многим разнообразным превратностям». Это так. Но об одном Дмитрий Иванович умолчал: проблема «систематического распределения элементов» была для научного сообщества сугубо маргинальной, а то и просто недостойной внимания серьезного ученого. К примеру, когда один из предшественников Менделеева – Джон Ньюлендс – представил Лондонскому химическому обществу свой вариант классификации элементов (так называемый «закон октав»), один из присутствующих заметил: «А не пытался ли он [Ньюлендс] расположить элементы по алфавиту? Ведь любое расположение их может представлять случайные совпадения» (Newlands, 1866, с. 113). Таким образом, Менделеев взялся за тему, которая в то время не только не представлялась актуальной, но и вызывала насмешки. Но он все-таки решил всерьез заняться проблемой классификации элементов
 18 октября (по старому стилю) 1867 г. тридцатитрехлетний профессор Санкт-Петербургского университета Дмитрий Иванович Менделеев был переведен с кафедры технической химии на кафедру химии в звании ординарного профессора. Тогда же, в октябре, он начал читать лекции по неорганической химии для студентов I курса физико-математического факультета. И читал ежегодно вплоть до своего ухода из университета в 1890 г. Естественно, ему надо было рекомендовать студентам какой-то учебник, но ничего подходящего он не нашел и решил написать свой, который назвал «Основы химии» (первоначально задуманное название: «Основы химии, или общедоступное и понятное изложение сведений неорганической химии, ее теории и приложений»).
18 октября (по старому стилю) 1867 г. тридцатитрехлетний профессор Санкт-Петербургского университета Дмитрий Иванович Менделеев был переведен с кафедры технической химии на кафедру химии в звании ординарного профессора. Тогда же, в октябре, он начал читать лекции по неорганической химии для студентов I курса физико-математического факультета. И читал ежегодно вплоть до своего ухода из университета в 1890 г. Естественно, ему надо было рекомендовать студентам какой-то учебник, но ничего подходящего он не нашел и решил написать свой, который назвал «Основы химии» (первоначально задуманное название: «Основы химии, или общедоступное и понятное изложение сведений неорганической химии, ее теории и приложений»).
Сам Менделеев вспоминал: «Писать начал, когда стал после Воскресенского читать неорганическую химию в Университете и когда, перебрав все книги, не нашел, что следует рекомендовать студентам. Писать заставляли и многие друзья, напр. Флоринский, Бородин. Писавши, изучил многое» (Архив Д. И. Менделеева. Т. 1, 1951, с. 52). Это – версия Менделеева. Однако был еще один важный стимул, заставивший Дмитрия Ивановича засесть за написание «толстого» учебника, – деньги.
К тому времени он уже начал реконструкцию недавно купленного в Тверской губернии имения Боблово, которое намеревался сделать «образцовым» и проводить там сельскохозяйственные опыты. Кроме того, у него уже была семья – сын, а вскоре должен был родиться и второй ребенок. Гонорар за учебник, который можно было переиздавать, мог стать неплохим дополнительным источником дохода. По словам Менделеева, «так как издавал сам, то получились и средства, а потом эта книга дала мне главный побочный доход – новыми изданиями» (Там же, с. 53). Правда, Дмитрий Иванович забыл упомянуть, что на издание «Основ», причем как на первое, так и на второе, университет назначил ему денежное пособие.
Д. И. Менделеев стоял у истоков российской метрологии. Точности измерения он уделял огромное значение, еще будучи студентом. «Наука начинается с тех пор, как начинают измерять, – считал он. – Точная наука немыслима без меры». Для своих опытов Менделеев или сам проектировал и мастерил приборы, или заказывал их у самых лучших мастеров. «Прототипом всех точных приборов» считал он весы. Точности взвешивания ученый уделял особое внимание, считая этот вид измерений наиболее результативным при проведении исследований«…Мое сочинение, – писал Менделеев, – не есть учебник: это, скорее, изложение целой совокупности моих воззрений, часть которых вошла потом в мемуары, много раз публиковавшиеся. Сам я, в изложении своих лекций, его не придерживаюсь» (Менделеев, 1876, с. 4).
Первый выпуск «Основ» был опубликован в конце мая или в начале июня 1868 г. Летом этого года он работал уже над вторым выпуском учебника, который был закончен в марте 1869 г. Именно в процессе работы над «Основами» Менделеев открыл Периодический закон.
Первая проба
История открытия Периодического закона и создания Периодической системы сложна и запутана, поэтому дальше я изложу лишь общий путь Менделеева к главному достижению его жизни. Начну со свидетельства самого Дмитрия Ивановича:
«Первая проба, сделанная в этом отношении, была следующая: я отобрал тела с наименьшим атомным весом и расположил их по порядку величины их атомного веса. При этом оказалось, что существует как бы период свойств простых тел, и даже по атомности элементы следуют друг за другом в порядке арифметической последовательности величины их пая:

1. «Не выражаются ли свойства элементов в их атомном весе, нельзя ли на нем основать систему?» (Там же, с. 18).
2. При расположении элементов в порядке возрастания их атомных весов наблюдается «как бы период свойств». Тем самым он если и не предложил (пока!) полную формулировку Периодического закона, то, по крайней мере, ухватил его суть – периодический характер изменения свойств элементов с изменением их атомных весов, и все дальнейшие его действия были направлены на проверку этой пока еще гипотезы.
3. Нельзя ли построить систему элементов из структурных блоков следующего вида:

Иными словами, Менделеев решил выстроить систему элементов укладыванием штабелями фрагментов типа (1) так, чтобы атомные веса увеличивались сверху вниз и слева направо.
Джон Ньюлендс (1837–1898) – английский физик и химик. В 1864 г. опубликовал таблицу, в которой расположил все известные элементы в порядке увеличения их атомных весов, используя данные С. Канниццаро. Ньюлендс пронумеровал элементы, сопоставил их номера с их свойствами и, отметив, что элементы с аналогичными свойствами регулярно повторяются, сделал вывод: «Восьмой элемент, начиная с данного элемента, является своего рода повторением первого, подобно восьмой ноте октавы в музыке…». Хотя термин «периодичность» он не употреблял, но по сути речь шла именно о периодическом изменении свойств элементов«Галоиды [галогены] и щелочные металлы, – писал Менделеев в «Основах химии», – составляют в некотором смысле самые крайние по характеру элементы, все прочие элементы или суть металлы, приближающиеся до некоторой степени к щелочным металлам и по способности давать соли и по отсутствию водородных соединений [гидриды металлов тогда еще не были открыты. – И. Д.], но они не столь энергичны, как щелочные металлы. … Наконец, есть еще разряд элементов, таких как углерод и азот [речь идет о простых веществах. – И. Д.], в которых ни металлических, ни галоидных свойств не выражено с резкостью и которые в этом отношении занимают промежуток между двумя вышеупомянутыми разрядами простых тел. Очевидно, что этот род простых тел составляет как раз переход между галоидными элементами и ясно металлическими. … Все это дает возможность распределить элементы между группами щелочных металлов и галоидов» (Менделеев, 1871 [на обл. 1870]. Ч. 2. Вып. 3).
Эти слова показывают, как Менделеев формировал «полюса» будущей системы и чем он предполагал заполнять пространство между ними. Его замысел был замечательным, но реализовать его было непросто, поскольку Дмитрий Иванович столкнулся со следующими трудностями:
– не все элементы были к тому времени известны;
– не для всех открытых элементов были правильно определены атомные веса (и было неясно, какие из них правильные, а какие – нет);
– число элементов в разных фрагментах типа (1) оказывалось различным: между Li и F, как и между Na и Cl, умещалось по пять элементов, тогда как между К и Br надо было разместить не менее 12 известных в то время элементов:

– существовало два типа аналогий между элементами, и это надо было как-то выразить в системе. На этой последней трудности следует остановиться детальней.
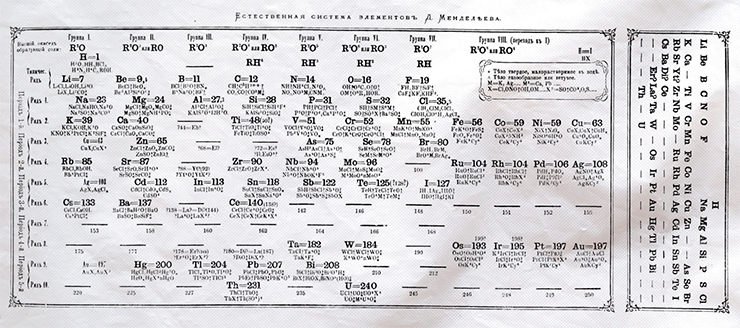
В варианте (2) в первых двух строчках элементы-аналоги стоят друг под другом, что естественно. А в третьей строке As – прямой аналог P, Se – прямой аналог S и Br – прямой аналог Cl оказались где-то в стороне, их потеснили другие элементы. Тогда Менделеев решил длинные строчки «сломать»:
Он знал, что «ванадию, судя по исследованиям Роско*, должно быть дано место в ряду азота, его атомный вес (51) заставляет его поместить [в одном столбце] между фосфором и мышьяком. Физические свойства оказываются ведущими к тому же самому определению положения ванадия: так, хлорокись ванадия VOCl3 представляет жидкость, имеющую при 14° удельный вес 1,841 и кипящую при 127°, что и приближает ее, а именно ставит выше соответственного соединения фосфора (т. е. POCl3 – И. Д.)» (Менделеев, 1869, с. 24–26).
* Генри Энфилд Ро́ско – британский химик, один из первых исследователей химии ванадия. – И. Д.Получается, что если присмотреться, то ванадий и фосфор (равно как хром и сера, хлор и марганец) не совсем «чужие» друг другу элементы. Между ними кое-какое сходство есть, но проявляется оно только в высших соединениях. Например, высшая степень окисления хлора и марганца равна 7 (потом они окажутся в седьмой группе), и соответствующие высшие соединения этих элементов (Cl2O7 и Mn2O7; KClO4 и KMnO4, и т. д.) проявляют сходные свойства. Менделеев об этом знал и до 1869 г. Более того, об этом знали многие химики до него, но оставался вопрос: сходство высших соединений (скажем, кислородных) обусловлено сходством самих элементов, оказавшихся в особом, «предельном» состоянии, или же кислорода в них так много, что он «стирает» различия в природе самих элементов? Для Менделеева это был один из самых трудных вопросов. И ответ на него он искал около года, если не больше.
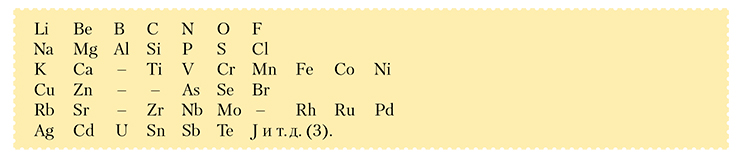
Итак, вариант системы типа (3), который вполне устраивает нас, для Дмитрия Ивановича в начале 1869 г. был совершенно неприемлем. И главная причина его отказа от этого варианта состояла в отсутствии ясных и строгих критериев объединения в один столбец элементов, как тогда говорили, разных разрядов, или, если использовать современную терминологию, элементов главных и дополнительных подгрупп. При том что Менделеев понимал: свойства элементов определяются не только величиной и весом атома, но и «внутренними различиями материи, входящей в состав атомов», т. е. внутриатомной структурой (Менделеев, 1871 [на обл. 1870]. Ч. 2. Вып. 3). Но это понимание тогда оставалось лишь блестящей догадкой.

Что делать дальше? В ситуации, когда критерии объединения элементов обоих «разрядов» в единую систему были еще не ясны, ему представилось более естественным разъединить элементы разных «разрядов». Именно поэтому, имея в руках вариант системы, по формальным признакам весьма близкий к тому, который впоследствии получил название «естественной системы» и который сейчас можно видеть в школьных и вузовских учебниках, Менделеев отказался размещать элементы «второго разряда» (дополнительных подгрупп) среди элементов первого, поскольку в этом случае «разорвалась бы естественность связи членов одного … ряда» (т. е. членов одной главной подгруппы, как бы мы сегодня сказали) (Менделеев, 1869, с. 26). Менделеев поначалу даже не решился объединить в один столбец Be=9,4; Mg=24; Ca=40; Zn=65; Sn=87; Cd=112 и Ba=137.
Задача объединения элементов разных «разрядов» лишь на первый взгляд может показаться сравнительно несложной. Надо было перегруппировать шестьдесят с лишним элементов, а не просто выбросить треть их из системы. При этом надо было сохранить их расположение в порядке возрастания атомных весов и, по возможности, периодический характер изменения их свойств. Задача осложнялась тем, что Cu, Ag, Zn и Cd Менделеев поначалу относил к элементам первого разряда (т. е. к элементам главных подгрупп).
Может быть, тогда подойдет другая форма, которую потом станут называть «длинной» (или «длиннопериодной»):

После долгих мучений Менделеев создал вариант системы, который с несвойственной ему скромностью назвал «Опытом системы элементов, основанной на их атомном весе и химическом сходстве» (далее сокр. «Опыт»). На рукописном листке с «Опытом» он проставил дату: 17 февраля 1869 г. (по ст. ст.).

Составление «Опыта» и написание статьи «Соотношение свойств с атомным весом элементов» подвели черту под важным этапом работы Менделеева по созданию рациональной систематики элементов.
Теперь он был уверен, что:
– атомный вес является одним из важнейших параметров, определяющих коренные свойства элементов, и потому «распределение элементов по атомному их весу не противоречит естественному сходству, существующему между элементами, а напротив того, прямо на него указывает» (Менделеев, 1869, с. 18–20);
– существующее «между естественными свойствами элементов и величиной их атомного веса» некоторое «точное отношение» имеет периодический характер в том смысле, что «элементы, расположенные по величине их атомного веса, представляют явственную периодичность свойств».
Опыт – сын ошибок трудных
 Итак, Менделеев понял главное – характер фундаментальной зависимости, которая связывает между собой все химические элементы. Но полученный результат никак не мог считаться окончательным, поскольку «Опыт» при всех его достоинствах не обладал ни цельностью, ни должной естественностью. Так, переходные элементы «второго разряда» явно демонстрировали известные аналогии с элементами «первого», в «Опыте» же они оказывались всего лишь «навесом» над остовом системы.
Итак, Менделеев понял главное – характер фундаментальной зависимости, которая связывает между собой все химические элементы. Но полученный результат никак не мог считаться окончательным, поскольку «Опыт» при всех его достоинствах не обладал ни цельностью, ни должной естественностью. Так, переходные элементы «второго разряда» явно демонстрировали известные аналогии с элементами «первого», в «Опыте» же они оказывались всего лишь «навесом» над остовом системы.
Отсюда сложное отношение Менделеева к своему созданию. Включив «Опыт» в первую часть «Основ» и в статью «Соотношение свойств» (не считая отдельных листков с таблицей, отпечатанных для рассылки коллегам), Менделеев больше никогда его не публиковал.
Только в статье «О месте церия в системе элементов», представленной Физико-математическому отделению СПб Академии наук академиком Н. Н. Зининым и адъюнктом А. М. Бутлеровым на заседании 24 ноября 1870 г. и опубликованной на немецком языке в «Бюллетенях» Академии, Менделеев приводит таблицу, озаглавленную просто и кратко «Система элементов» (Mendeleev, 1871). Именно последняя и стала прообразом известной сегодня короткой формы системы, которую Менделеев уже в другой статье назвал «Естественной системой химических элементов» (1870). Графическое выражение Периодического закона, представленное в «Естественной системе», является более совершенным и зрелым. Оно было включено Менделеевым во вторую часть первого издания «Основ химии» (1871).
К концу 1870 г. Дмитрий Иванович понял, что «предельные» (высшие) формы кислородных соединений и их свойства определяются не «самими свойствами кислорода» и не наличием «грани О4», т. е. особо устойчивой группировки из четырех кислородных атомов (например, H2SO4 ~ H2CrO4; HClO4 ~ HMnO4 и т. д.), но «состоянием», т. е., в конечном счете, природой элемента, находящегося в его высших кислородных соединениях.
 Определенное влияние на размышления Менделеева о соотношении элементов разных разрядов могли оказать соображения, высказанные в 1869 г. некоторыми отечественными химиками. Так, Н. Н. Бекетов, выступая в 1869 г. на Втором съезде естествоиспытателей в Москве с докладом, посвященном концепции атомности (валентности), сформулировал некоторые идеи, которые вполне могли привлечь внимание Менделеева:
Определенное влияние на размышления Менделеева о соотношении элементов разных разрядов могли оказать соображения, высказанные в 1869 г. некоторыми отечественными химиками. Так, Н. Н. Бекетов, выступая в 1869 г. на Втором съезде естествоиспытателей в Москве с докладом, посвященном концепции атомности (валентности), сформулировал некоторые идеи, которые вполне могли привлечь внимание Менделеева:
«Причины, обусловливающие предел соединения двух элементов, могут быть двоякого рода, чисто геометрические и физико-химические. Первые зависят от формы частичек, которая допускает присоединение только известного числа частичек другого тела; вторые, зависящие от химических свойств материи, выражаются по преимуществу количеством теплоты, отделяющейся при соединении. Чем более два элемента при своем соединении могут выделять теплоты, тем они способнее к соединению и тем прочнее происшедшее соединение. Потому мы можем себе представить, что непрочность возможного по аналогии соединения не позволит ему образоваться… Итак, по крайней мере два фактора имеют влияние на предел соединения, а следовательно, и на атомность элементов. А потому естественно, что когда одно условие, по-видимому, постоянное (форма частиц), допускает возможность неизменной атомности, другое, изменяющееся (химическая энергия соединения), своим влиянием изменяет предел, а следовательно, и самое атомность» (Бекетов, 1869, с. 236).
Другое сообщение, которое могло заинтересовать Менделеева, было сделано на том же съезде А. Н. Энгельгардтом. Его идея состояла в том, что деление элементов на металлические и неметаллические относительно, высшие кислородные соединения таких типичных металлов, как марганец и хром, обладают кислотными свойствами, что сближает их с высшими оксидами йода, селена и т. д. А потому, если прав Бекетов, сходство, скажем, перхлората и перманганата калия, как и сходство высших оксидов марганца и хлора, обусловлено не влиянием кислорода, но сходством самих элементов, т. е. близостью их «химической энергии».
«Дмитрий Иванович, пора заняться работать»
Но вернемся к более ранним событиям 1869 г. Менделеев прекрасно понимал значимость сделанного им открытия. Но предстояло еще убедить в этом других, для чего следовало прежде всего познакомить отечественных и, что особенно важно, зарубежных химиков с открытым им законом и созданной на его основе системой элементов. Это было важно и с приоритетной точки зрения.
Как известно, в день создания «Опыта» Менделеев, который «не скучал изучать все ветви сельского хозяйства», должен был ехать в Тверскую губернию обследовать артельные сыроварни Н. В. Верещагина (Архив Д. И. Менделеева, т. 1, с. 58). Открытие Периодического закона вынудило его отложить поездку на 12 дней, чтобы закончить статью «Соотношение свойств с атомным весом элементов». Рукопись он передал Н. А. Меншуткину для публикации в «Журнале Русского химического общества»* и для сообщения о своем открытии на предстоящем заседании РХО. А сам 1 марта (ст. ст.) 1869 г. отправился на сыроварни.
* Н. А. Меншуткин был делопроизводителем и редактором журнала РХО. В1860-х гг. он стал близким другом и помощником Менделеева.**До сих пор в литературе можно встретить утверждения, будто Менделеев «в марте 1869 года на заседании Русского химического общества … доложил об открытии периодического закона» (см., например: Спектор, 2017, с. 10).
Меншуткин просьбу Менделеева исполнил и 6 марта (ст. ст.) сделал от имени последнего сообщение о Периодическом законе**.Собрания Общества начинались в восемь вечера и обычно продолжались часа два. В тот вечер было заслушано десять докладов, в основном по органической химии. Вряд ли у Меншуткина было более 10 минут на сообщение о системе Менделеева. В протоколе Общества сказано: «За отсутствием Д. Менделеева обсуждение этого сообщения отложено до следующего заседания» (ЖРХО, 1869, с. 35). Следующее собрание состоялось 3 апреля того же года, но вопрос о классификации элементов ни тогда, ни позднее даже не поднимался.
В литературе часто дискутируется вопрос: почему Менделеев сам не выступил с докладом о своем открытии? Ответы давались разные. На мой взгляд, главная причина, по которой Менделеев не решился сам докладывать коллегам о своем открытии, состояла в неразрешенности многих важных вопросов. «Опыт» стал своего рода компромиссным вариантом системы. В 1869 г. физико-химическая часть таксономической задачи – открытие периодического характера зависимости свойств («химической энергии») элементов от их атомных весов – оказалась куда более продвинутой, нежели ее химическая часть – определение критериев объединения в одну группу неполных аналогов, т. е. элементов разных разрядов.
 Возможно, была и другая причина «неторопливости» Менделеева в обнародовании своего открытия. Он прекрасно понимал, что никакой реакции на него не будет, как в силу периферийности темы, так и по причине весьма настороженного отношения к нему многих представителей российского химического сообщества. Его студенческая и магистерская диссертация были не экспериментальными работами с неясными результатами; исследования капиллярности в Германии скорее относились к области физики, а докторская диссертация («Соединение спирта с водой») имела явно прикладную направленность…
Возможно, была и другая причина «неторопливости» Менделеева в обнародовании своего открытия. Он прекрасно понимал, что никакой реакции на него не будет, как в силу периферийности темы, так и по причине весьма настороженного отношения к нему многих представителей российского химического сообщества. Его студенческая и магистерская диссертация были не экспериментальными работами с неясными результатами; исследования капиллярности в Германии скорее относились к области физики, а докторская диссертация («Соединение спирта с водой») имела явно прикладную направленность…
Это отношение с афористической краткостью выразил акад. Н. Н. Зинин: «Дмитрий Иванович, пора заняться работать». Но и игнорировать РХО Менделеев не мог, поскольку то была единственная профессиональная химическая среда в России, объединявшая химиков, работавших в самых разных местах. Именно в журнале Общества естественней всего было публиковать на русском языке статью об открытии закона, для чего необходимо было сделать хотя бы формальное предварительное представление ее на заседании РХО.
Таким образом, Менделеев нашел оптимальный путь презентации своей работы: доклад Н. А. Меншуткина, редактора журнала, от имени автора предстоящей публикации, и без риска излишних словопрений. И только в научно-популярной литературе легковесно-пошловатого толка можно встретить утверждения о том, какое колоссальное впечатление произвело сообщение об открытии Периодического закона на членов РХО.
Вопрос приоритета
Вернувшись из командировки, Менделеев, вероятно, поинтересовался у Меншуткина, как прошло заседание, и тот сообщил, что по сути никакой реакции не было, и решено было вернуться к теме доклада в апреле.
 Между тем сам Менделеев решил – преимущественно из соображений приоритетного свойства – отпечатать сотни полторы листков с «Опытом» и разослать их российским и иностранным химикам. Как показал П. А. Дружинин (Дружинин, 2019), листки были отпечатаны около 17 марта: 100 экземпляров с русским заглавием, 50 – с французским. По мнению М. Гордина, тот факт, что «русских» листков было вдвое больше «французских», означает, что «в тот момент целевой аудиторией Менделеева была российская, а не международная» (Gordin, 2004, с. 28). Я думаю, что указанный факт объясняется тем, что, во‑первых, в России у Менделеева было больше знакомых химиков, чем за границей, плюс студенты, интересующиеся новыми научными идеями, а во‑вторых, соображениями экономии (о чем далее).
Между тем сам Менделеев решил – преимущественно из соображений приоритетного свойства – отпечатать сотни полторы листков с «Опытом» и разослать их российским и иностранным химикам. Как показал П. А. Дружинин (Дружинин, 2019), листки были отпечатаны около 17 марта: 100 экземпляров с русским заглавием, 50 – с французским. По мнению М. Гордина, тот факт, что «русских» листков было вдвое больше «французских», означает, что «в тот момент целевой аудиторией Менделеева была российская, а не международная» (Gordin, 2004, с. 28). Я думаю, что указанный факт объясняется тем, что, во‑первых, в России у Менделеева было больше знакомых химиков, чем за границей, плюс студенты, интересующиеся новыми научными идеями, а во‑вторых, соображениями экономии (о чем далее).
Заметим, что в отпечатанных в марте 1869 г. листках с «Опытом» нет никаких пояснений к приведенной таблице. Тому были свои причины: Менделеев торопился утвердить свой приоритет. В России у него конкурентов не было, но за границей многие занимались классификацией элементов и, что называется, наступали ему на пятки. Если бы он включил в эти листки дополнительную информацию, то для их печати потребовалось бы предварительное цензурное разрешение, что заняло бы время (Дружинин, 2019). А пока статья не вышла из печати, нужно было сделать хоть какой-то шаг для утверждения приоритета.
Заметим, что на беловом варианте «Опыта» Менделеев делает следующую запись: «Бумагу взять такую, по которой можно писать, но тонкую, чтобы было легко [по весу]». Согласно пояснению П. А. Дружинина, «пожелание легкой бумаги имело причину: Менделееву, человеку, умеющему считать деньги, требовалось, чтобы письмо не превышало минимального веса международных писем (15 г с учетом веса конверта и, возможно, сопроводительной записки), поскольку за отправку даже одного такого письма в государства Германского почтового союза в самом дешевом варианте взималось 14 коп. серебром (Там же, с. 118). Как видим, Дмитрий Иванович не желал оплачивать из своего кармана даже дополнительные расходы по утверждению Периодического закона.
Уже в начале апреля 1869 г. французский вариант «Опыта» был опубликован в немецком «Журнале практической химии» (Mendeleeff, 1869).
Разумеется, Менделеев осознавал недостаточность рассылки листков с «Опытом» для получения приоритетных гарантий. Поэтому, как только вышел номер ЖРХО с его статьей о Периодическом законе*, он немедленно, в мае 1869 г., составил ее краткую аннотацию из трех частей: заглавие, таблица («Опыт») и основные выводы. Менделеев предполагал опубликовать этот реферат в немецком ежемесячном полуреферативном журнале Zeitschrift für Chemie, который был основан группой доцентов Гейдельбергского университета.
*Не позднее 8 мая (ст. ст.) 1869 г. (Дружинин, 2019).Сам Менделеев, изучавший немецкий язык в гимназии и в институте, а затем два года бывший на стажировке в Германии, тем не менее чувствовал себя в немецком неуверенно, особенно когда надо было написать научную статью. Поэтому он воспользовался предложением одного из редакторов этого журнала, Ф. Ф. Бейльштейна, сдавать статьи и рефераты только на русском.
Но Бейльштейн, крайне загруженный работой, отдал реферат Менделеева своему ассистенту по Технологическому институту А. А. Ферману. И тот при переводе первого и ключевого положения реферата – «элементы, расположенные по величине их атомного веса, представляют явственную периодичность свойств» – вместо термина «периодичность» использовал термин stufenweise, т. е. ступенчатое (последовательное, постепенное) изменение (Mendeleeff, 1869, с. 405).
 Б. М. Кедров (1953), по свойственной многим советским и российским авторам привычке в любой ошибке или глупости видеть «вражеские происки», тут же безапелляционно заявил: «Такие искажения не могут быть случайностью; они свидетельствуют о явной злонамеренности составителя реферата, исказившего основное содержание великого открытия, сделанного русским ученым, и пытавшегося представить это открытие в виде простого сведения элементов в таблицу». Бонифатию Михайловичу даже не пришло в голову, что для сознательного искажения «основного содержания великого открытия» это содержание надо было еще понять и оценить его величие. А вот этого мы не наблюдаем в 1869 г., да и позднее, ни у кого из современников Менделеева, даже занимавшихся классификацией химических элементов. Что касается представления великого открытия русского ученого «в виде простого сведения элементов в таблицу», то интересно, что бы сказал Кедров, доживи он до наших дней, и узнав, что по инициативе Российской академии наук и Российского химического общества им. Д. И. Менделеева 2019 г. был объявлен «Международным годом Периодической таблицы»?
Б. М. Кедров (1953), по свойственной многим советским и российским авторам привычке в любой ошибке или глупости видеть «вражеские происки», тут же безапелляционно заявил: «Такие искажения не могут быть случайностью; они свидетельствуют о явной злонамеренности составителя реферата, исказившего основное содержание великого открытия, сделанного русским ученым, и пытавшегося представить это открытие в виде простого сведения элементов в таблицу». Бонифатию Михайловичу даже не пришло в голову, что для сознательного искажения «основного содержания великого открытия» это содержание надо было еще понять и оценить его величие. А вот этого мы не наблюдаем в 1869 г., да и позднее, ни у кого из современников Менделеева, даже занимавшихся классификацией химических элементов. Что касается представления великого открытия русского ученого «в виде простого сведения элементов в таблицу», то интересно, что бы сказал Кедров, доживи он до наших дней, и узнав, что по инициативе Российской академии наук и Российского химического общества им. Д. И. Менделеева 2019 г. был объявлен «Международным годом Периодической таблицы»?
Скорее всего, термин «периодический», возвращаюсь в XIX в., переводчик счел не вполне уместным, поскольку в математике периодической называется функция, повторяющая свои значения через некоторый регулярный интервал аргумента. Тогда как в случае системы элементов такого, строго говоря, не наблюдается: через некоторое число элементов (в разных случаях разное) повторяются элементы-аналоги. Иными словами, строгое математическое понимание периодического изменения в случае системы элементов «размывается». В то же время немецкое существительное Stufe имеет значения: ступень; ярус, фаза, стадия; интервал, градация, этап. Видимо, переводчик решил, что речь у Менделеева идет о некотором чередовании свойств элементов, напоминающем чередование лестничных ступенек или театральных ярусов. И нельзя сказать, что такое понимание, при всех его недостатках, полностью извратило суть менделеевского открытия.
Среди химиков и преподавателей химии, особенно отечественных, традиционно было принято различать три понятия: Периодический закон, Периодическая система и Периодическая таблица (иногда две последние отождествляют). Периодический закон – это закон, лежащий в основе систематики элементов и (в формулировке Менделеева) гласящий: «Физические и химические свойства элементов, проявляющиеся в свойствах простых и сложных тел, ими образуемых, стоят в периодической зависимости … от их атомного веса». В настоящее время этот закон формулируется несколько иначе (свойства элементов ставятся в периодическую зависимость от заряда ядра), но, тем не менее, он остается важнейшим законом природы.
Периодическая система определяет общие принципы систематизации элементов в соответствии с Периодическим законом, т. е. топологию межэлементных отношений.

Периодическая таблица – это графическое выражение Периодического закона и системы. Как выразился Менделеев, «подобных распределений возможно большее число. Они не изменяют существа системы» и, добавлю, закона. И в настоящее время существует несколько сотен вариантов графического изображения Периодической системы (Mazurs, 1974).
К сожалению, об этих элементарных вещах в настоящее время стали забывать. И это проявилось, к примеру, в том, что 2019 г. стараниями российской научной элиты был объявлен Международным годом Периодической таблицы, но не Периодического закона, что довольно безграмотно как с исторической, так и с химической точки зрения, но хорошо гармонирует с имиджево-бессодержательным характером современной российской культуры.
Литература
Архив Д. И. Менделеева. Т. 1. Автобиографические материалы. Сборник документов / Сост. М. Д. Менделеева и Т. С. Кудрявцева. Под общей ред. С. А. Щукарева и С. Н. Валка. Л., 1951. С. 52.
Дружинин П. А. Загадка «Таблицы Менделеева»: История публикации открытия Д. И. Менделеевым Периодического закона. М.: Новое литературное обозрение, 2019. (Серия: История науки). С. 118.
Менделеев Д. И. Соотношение свойств с атомным весом элементов // Менделеев Д. И. Периодический закон. Основные статьи / Редакция, статьи и примечания Б. М. Кедрова. М., 1958.
Gordin M. D. A Well-ordered Thing. Dmitrii Mendeleev and the Shadow of the Periodic Law. New York: Basic Book, 2004. P. 28.








