Повреждение мембраны может не убить клетку, а запустить процесс клеточного старения
Подавляющее большинство клеток организма со временем стареют и перестают делиться, начиная специфически влиять на свое окружение. Недавно ученые обнаружили ранее неизвестный способ появления таких клеток – это открытие может послужить основой для разработки методов терапии ряда заболеваний, в том числе возрастзависимых
Как известно, неограниченно делиться могут лишь раковые и недифференцированные стволовые клетки. Обычная тканеспецифичная клетка после приблизительно 50 делений (предел Хейфлика) теряет эту способность, хотя еще долго может сохранять жизнеспособность и метаболическую активность. Такое состояние принято называть клеточное старение.
В отличие от молодых и здоровых клеток, стареющие секретируют особый спектр молекул, которые могут влиять не только на клетки-соседей и близлежащие ткани, но и на отдаленные органы. При этом такое воздействие может быть как негативным, способствующим старению и развитию рака, так и позитивным, помогающим заживлению ран.
Причины появления стареющих клеток в организме человека остаются предметом дискуссии, хотя известно, что его триггерами могут послужить повреждение ДНК, укорочение концевых участков хромосом (теломер), активация онкогенов, эпигенетические (надгеномные) изменения.
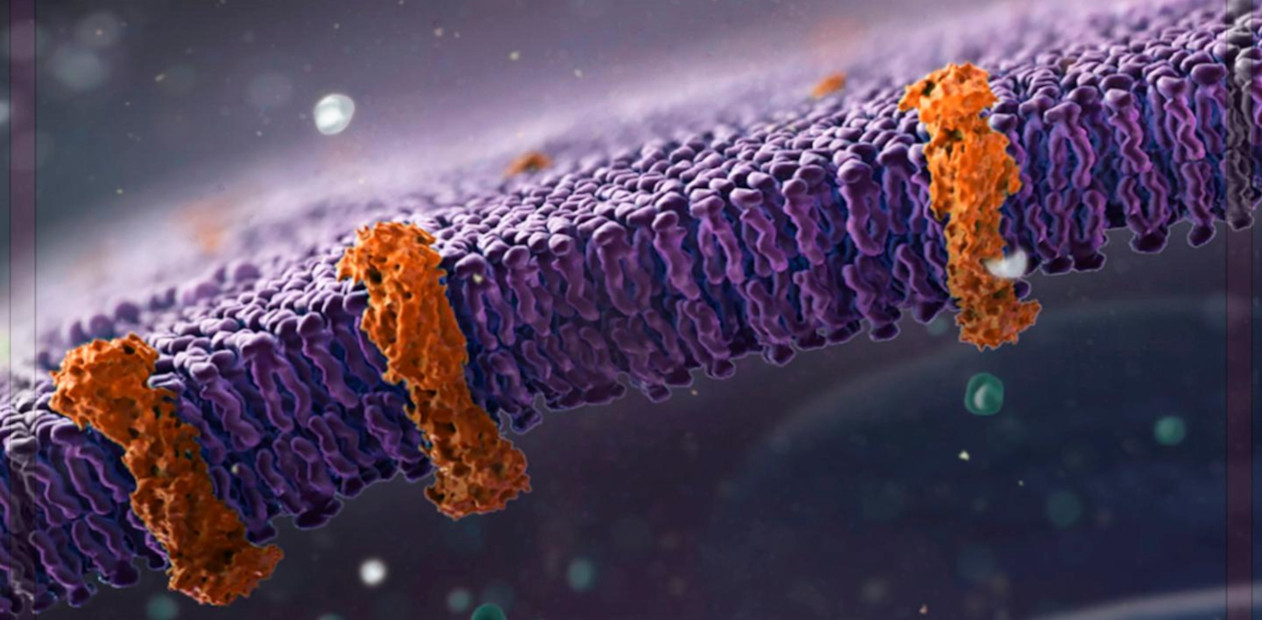
Недавно исследователи из Японии обнаружили еще один стимул, способствующий развитию фенотипа стареющей клетки, который связан с плазматической мембраной, отграничивающей содержимое клетки от окружающей среды.
Клеточная мембрана очень тонкая (ее толщина всего 5 нм) и легко повреждается в результате физического воздействия (например, мышечной работы) или атаки патогенов. Клетка легко устраняет небольшие дефекты мембраны – такие механизмы хорошо изучены. К ним относится, в частности, зависимое от ионов Ca2+ слияние с мембраной лизосом – окруженных мембраной клеточных органоидов, содержащих гидролитические ферменты. Серьезные повреждения мембраны приводят к гибели клетки в результате пироптоза – одного из вариантов программируемой клеточной смерти, связанного с воспалением.
До недавнего времени считалось, что возможны только два исхода повреждения мембраны – восстановление или гибель. Сейчас ученые обнаружили неожиданный третий вариант, реализующийся при повреждениях средней тяжести.
Исследования проводились на модельных объектах – клетках пекарских дрожжей (Saccharomyces cerevisiae) и фибробластах, клетках соединительной ткани человека. Для повреждения клеточной мембраны использовали оригинальный метод – обработку поверхностно-активным соединением додецилсульфатом натрия. В этом случае восстановление мембраны происходило с помощью Ca2+-зависимых механизмов.

Относительно мягкое повреждение мембраны в эксперименте ограничило число делений у дрожжевых клеток, а у фибробластов вызвало стресс-зависимое преждевременное старение. Механизм последнего включал в себя активацию гена, кодирующего белок p53, который участвует в регуляции клеточного цикла. Проанализировав профили активности генов в клетках с поврежденной и восстановленной мембраной с помощью методов биоинформатики, ученые доказали, что такие клетки действительно могут превращаться в стареющие. У них даже активировались гены, способствующие заживлению ран!
Итак, клетка при повреждении мембраны может «залечить» дефект, но через несколько дней превратиться в стареющую. Это означает, что такие клетки требуют к себе большего внимания.
Известно, что препараты, избавляющие организм от стареющих клеток, могут уменьшить развитие возраст-зависимых патологий. Также есть данные, что неэффективный «ремонт» повреждений мембраны вызывает различные заболевания. К примеру, мутации в гене, кодирующем белок TMEM16F, который участвует в репарации мембраны, провоцируют развитие синдрома Скотта, при котором нарушается свертываемость крови. Так что результаты исследования японских ученых могут помочь в разработке методов терапии болезней, связанных с повреждением мембран, и, возможно, самого старения.
Фото: https://ndla.no и https://www.flickr.com
Публикации по теме
Можно ли отменить старение?
Структура и длина теломер: загадкам нет конца
«Секрет продления жизни в том, чтобы ее не укорачивать»
Смерть ради жизни, или Терапевтический потенциал «клеточного самоубийства»