Инфракрасный диагност
Все важнейшие процессы жизнедеятельности протекают с выделением тепла, следствием чего является локальное повышение температуры в тканях и органах. Поверхностное распределение температуры служит зеркалом микроциркуляторного, периферического и центрального кровообращения, связанных, в свою очередь, с нейровегетативными реакциями и изменениями обмена веществ. Однако при многих патологических процессах нормальное распределение температуры на поверхности тела видоизменяется, причем зачастую такие температурные проявления опережают другие клинические проявления.
Визуализировать и вести количественный контроль за быстрыми изменениями температуры одновременно на всей поверхности тела позволяют технологии тепловидения. Матричные тепловизоры нового поколения отличают компактность, мобильность и удобный пользовательский интерфейс. Использование их в составе единого клинико-тепловизионного комплекса способно существенно увеличить информативность и повысить степень достоверности диагностического исследования
Значимость диагностики функционального состояния организма человека трудно переоценить. Ведь ослабление функции органа или системы служит предвестником заболевания на самых ранних стадиях развития патологии, когда морфологические изменения в пораженных участках еще не выражены. Как известно, «болезнь легче предупредить, чем излечить», поэтому так важны исследования по разработке медицинских технологий, направленных на выявление доклинических диагностических признаков.
 К сожалению, современные методы и подходы такой донозологической («предболезненной») диагностики отстают от обычных диагностических методов, используемых в ситуациях, когда симптомы заболевания уже явно выражены. Однако благодаря новейшим достижениям в физико-технических и биомедицинских науках сегодня разрабатываются перспективные, принципиально новые технологии тепловизионной доклинической диагностики, позволяющие расширить диагностический диапазон и значительно увеличить достоверность получаемых результатов.
К сожалению, современные методы и подходы такой донозологической («предболезненной») диагностики отстают от обычных диагностических методов, используемых в ситуациях, когда симптомы заболевания уже явно выражены. Однако благодаря новейшим достижениям в физико-технических и биомедицинских науках сегодня разрабатываются перспективные, принципиально новые технологии тепловизионной доклинической диагностики, позволяющие расширить диагностический диапазон и значительно увеличить достоверность получаемых результатов.
Все важнейшие процессы жизнедеятельности в организме человека протекают с выделением тепла, следствием чего является локальное повышение температуры в тканях и органах. Поскольку теплопродукция представляет собой неотъемлемое от жизни, физиологически обусловленное явление, определение параметров «теплового» статуса организма может дать много полезной информации о состоянии здоровья.
Как известно, человеку, как и любому гомойотермному (т. е. поддерживающему постоянную температуру тела) организму для поддержания температурного гомеостаза требуется сбрасывать избыточную тепловую энергию во внешнюю среду. Основным механизмом этого процесса при нормальных условиях является передача теплоты через кожу.
Однако при многих патологических процессах нормальное распределение температуры на поверхности тела видоизменяется, причем зачастую такие температурные проявления опережают другие клинические признаки. Дело в том, что поверхностное распределение температуры служит «зеркалом» микроциркуляторного, периферического и центрального кровообращения, связанного, в свою очередь, с нейровегетативными реакциями и изменениями обмена веществ. Именно поэтому определение изменений в тепловом статусе организма так важно для ранней постановки диагноза и проведения своевременного лечения.
Существует три основных типа тепловизионных камер, отличающиеся конструкцией встроенного в них детектора инфракрасного излучения. Самые простые тепловизоры имеют одноэлементный приемник излучения; более сложные – линейный (или линейчатый) фотоприемник. Наконец, в наиболее современных тепловизионных системах используется двумерный матричный фотодетектор.Чтобы отобразить двумерный объект с помощью одноэлементного или линейчатого фоточувствительного модуля, в тепловизор встраивают оптико-механическую сканирующую систему, что технически усложняет конструкцию тепловизионной камеры и влечет за собой ряд неблагоприятных эффектов: высокую шумность, увеличение веса, более низкую чувствительность и быстродействие по сравнению с матричными тепловизорами при том же формате кадра.
Поэтому одноэлементные и линейчатые камеры сегодня используют в основном лишь для решения специальных задач. Преимущественное распространение в мире приобретают матричные тепловизоры – тепловизоры нового поколения
Визуализировать и вести объективный количественный контроль за быстрыми изменениями температуры сразу на всей поверхности тела и сопоставлять это с физиологическими характеристиками организма на сегодня возможно только одним способом – с помощью тепловидения.
В ответ на интервенцию
В США значимость тепловизионного метода для практической медицины была подтверждена несколькими исследованиями, инициированными Управлением по контролю качества пищевых продуктов и лекарственных препаратов (FDA). Что касается нашей страны, то еще в СССР имелись утвержденные тепловизионные методики, однако стандарты, регламентирующие использование тепловизоров нового поколения, до сих пор отсутствуют.
Вместе с тем изучение современного состояния медицинской тепловизионной диагностики (Vainer, 2012) показало, что несмотря на высокую чувствительность этого метода, с помощью уже устоявшихся в данной сфере подходов до сих пор не удалось найти и описать хоть сколько-нибудь убедительные тепловизионные признаки, строго специфичные для тех или иных заболеваний человека.
Решить эту важнейшую задачу призвана так называемая интервентная тепловизионная диагностика – одно из наиболее перспективных направлений диагностического тепловидения (Вайнер, 2011). В рамках этого подхода организм рассматривается как своего рода «черный ящик», для выяснения свойств которого необходимо воздействие внешних возмущающих сигналов. При этом предполагается, что у здорового организма и организма с отклонениями регистрируемые отклики будут принципиально различаться, поскольку генерируемые извне возбуждения заведомо имеют определенную диагностическую направленность.
На практике во время интервентного тепловизионного обследования на организм оказывается определенное активное (провоцирующее) воздействие с регистрацией ответного отклика в реальном масштабе времени. Недавние исследования авторов этой статьи показали, что существенно улучшить достоверность диагноза можно благодаря комплексному подходу, который подразумевает синхронное сопровождение тепловизионного обследования другими аппаратными средствами медицинского контроля. К последним относится аппаратура для электрокардиографии, лазерной доплеровской флоуметрии (ЛДФ), позволяющей выявлять характеристики сосудистой микроциркуляции, пульсоксиметрии, неинвазивного определения артериального давления и др.
Ожидается, что применение именно такого комбинированного подхода совместно с использованием высокотехнологичных матричных тепловизоров нового поколения и с быстрой математической и компьютерной обработкой гетерогенных нестационарных тепловизионных термограмм позволит выявить наиболее ранние признаки развития патологического состояния организма, что и является конечной целью любой медицинской диагностики.
Инфракрасное «око»: новое поколение
Многие современные подходы в экспериментальном тепловидении ранее не могли развиваться по той причине, что в арсенале физического экспериментального, а также медицинского диагностического, оборудования отсутствовали матричные компьютеризированные тепловизионные камеры. Именно с приходом в медицину матричных тепловизоров нового поколения появилась возможность прецизионной регистрации быстрых реакций кровеносных сосудов и температурного отклика, задающего топографию теплообмена человека с внешней средой в ответ на активное воздействие на организм (Вайнер, 2004).
 В научно-исследовательском интеграционном проекте, в котором участвуют специалисты Института физики полупроводников им. А. В. Ржанова СО РАН, Центра новых медицинских технологий Института химической биологии и фундаментальной медицины СО РАН и Новосибирского научно-исследовательского института патологии кровообращения им. академика Е. Н Мешалкина, используется тепловизионная аппаратура матричного типа, быстродействие и чувствительность которой в десятки и сотни раз превышают аналогичные параметры тепловизоров прежних поколений.
В научно-исследовательском интеграционном проекте, в котором участвуют специалисты Института физики полупроводников им. А. В. Ржанова СО РАН, Центра новых медицинских технологий Института химической биологии и фундаментальной медицины СО РАН и Новосибирского научно-исследовательского института патологии кровообращения им. академика Е. Н Мешалкина, используется тепловизионная аппаратура матричного типа, быстродействие и чувствительность которой в десятки и сотни раз превышают аналогичные параметры тепловизоров прежних поколений.
Более совершенная аппаратура позволяет реализовать режим динамической тепловизионной диагностики во время обследования с применением провоцирующих воздействий (функциональных проб). Фотографическое качество получаемого изображения, широкий динамический диапазон, низкий уровень шума матричных тепловизоров позволяет уловить и количественно проанализировать в тепловом рисунке многие тонкие нюансы, бывшие недоступными для приборов, на базе которых построены практически все используемые сегодня тепловизионные медицинские методики.
Приборный арсенал
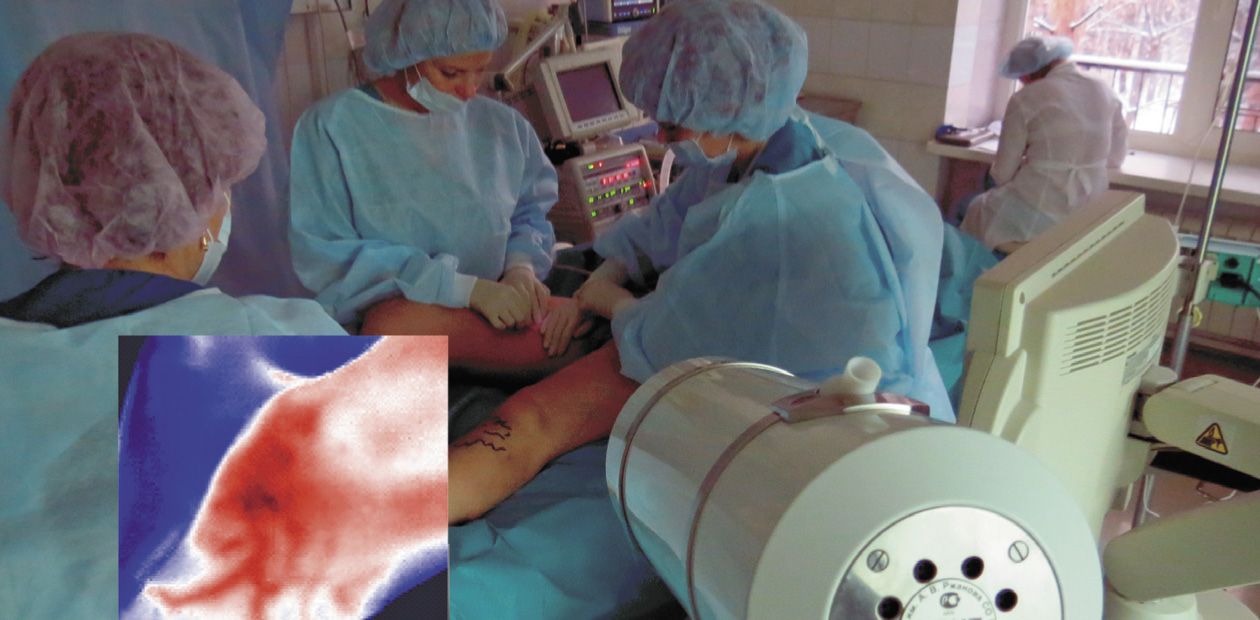
В работе, выполняемой в рамках вышеупомянутого интеграционного проекта, в качестве одного из базовых интервентных воздействий на организм применялось кратковременное сдавливание плеча круговой манжетой, давление воздуха в которой составляло около 200 мм рт. ст. (по сути, эта процедура аналогична той, которая проводится во время стандартного измерения артериального давления). Ранее такой прием уже применялся в подобных целях и оказался весьма результативным при проведении дифференциальной диагностики сосудистой реактивности организма (Vainer, Markel, 2010). При этом было обнаружено, что кратковременное сдавливание магистральных сосудов одной лишь верхней конечности вызывает выраженные температурные реакции одновременно во всех конечностях, причем у разных людей они могут очень сильно различаться.

По этой причине в новых экспериментальных исследованиях был использован ряд дополнительных методик, позволяющих независимо контролировать циркуляцию крови: прямой метод измерения кровотока в микрососудах – лазерная доплеровская флоуметрия, а также мониторинг основных показателей сердечно-сосудистой деятельности – неинвазивное измерение артериального давления, пульсоксиметрия, сфигмография, регистрация частоты сердечных сокращений.
В качестве основной измерительной тепловизионной системы использовался арсенид-индиевый матричный тепловизор ТКВр-ИФП/СВИТ с рабочим спектральным диапазоном 2,45—3,05 мкм. Тепловизионная камера устанавливалась на расстоянии нескольких метров от обследуемого так, что в поле зрения объектива попадали одновременно верхние и нижние конечности. Количественные результаты тепловизионных, ЛДФ- и остальных измерений непрерывно записывались и служили исходными данными для последующей цифровой и аналитической обработки.
Отметим, что при разработке диагностического комплекса помимо коротковолнового тепловизора было также проведено тестовое испытание тепловизора иного типа – неохлаждаемого прибора с рабочим спектральным диапазоном 8—14 мкм, использующего в качестве детектора излучения матрицу микроболометров на основе оксида ванадия (Демьяненко и др. 2010). Следует отметить, что несмотря на разные области спектральной чувствительности приборов, тепловые изображения кожи человека, полученные разными тепловизорами, отличались друг от друга незначительно.
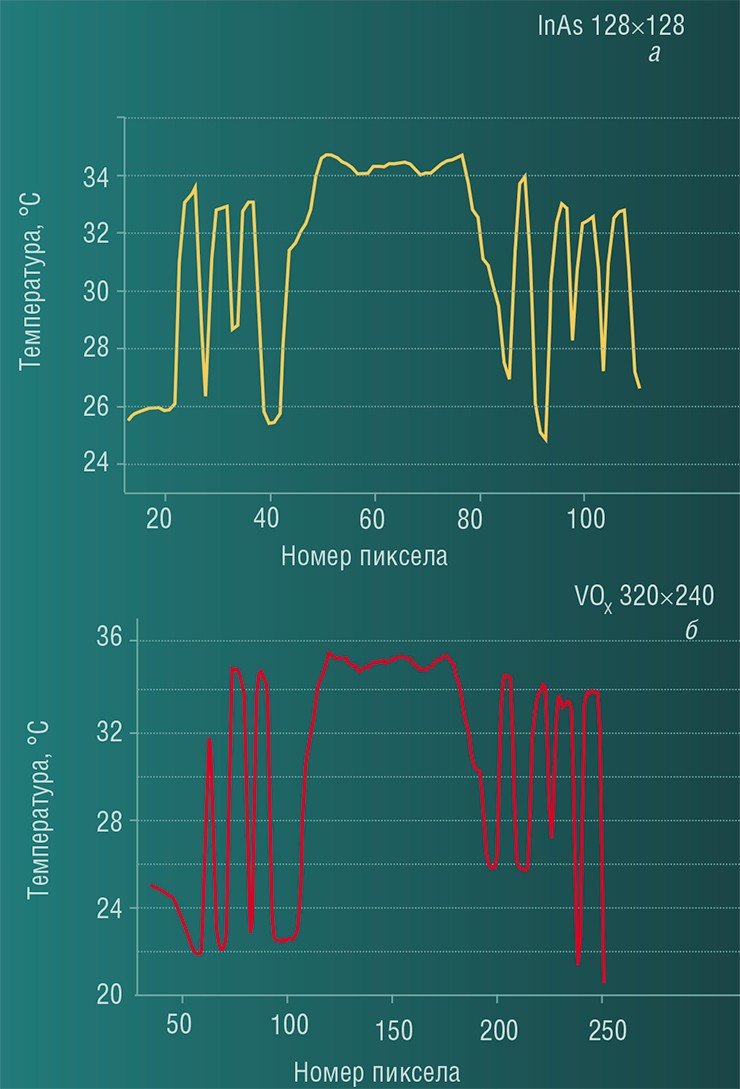
Тепловизоры на основе матричных микроболометрических приемников, не требующие глубокого охлаждения, очень перспективны для медицины. Отказ от использования жидких хладагентов или микрохолодильников замкнутого цикла, необходимых для поддержания низкой рабочей температуры детекторов инфракрасного излучения, позволяет снизить вес, размеры, энергопотребление и в конечном счете стоимость тепловизионной системы. Это также заметно повышает удобство в эксплуатации и доступность измерительного комплекса, поскольку отпадает необходимость всегда иметь в наличии жидкий азот.
Клиническая апробация
Пилотные исследования, проведенные на описанном выше универсальном клинико-тепловизионном диагностическом комплексе, дали ряд многообещающих результатов.
Как и ожидалось, в группе обследованных было зарегистрировано большое разнообразие общих реакций организма на внешнее интервентное воздействие. При этом периферические сосуды проявляли как полную синхронность в своем поведении, так и полную индифферентность по отношению к воздействию. Показатели ЛДФ среагировали на интервентное воздействие аналогичным образом, хотя этот отклик и оказался менее выраженным по сравнению с результатами тепловизионных измерений.
Ясно, что для корректной интерпретации данных, получаемых методом ЛДФ, требуется дальнейшее накопление материала и привлечение соответствующего математического анализа. Но уже имеющиеся результаты дают основание надеяться, что в итоге удастся установить точный характер связи между тепловизионными и ЛДФ- показателями физиологического статуса организма. Это предвосхищает интересную научную задачу о поиске соответствия между макроэффектами температурных изменений и изменениями кровоснабжения на микроциркуляторном уровне.
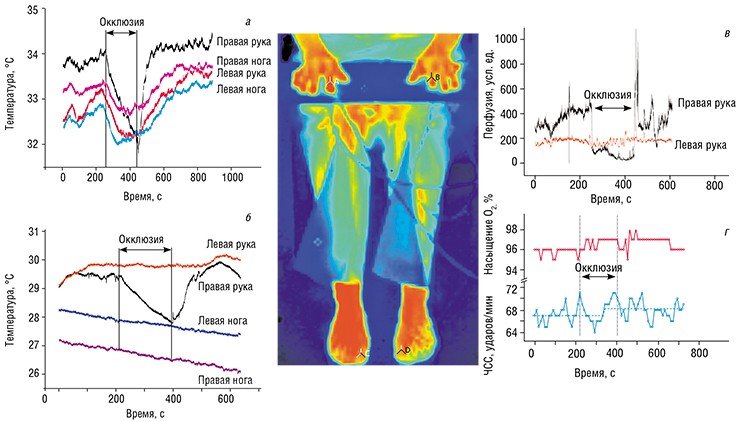
Следует отметить, что у лабильных участников исследований была также зафиксирована реакция со стороны таких показателей, как насыщение крови кислородом(в контралатеральной руке) и частота сердечных сокращений. Это подтверждает, что комбинированное тепловизионное обследование можно использовать для одномоментного получения объективных всесторонних данных о текущем состоянии организма.
На клинико-тепловизионном диагностическом комплексе были также проведены исследования, связанные с разработкой метода определения сосудистой реактивности, основанные на тепловизионном наблюдении реакции организма в ответ на общую гипоксию и гипероксию. Подобные условия реализуются, в частности, при проведении плановых хирургических операций под общим обезболиванием с искусственной вентиляцией легких кислородно-воздушной смесью с различным процентным содержанием кислорода.
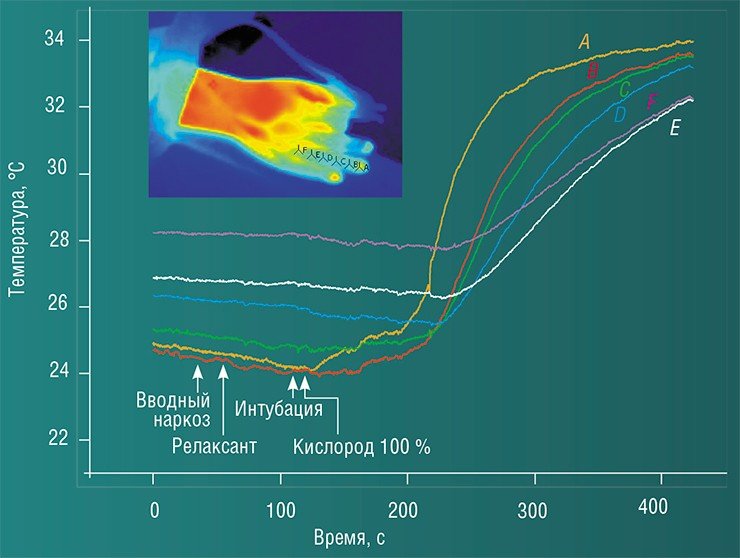
Особый интерес при этом вызывают закономерности изменения температурной топографии кожного покрова в состоянии общей гипоксии и гипероксии. Изучение подобных реакций может помочь продвинуться в понимании фундаментальных биофизических механизмов центральной регуляции организма человека.
В ходе стандартного этапа вводного наркоза и интубации трахеи на примере исследования температурной карты правой руки было показано, что повышенное содержание кислорода в газовой смеси вызывает резкое повышение температуры конечности: сначала пальцев, а в дальнейшем и всей кисти. Эти реакции могут быть связаны как с усилением метаболизма в периферических тканях, так и с расширением сосудов.
Полученные экспериментальные данные дают основание считать, что новые тепловизионные технологии являются весьма перспективными для применения в медицине благодаря их высокой информативности, безопасности и простоте обслуживания.
Тепловизоры нового поколения отличают компактность, мобильность и удобный интерфейс. Все это в полной мере относится как к тепловизорам с арсенид-индиевыми охлаждаемыми матричными детекторами среднего ИК-диапазона, так и к неохлаждаемым матричным тепловизорам длинноволнового ИК-диапазона с микроболометрическими детекторами на основе оксида ванадия.
Использование же подобных тепловизоров синхронно с другими независимыми методами контроля состояния организма в составе единого клинико-тепловизионного комплекса способно существенно увеличить информативность метода и повысить степень достоверности при постановке диагноза. Исследования в этом направлении – высокоперспективный и многообещающий тренд в современной медицинской науке.
Литература
Балакин В. В., Степаненко И. С., Кралькин А. Ю., Рахманов С. А., Вайнер Б. Г. Применение тепловидения и лазер-доплеровской флоуметрии в исследовании регуляторных процессов организма. // 50-я Междунар. студ. науч. конф. (шк. секц.). 7–9 апреля 2012 г., г. Новосибирск – 2012, Новосибирск, НГУ, с. 13.
Вайнер Б. Г. Интервентная тепловизионная диагностика в медицине и физиологии // Сб.: Современные тенденции в науке: новый взгляд// Материалы Межд. заоч. науч.-практ. конф. 29 ноября 2011 г.: в 9 ч. Ч. 7; Мин-во обр. и науки РФ. Тамбов: Изд-во ТРОО “Бизнес-Наука-Общество”. 2011. С. 21—24.
Демьяненко М. А., Фомин Б. И., Васильева Л. Л. и др. Неохлаждаемое микроболометрическое фотоприемное устройство формата 320´240 на основе золь-гель VOx // Прикладная физика, 2010. № 4. С. 124–130.
Вайнер Б. Г. Матричное тепловидение в физиологии: Исследование сосудистых реакций, перспирации и терморегуляции у человека. Новосибирск: Изд-во СО РАН, 2004. 96 с.
Vainer B. G. Applications of infrared thermography to medicine // Chapter 3 in Infrared Thermography Recent Advances and Future Trends. Bentham Science Publishers Ltd., Bentham e-Books, 2012. P. 61—84.
Vainer B. G., Markel A. L. Imaging and quantitative characterization of bilateral vasomotor reactions in humans using high-performance thermography // QIRT10: Proc. 10th edition of the Quantitative Infrared Thermography/Intern. Conf. July 27—30, 2010, Quebec City (Canada)/ X.P.V. Maldague (Ed). Canada: Universite Laval, 2010. P. 91—94.
Работа выполнена при финансовой поддержке СО РАН (интеграционный проект 2012–2014 гг. №40Б)
Авторы благодарят Е. В. Ковалеву, Ю. Г. Кулешову, А. И. Молокоедова, Я. В. Новикову и А. Ю. Патрушева (ЦНМТ СО РАН, Новосибирск), М. А. Демьяненко и И. В. Марчишина (ИФП СО РАН, Новосибирск), В. И. Баранова (ИФ СО РАМН, Новосибирск) за участие в обследованиях и предоставление необходимого оборудования