Рыбы Байкала в борьбе с атеросклерозом
О новом экспериментальном объекте для медицины
Нарушения обмена холестерола (холестерина) приводят к развитию атеросклероза и являются причиной инфаркта миокарда или инсульта. Атеросклероз и спровоцированные им сердечно-сосудистые заболевания вносят основной вклад в смертность среди населения России и других индустриально развитых стран. Для разработки эффективных методов ранней диагностики и лечения этого заболевания необходимо детально знать механизмы его развития. И в этом, как ни удивительно, могут помочь рыбы озера Байкал
Холестерин, или, как более правильно называют его по химической номенклатуре, холестерол и другие жиры переносятся по кровотоку в виде липопротеидов. Это достаточно сложно устроенные частицы, состоящие из «капли» жира и специальных белков, которые помогают взаимодействовать этим каплям с клетками организма. Липопротеиды либо частично обмениваются липидами с клетками, либо полностью захватываются ими.
Холестерол – плохой и хороший
Нарушения обмена холестерола в основном характеризуются повышением его уровня в крови, при этом изменяется соотношение его фракций. Есть несколько типов липопротеидов (или фракций холестерола). К первому типу относят липопротеиды очень низкой плотности (ЛПОНП) и липопротеиды низкой плотности (ЛПНП) – это атерогенные липопротеиды, как говорят пациенты, «плохой» холестерол, который как раз и является основной причиной развития атеросклеротических бляшек. Эти частицы переносят холестерол из печени к клеткам кровеносных сосудов. Второй тип – «хороший» холестерол, или антиатерогенные липопротеиды: липопротеиды высокой плотности (ЛПВП), которые транспортируют холестерол, наоборот, от сосудов к клеткам печени и таким образом сдерживают развитие атеросклероза. Печень служит главным регулятором обмена холестерола и других жиров и может выводить из организма его избыток с желчью.


Организм с помощью сложных биохимических, генетических механизмов, из которых еще далеко не все известны, поддерживает тонкое равновесие между фракциями «плохого» и «хорошего» холестерола крови. Это равновесие может быть нарушено, и важно знать механизмы, управляющие адаптацией обмена холестерола крови, сохраняющие баланс между «плохими» и «хорошими» фракциями при действии различных неблагоприятных факторов. Таких факторов достаточно много: диета с высоким содержанием холестерола, курение, накопление жира в клетках печени и многое другое (Климов, Никульчева, 1999).
Байкальская модель
Все виды животных обладают индивидуальными особенностями системы обмена холестерола, и это определяет степень устойчивости к развитию нарушений липидного обмена. Видоспецифичные различия в системах обмена холестерола – уникальный материал для выявления механизмов устойчивости к патологическим изменениям и их возможного использования в профилактике и лечении сердечно-сосудистых заболеваний человека. Например, сравнительный анализ соотношений фракций холестерола крови у устойчивых к развитию атеросклероза животных помог выявить в этом важную роль ЛПВП (Климов, Никульчева, 1999), благодаря чему холестерол ЛПВП и стали называть «хорошим».
Для таких исследований заболевание искусственно воспроизводят (моделируют) на животных. К сожалению, используемые в настоящее время модельные организмы относятся к разным систематическим группам: млекопитающим, птицам, рыбам (Getz, Reardon, 2012), и имеют между собой очень отдаленное эволюционное и, соответственно, генетическое родство, что затрудняет понимание общих закономерностей адаптации обмена холестерола. Для решения поставленной задачи нужно изучать группы генетически близких организмов, но занимающих различные экологические ниши и имеющих в связи с этим разные показатели липидного обмена.

Подходящей моделью могут быть эндемичные близкородственные представители рогатковидных рыб озера Байкал (Cottoidei). Это группа рыб из 26 видов, которые произошли от небольшого количества исходных форм (Sideleva, 2003). Разные виды Cottoidei отличаются широким разнообразием, адаптированы к различным условиям обитания и пищевому рациону с разным уровнем риска развития атеросклероза. Важно, что по сравнению с другими водными бассейнами в озере Байкал минимально антропогенное загрязнение (Shimaraev et al., 2000), что позволяет исключить возможность связанного с ним искажения данных.
Разные виды – разные липиды
Для исследований были выбраны четыре вида рыб Cottoidei с разным типом питания и поведения: большая красная широколобка (Procottus major, Taliev, 1944), длиннокрылка (Cottocomephorus inermis, Yakovlev, 1890), плоская широколобка (Limnocottus bergianus, Taliev, 1935) и байкальская большеголовая широколобка (Batrachocottus baicalensis, Dybowski, 1874) (Sudakov et al., 2015). Уровень суммарного холестерола в крови рыб оказался специфичным для каждого вида. Самый низкий уровень холестерола, кстати, сопоставимый с таковым у человека (Flaim et al., 1981), наблюдался у длиннокрылки, обитающей в толще воды. У остальных трех видов, обитающих на дне, этот показатель был более высоким.
Еще сильнее различался фракционный состав холестерола. Самый высокий уровень антиатерогенного холестерола был у большой красной широколобки, а самый низкий – у длиннокрылки, но при этом у обоих этих видов содержание атерогенного холестерола было низким. Напротив, у плоской широколобки и байкальской большеголовой широколобки атерогенный холестерол был высоким. Другими словами, у большой красной широколобки «хороший» холестерол преобладает над «плохим», а у остальных трех видов – наоборот, «плохой» холестерол преобладает над «хорошим».


Интересно, что наблюдаемые различия липидных спектров крови рыб не являются следствием их особенностей питания. Это говорит о том, что уровни фракций холестерола крови этих близкородственных организмов жестко предопределены на генетическом уровне. Например, несмотря на то что плоская широколобка и большая красная широколобка питаются преимущественно амфиподами (ракообразными), их липидные спектры крови противоположны по соотношению атерогенной и антиатерогенной фракций холестерола. Поразительно, что к показателям питающейся в основном амфиподами плоской широколобки близок липидный спектр наиболее активного хищника семейства Cottoidei – байкальской большеголовой широколобки. Амфиподы составляют 70 % ее пищевого рациона, но оставшиеся 30 % – другие Cottoidei.
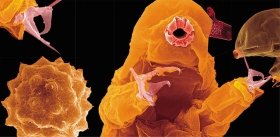
Кроме того, рыбы могут представлять интерес в связи с важной ролью их печени в запасании жиров (Henderson, Torcher 1987). Микроскопический анализ показал, что в ткани печени Cottoidei много клеток с крупными липидными каплями. Высокое содержание липидов в печени некоторых представителей рогатковидных рыб было обнаружено и биохимическими методами (Kozlova, 1998). Удивительно, но большой объем жировых капель в клетках печени рыб не сопровождается развитием нарушений обмена холестерола и атеросклерозом, что было бы невозможным у человека и других млекопитающих. Видимо, жировые капли – неотъемлемый компонент клеток печени Cottoidei, как и многих других рыб, а не патологические образования, как это бывает при избыточном накоплении жиров в печени млекопитающих (Takahashi et al., 2012).
Исследованные виды Cottoidei – это уникальный комплекс модельных организмов, на которых можно изучать генетические, физиологические и экологические механизмы устойчивости к развитию нарушений обмена холестерола и атеросклероза.
Несмотря на общность происхождения, представители видов имеют широкий диапазон значений уровня общего холестерола крови и его фракций, четко выраженные индивидуальные особенности липидного спектра крови. Исследуя механизмы, формирующие эти различия, мы приблизимся к пониманию закономерностей адаптации обмена холестерола и устойчивости к развитию атеросклероза, а особенности содержания жиров в печени рыб помогут понять механизмы устойчивости к негативным эффектам их избыточного накопления в печени.
Литература
Климов А. Н., Никульчева Н. Г. Обмен липидов и липопротеидов и его нарушения. 3-е изд., перераб. и доп. СПб.: Питер Ком, 1999. 512 с.
Getz G. S., Reardon C. A. Animal models of atherosclerosis // Arterioscler Thromb Vasc Biol. 2012. V. 32, N 5. P. 1104—1115.
Flaim E., Ferreri L. F., Thye F. W. et al. Plasma lipid and lipoprotein cholesterol concentrations in adult males consuming normal and high cholesterol diets under controlled conditions // Amer. J. Clin. Nutr. 1981. V. 34, N 6. P. 1103—1108.
Henderson R. J., Torcher D. R. The lipid composition and biochemistry of freshwater fish // Prog. Lipid Res. 1987. V. 26. P. 281—347.
Kozlova T. A. Lipid class composition of benthic-pelagic fishes (Cottocomephorus, Cottoidei) from Lake Baikal // Fish. Physiol. Biochem. 1998. V. 19, N 3. P. 211—216.
Martirosyan D. M., Miroshnichenko L. A., Kulokawa S. N. et al. Amaranth oil application for heart disease and hypertension // Lipids Health Dis. 2007. V. 6. Article 1. Published online.
Shimaraev M. N., Parfenova V. V., Kostornova T. Ya. et al. Exchange processes and distribution of microorganisms in the deep zone of Lake Baikal // Dokl. Biol. Sci. 2000. V. 372. P. 279—282.
Sideleva V. G. Endemic fishes of Lake Baikal. Backhuys Publishers. Leiden. Netherlands, 2003. P. 270.
Sudakov N. P., Klimenkov I. V., Pastukhov M.V. Lake Baikal Endemic Sculpins (Cottoidei): A Promising Model to Study Adaptive Plasticity of Blood Cholesterol Metabolism // Brazilian Arch. Biol. and Technol. 2015. V. 58, N 4. P. 613—616.
Takahashi Y., Soejima Y., Fukusato T. Animal models of nonalcoholic fatty liver disease/nonalcoholic steatohepatitis // World J Gastroenterol. 2012. V. 18. P. 2300—2308