Макрофаги, разрушающие амилоидные бляшки при болезни Альцгеймера, работают «по часам»
Болезнь Альцгеймера, приводящая к старческому слабоумию, поражает миллионы людей. Это нейродегенеративное заболевание характеризует накопление в мозге амилоидных бляшек из патологического белка. И недавно при исследовании работы иммунных клеток ученые обнаружили механизм усиления этого процесса
Решающим этапом в развитии болезни Альцгеймера сегодня считают накопление бета-амилоида в результате снижения способности мозга утилизировать этот патологический белок. С другой стороны, известно, что развитие болезни Альцгеймера связано с нарушением циркадных ритмов (биологических часов) организма, включая нарушения сна, которые могут происходить за годы до проявления симптомов заболевания.
Установлено, что у здоровых людей содержание бета-амилоида в спинномозговой жидкости в течение суток колеблется, однако у пациентов с болезнью Альцгеймера этого не наблюдается. При этом молекулярный механизм, лежащий в основе взаимосвязи циркадных ритмов и этой мозговой патологии, до сих пор не изучен.
На молекулярном уровне работой внутренних «биологических часов» управляют несколько особых белков, которые вызывают циклические колебания множества биологических процессов с периодом около суток. Закономерности, связанные с такими колебаниями, сегодня служат предметом интенсивного изучения
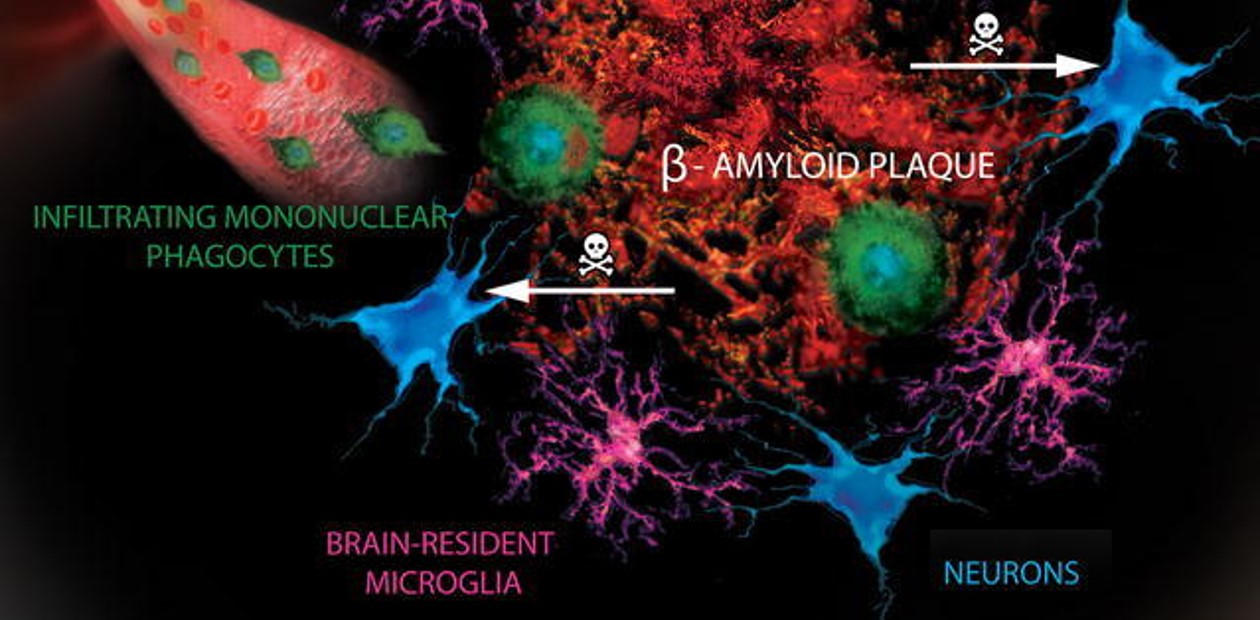
Известно, что важную роль в патогенезе болезни Альцгеймера играют иммунные клетки макрофаги («пожиратели»). На ранних этапах развития болезни эту роль выполняют клетки микроглии – тканевые макрофаги, базирующиеся исключительно в головном мозге. Одна из функций этих клеток – служить «мусорщиками»; в частности, они уничтожают бета-амилоид, поглощая его в процессе фагоцитоза.
На более поздних этапах болезни, когда нейровоспаление усиливается, на помощь микроглии в мозг начинают мигрировать и макрофаги периферической крови. Однако процесс накопления амилоидных бляшек не останавливается.
Ранее ученые из Политехнического института Ренсселера (США) выяснили, какие молекулы РНК и клеточных белков макрофагов подчиняются циркадным ритмам. Среди них оказались ферменты, участвующие в биосинтезе двух сложных белков протеогликанов – гепарансульфата и хондроитинсульфата, располагающихся на поверхности клеток. И недавно исследователи проверили гипотезу, что именно эти молекулы являются связующим звеном между циркадной системой и болезнью Альцгеймера.
В серии экспериментов с использованием клеточной культуры макрофагов, полученных из костного мозга лабораторных мышей, ученые выяснили, что количество бета-амилоида, потребляемого макрофагами, колеблется в соответствии с суточным ритмом. Но если в этих иммунных клетках «отключить» ген per – один из главных циркадных генов, то эта закономерность пропадает.
Когда исследователи измерили суточные колебания уровней гепарансульфата и хондроитинсульфата на поверхности макрофагов с нормальным циркадным циклом, они обнаружили, что у макрофагов процессы поглощения бета-амилоида и продукции протеогликанов идут в противофазе. При этом полное удаление протеогликанов с поверхности этих иммунных клеток усиливает их фагоцитарную активность.
Эти результаты говорят о том, что поверхностные протеогликаны макрофагов подавляют фагоцитоз патологического амилоидного белка. По-видимому, они способствуют его агрегации и связыванию на поверхности клеток, что затрудняет поглощение и дальнейшую деградацию бета-амилоида уже внутри клетки.
Можно предположить, что при отсутствии циркадного ритма, когда «внутренние часы» макрофагов «останавливаются» на фазе производства протеогликанов и их фагоцитирующая активность падает, удаление патологического амилоида замедляется, что способствует образованию амилоидных бляшек. Полученные данные можно будет использовать для разработки методов стимуляции внутренних механизмов избавления от бета-амилоида. Эти результаты также подтверждают важность здорового сна для ослабления симптомов болезни Альцгеймера.
Фото: https://www.maxpixel.net, https://commons.wikimedia.org