Новый кандидат на лекарство от болезни Альцгеймера
В 2016 г. американские исследователи объявили о первом успехе клинических испытаний очередного потенциального лекарства от болезни Альцгеймера – одной из самых частых причин старческого слабоумия. Если новый препарат на основе моноклональных антител к патологическому пептиду бета-амилоиду докажет свою эффективность, это не только даст надежду многим тысячам больных, но и подтвердит справедливость амилоидной теории возникновения этого тяжелейшего нейродегенеративного заболевания
Положительные результаты первых клинических испытаний нового препарата адуканумаба (Aducanumab) – это хорошая новость для ученых, рассматривающих образование так называемых амилоидных бляшек (отложений белка – амилоида) как одну из основных причин развития болезни Альцгеймера. Важно, что на фоне приема препарата наряду с уменьшением размера амилоидных бляшек в тканях мозга больных замедляется и темп снижения когнитивных способностей.
Амилоидная гипотеза развития болезни Альцгеймера была предложена еще четверть века назад, но до сих пор существуют и другие объяснения патогенеза этой болезни, которые отрицают значение амилоидных фибрилл в ее развитии. Есть даже предположение, что само образование амилоидных бляшек вторично и направлено на то, чтобы понизить содержание в мозге токсичной растворимой формы амилоидного белка. Поэтому доказательства эффективности адуканумаба могут послужить прямым доказательством связи между болезнью и появлением амилоидных бляшек.
Молекулы некоторых белков, в норме имеющих глобулярную (сферическую) форму, могут разворачиваться и слипаться в длинные амилоидныe фибриллы. Бляшки, образующиеся из таких фибрилл, могут негативно влиять на процессы жизнедеятельности живой клетки и стать причиной развития многих практически не поддающихся лечению заболеванийПока опубликованы только предварительные данные первых клинических испытаний, полученные на относительно небольшой выборке из 165 больных, которые принимали препарат в течение года. Чтобы сделать окончательный вывод, необходимо набраться терпения, пока не будут получены результаты более массовых тестов. Как известно, низкую эффективность аналогичных препаратов на основе антител к амилоидным белкам – соланезумаба (Solanezumab) и бапинейзумаба (Bapineuzumab) – удалось выявить лишь на третьей фазе клинических испытаний, которые были проведены в 2014 г. Тогда казалось, что эта неудача закроет целое направление в поиске лекарственных препаратов против болезни Альцгеймера. К счастью, этого не случилось.
В случае успеха дальнейшего тестирования адуканумаба, который подтвердит ключевую роль амилоидных фибрилл в прогрессировании болезни Альцгеймера, дополнительный импульс могут получить не только работы по поиску специфических антител против бета-амилоида, но и разработки низкомолекулярных ингибиторов процесса формирования амилоидной формы этого пептида. Такие низкомолекулярные соединения могут иметь преимущества по сравнению с антителами, так как они дешевле в производстве, обладают более высокой проникающей способностью и способны действовать в мозгу на самой ранней стадии формирования фибрилл, когда их еще не могут распознать антитела. Лекарства на основе этих соединений можно начинать принимать до появления клинических проявлений болезни. В связи с ростом продолжительности жизни, а с возрастом – ростом вероятности болезни Альцгеймера, актуальность таких профилактических препаратов не вызывает сомнений.
Еще один путь атаки на болезнь Альцгеймера связан с использованием низкомолекулярных ингибиторов фермента BACE 1, который «отрезает» пептиды, образующие впоследствии амилоидные фибриллы, от белка-предшественника. Такие препараты уже проходят разные фазы испытаний, в том числе на людях. Правда, пока неясно, будут ли они вызывать серьезные побочные эффекты при длительном приеме, так как этот фермент может играть важную роль в организме человека, о которой мы пока не знаем.
Антитела «конструируются» самой природой благодаря естественным механизмам адаптивного иммунитета, а соединения-ингибиторы должны быть спроектированы учеными. Для этого необходимо хорошо понимать, как образуются и как именно устроены амилоидные фибриллы. Изучение строения и формирования таких патологических структур – одна из задач лаборатории структурной биоинформатики и молекулярного моделирования Новосибирского государственного университета, и мы надеемся, что в сотрудничестве с другими учеными Новосибирского научного центра сможем внести серьезный вклад в разработку новых лекарственных препаратов против болезней, в развитии которых участвуют амилоидные фибриллы.
Так, специалисты Новосибирского института органической химии им. Н. Н. Ворожцова СО РАН уже разработали препарат на основе природного вещества из сосновой смолы, который устраняет симптомы болезни Паркинсона у лабораторных мышей. Ведь болезнь Альцгеймера, хотя и самая известная из «амилоидных» патологий, но далеко не единственная. Болезнь Паркинсона, деменция с тельцами Леви, болезнь Хантингтона, диабет II типа, губчатая энцефалопатия, некоторые редкие наследственные заболевания также сопровождаются образованием амилоидных фибрилл в различных тканях. И это наверняка только вершина айсберга…
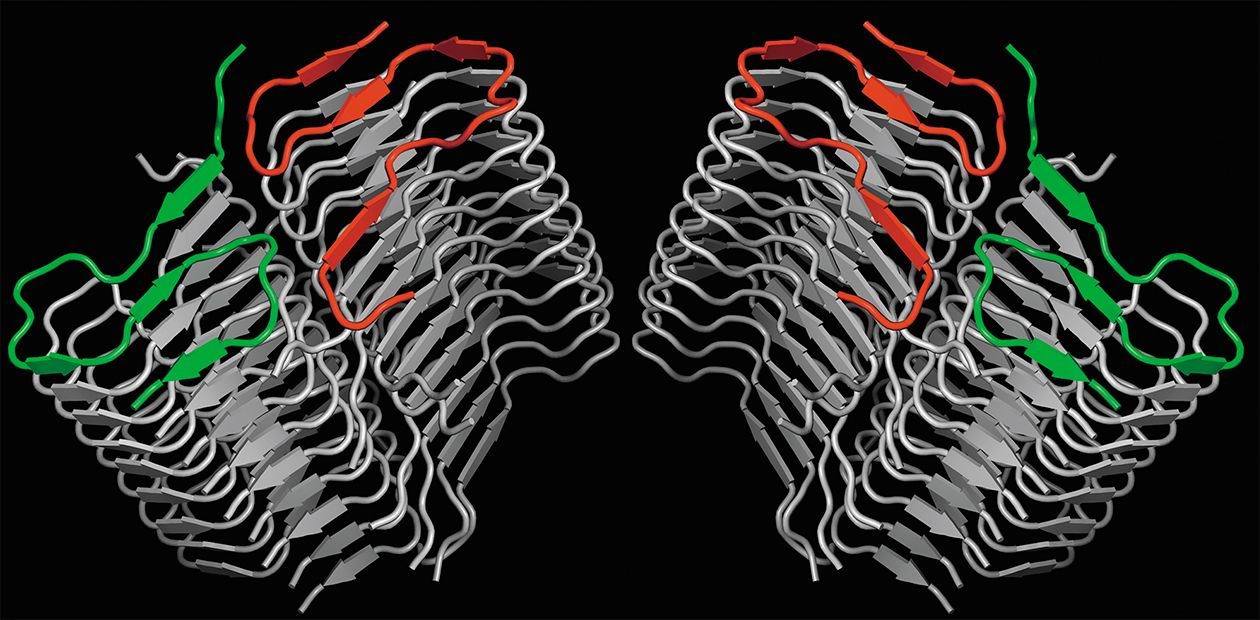
На слайдере: фибрилла (вверху), образованная амилоидным пептидом Aβ42. Красным и зеленым цветом окрашены два верхних пептида в стопке, состоящей из таких же пептидов. Нельзя утверждать, что структура фибриллы, полученной с помощью методов математического моделирования, полностью совпадает со структурой фибриллы в мозгу больного Альцгеймером, но общие принципы организации и состав совпадают. Фото модели предоставлено к.б.н. А. Ю. Бакулиной (НГУ, Новосибирск)
Литература
Vassar R. BACE1 inhibitor drugs in clinical trials for Alzheimer’s disease // Alzheimers Res Ther. 2014. V. 6(9). 89 p.
Ow S. Y., Dunstan D. E. A brief overview of amyloids and Alzheimer’s disease // Protein Sci. 2014. V. 23(10). P. 1315–1331.
Salloway S, Sperling R, Fox NC et al. Two phase 3 trials of bapineuzumab in mild-to-moderate Alzheimer’s disease // The new England Journal of Medicine. 2014. V. 370(4). P. 322–333.
Thompson D. 2 Alzheimer’s Drugs Found Ineffective in Clinical Trials. 2014. https://consumer.healthday.com/cognitive-health-information-26/alzheimer-s-news-20/2-alzheimer-s-drugs-found-ineffective-in-clinical-trials-684115.html