Такие разные радикалы
«Радикалом» (от radix – корень) в обыденном русском языке чаще всего называют сторонника крайних и решительных мер. В органической химии этот термин вначале использовался для обозначения «коренной» части молекулы, не изменяющейся в химических реакциях. Однако позже «свободным радикалом» стали называть молекулу с «оборванной» химической связью, обладающей, напротив, высокой реакционной способностью и вследствие этого крайне неустойчивой. Однако имеются радикалы особого «сорта» – так называемые стабильные радикалы, которые могут существовать сколь угодно продолжительное время, и не только в эфемерных концентрациях, но даже как индивидуальные вещества!
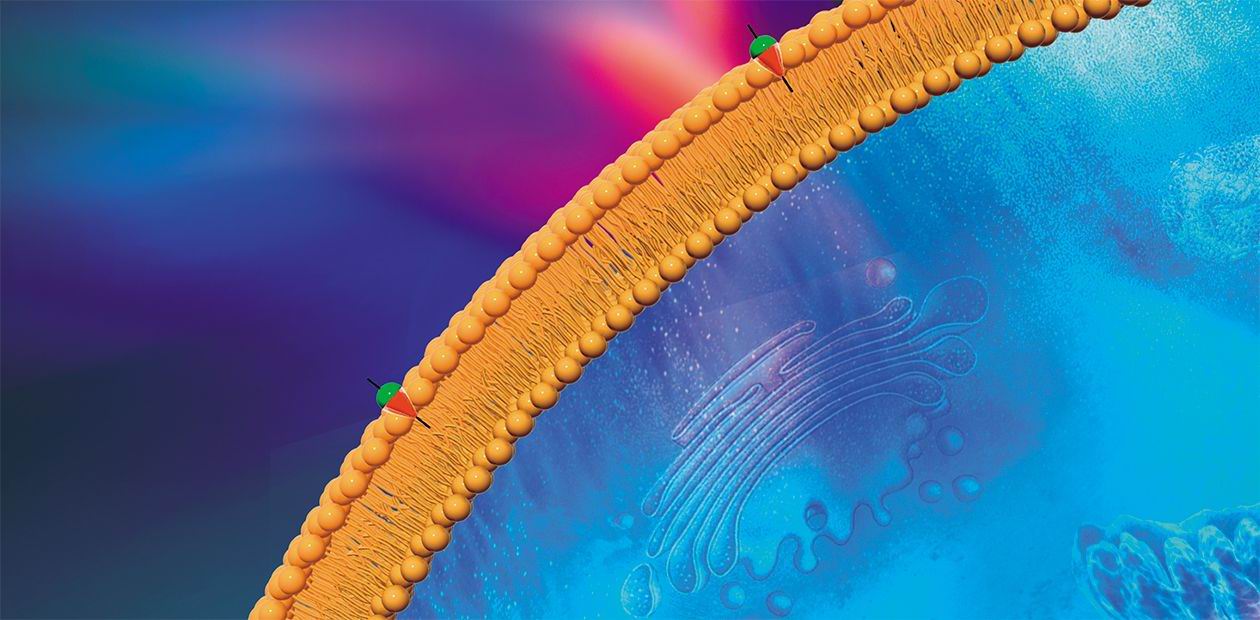
Вторая половина XX в. характеризуется фантастическим всплеском интереса научной общественности к стабильным нитроксильным радикалам – органическим молекулам, в состав которой входит нитроксильная группа N–O, на которой и локализован неспаренный электрон. Синтез новых НР и изучение их химических свойств не является самоцелью: эти соединения используются при решении различные задачи с применением спектроскопии электронного парамагнитного резонанса (ЭПР). Метод спиновых меток и зондов сегодня широко применяется в самых разных областях химии, биологии и медицины, являясь поистине универсальным исследовательским инструментом
There are more things in heaven and earth, Horatio,
Than are dreamt of in your philosophy
W. Shakespeare, Hamlet
Термином «радикал» (от латинского radix – корень) в обыденном русском языке чаще всего называют человека, сторонника крайних и решительных мер. В органической химии этот термин вначале использовался для обозначения «коренной» части молекулы, не изменяющейся в химических реакциях, т. е. как символ чего-то консервативного и незыблемого. В той же химии затем появился термин «свободный радикал», указывающий, напротив, на склонность частицы вступать в различные химические взаимодействия, характеризуя его крайнюю неустойчивость.
Какую же сущность скрывает в себе еще более удивительное грамматическое сочетание – стабильный радикал?
Что представляет собой частица вещества (молекула, атом), которую называют радикалом? Обычно у молекул все электроны, которые образуют межатомные связи, равно как и собственные электроны каждого атома существуют парами (поскольку это наиболее энергетически выгодное состояние молекулы). Но если по каким-то причинам получилась частица с нечетным числом электронов, то один из электронов в ней неспаренный – и она является радикалом. Бывают и молекулы-бирадикалы с четным числом неспаренных электронов, которые находятся на разных молекулярных орбиталях.
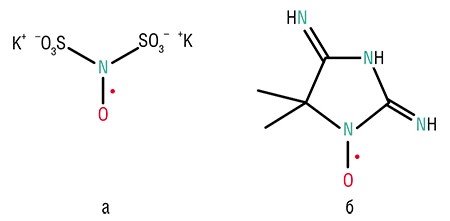 Молекулы с такой электронной конфигурацией обладают очень высокой химической активностью, направленной на «ликвидацию нечетности» путем взаимодействия с другим радикалом (это процесс рекомбинации). Но из-за очень малой концентрации радикалов такая ситуация реализуется сравнительно редко; чаще они взаимодействуют с «первой встречной» молекулой независимо от того, радикальна она или нет. Однако при взаимодействии с нерадикальной молекулой нечетность системы сохраняется. Иначе говоря, из одного радикала после такого взаимодействия возникает другой. Этот последний, как правило, менее активен, чем исходный, однако в любом случае радикальность не исчезает, а лишь меняет свой характер, вследствие чего одна возникшая в системе радикальная частица способна породить целый каскад реакций с участием различных радикалов – так называемый цепной радикальный процесс. Примером является горение, в котором инициатором цепи реакций окисления может выступать молекула кислорода, которая как раз является бирадикалом – в отличие, например, от молекулы азота (даже неискушенному в химии известно, что химическая активность этих двух простых веществ очень сильно отличается).
Молекулы с такой электронной конфигурацией обладают очень высокой химической активностью, направленной на «ликвидацию нечетности» путем взаимодействия с другим радикалом (это процесс рекомбинации). Но из-за очень малой концентрации радикалов такая ситуация реализуется сравнительно редко; чаще они взаимодействуют с «первой встречной» молекулой независимо от того, радикальна она или нет. Однако при взаимодействии с нерадикальной молекулой нечетность системы сохраняется. Иначе говоря, из одного радикала после такого взаимодействия возникает другой. Этот последний, как правило, менее активен, чем исходный, однако в любом случае радикальность не исчезает, а лишь меняет свой характер, вследствие чего одна возникшая в системе радикальная частица способна породить целый каскад реакций с участием различных радикалов – так называемый цепной радикальный процесс. Примером является горение, в котором инициатором цепи реакций окисления может выступать молекула кислорода, которая как раз является бирадикалом – в отличие, например, от молекулы азота (даже неискушенному в химии известно, что химическая активность этих двух простых веществ очень сильно отличается).
Однако есть радикалы и несколько иного сорта, которые, несмотря на наличие неспаренного электрона, могут существовать сколь угодно продолжительное время, причем не только в эфемерных концентрациях, но даже как индивидуальные вещества! В-общем, речь пойдет о так называемых стабильных радикалах.
«Ничейный» электрон
Первым известным человеку стабильным радикалом стала так называемая соль Фреми, открытая в середине XIX в. Но в то время даже мысль о том, что эта молекула является свободным радикалом, возникнуть не могла. В современном смысле этот термин стали использовать только после открытия американского химика-органика М. Гомберга (1900 г.). Он пытался синтезировать молекулу углеводорода – гексафенилэтана, но получил неизвестное соединение, структура которого была установлена лишь спустя 68 лет.
Синтезированное Гомбергом вещество обладало странными свойствами: будучи бесцветным, образовывало растворы желтого цвета и при этом очень легко реагировало с кислородом воздуха. При испарении растворителя без доступа воздуха вновь образовывался исходный бесцветный углеводород. Гомберг справедливо предположил, что полученное им соединение в растворе обратимо диссоциирует – распадается на два трифенилметильных радикала. Это было очень смелое предположение для того времени, и хотя трифенилметильный радикал мог существовать только в растворе и при отсутствии кислорода, он стал первым стабильным радикалом *.
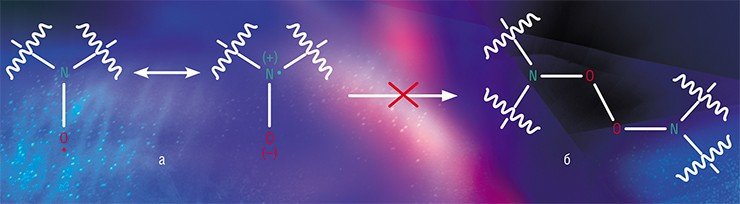
«Слуга» двух «господ»Поразительная стабильность этого типа радикалов обусловлена тем, что его рекомбинация энергетически невыгодна, так как при этом образуется цепочка из четырех неуглеродных атомов (N–O–O–N), которая крайне неустойчива. Кроме того, устойчивость радикала значительно выше, когда нитроксильная группа находится в тетраалкильном окружении, которое препятствует реализации других путей гибели
Причиной стабильности трифенилметильного радикала Гомберг не без основания считал тот факт, что -неспаренный электрон в этом случае не был локализован на центральном атоме углерода, а в значительной мере распределен по ароматическим кольцам.
Примерно в то же время был получен другой стабильный органический радикал порфироксид, содержащий нитроксильную группу NO (Пилоти и Шверин, 1901). Он был настолько стабильным, что, в ряде реакций с участием других своих функциональных групп, его радикальный центр оставался без изменений. Неудивительно, что даже сами создатели порфироксида не могли предположить, что имеют дело с первым стабильным нитроксильным радикалом (НР). Несколько позже синтезом подобных «азот-окисных» стабильных радикалов занимался Нобелевский лауреат Г. Виланд.
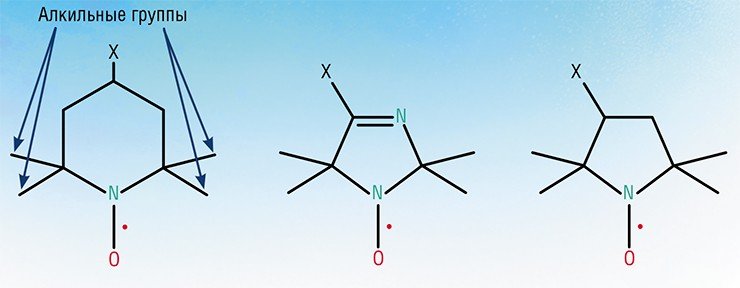
Вторая половина XX в. характеризуется фантастическим всплеском интереса научной общественности к нитроксильным радикалам. Начало «новой эры» было положено советскими химиками О. Л. Лебедевым и С. Н. Казарновским, наблюдавшими очень стабильный радикал, который мог существовать в растворе сколь угодно долго без всяких предосторожностей. Однако их статью, опубликованную в 1959 г. в малоизвестном региональном журнале, международная общественность просто не заметила.
В 1998 г. за выявление роли этой молекулы (которая, кстати, сама является простейшим нитроксильным радикалом) группа американских ученых была удостоена Нобелевской премии в области физиологии и медицины. «Злые языки» утверждали, что премия была присуждена за создание широко известного препарата под названием «Виагра», принцип действия которого как раз и заключается в регулировании концентрации оксида азота. Действительно, сначала планировалась разработка именно кардиостимулирующего средства, а впоследствии обнаружился широко известный ныне «побочный эффект», также связанный с обменом NO в организме
Бурное развитие химии НР в нашей стране и во всем мире началось благодаря работам московского химика Э. Г. Розанцева и его коллег, удостоенных Государственной премии СССР в 1977 г. Они не только смогли выделить ряд суперстабильных радикалов, но и научились получать их в больших количествах. Было установлено, что протекание многих химических реакций с подобными радикалами без участия радикального центра (неспаренного электрона) – явление достаточно общее. В последующие годы в нашей и других странах сформировались мощные научные школы химиков-органиков, разрабатывающие методы синтеза стабильных радикалов этого типа.
Чем же так интересны оказались эти экзотические соединения? Ведь необычность или красота молекулярной структуры сама по себе вовсе не повод для многих сотен публикаций, которые продолжают выходить ежегодно на протяжении многих десятилетий.
Дело в том, что НР оказались в прямом смысле слова счастливой находкой.
Счастливая находка
Значимость нитроксильных радикалов во многом определяется тем, что они оказались исключительно полезным инструментом для научных исследований в целом ряде областей научного знания.
Как известно, помимо заряда электрон имеет еще и магнитную характеристику – спин. Поэтому отличительной особенностью НР является парамагнетизм – способность намагничиваться в направлении, совпадающем с направлением внешнего магнитного поля.
В магнитном поле спиновые состояния электрона в молекуле НР оказываются энергетически неэквивалентными – эта разница в энергетических состояниях и будет определять величину энергии, которое парамагнитное вещество будет поглощать в определенных условиях. Фиксируя интенсивность поглощения энергии в зависимости от мощности поля, мы получаем спектр электронного парамагнитного резонанса (ЭПР).
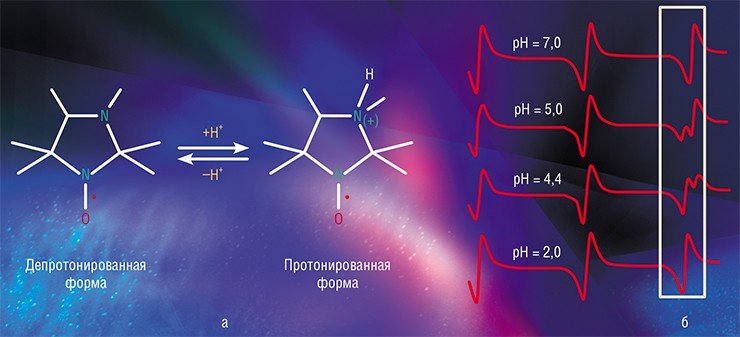
Вид спектра ЭПР зависит от того, на каких магнитоактивных ядрах происходит локализация спиновой плотности, то есть где расположен неспаренный электрон. В нитроксильной группе таким свойством обладает ядро атома азота 14N, в этом случае типичный спектр представляет собой триплет (три линии на равном расстоянии друг от друга, называемом константой сверхтонкого взаимодействия).
Чувствительность ЭПР позволяет обнаруживать радикалы в растворе даже в очень малой (порядка 10–10 моль/л) концентрации. Но какую информацию может получить исследователь из такого спектра, кроме факта наличия самих радикалов? Оказывается, очень значимую, поскольку ближайшее окружение нитроксильной группы (причем не только в молекуле НР, но и в соседних молекулах) оказывает существенное влияние на сверхтонкую структуру спектра. Именно эта особенность стабильных НР позволяет исследователю получать разнообразные характеристики изучаемых объектов.
В связи с вышесказанным, синтез новых НР и изучение их химических свойств сегодня не является самоцелью: создаваемые новые структуры НР призваны решать различные задачи с применением спектроскопии ЭПР. Такой подход получил название метода спиновых меток и зондов. Сегодня этот метод широко применяется в самых разных областях химии, биологии и медицины, являясь поистине универсальным исследовательским инструментом.
Универсальный инструмент
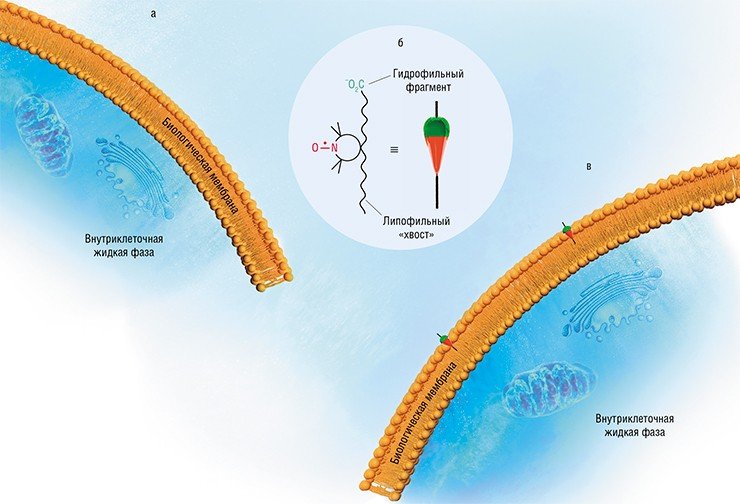
Метод спиновых меток оказался очень удобным для изучения структуры активного центра ферментов. Как известно, организм борется с поступающими в него из окружающей среды токсическими веществами, окисляя их и переводя в водорастворимую форму для последующего выведения. Для этих целей используются, в частности, ферменты группы Р-450. Для их исследования были специально синтезированы молекулы НР, которые фермент способен распознавать как ксенобиотик и избирательно захватывать его для «переработки». В результате молекулы НР адресно доставляются в активный центр фермента, после чего спектроскопическое изучение позволяет судить о геометрии и топологии последнего в динамике.
Интересен оказался «побочный» эффект подобного зонда: при захвате НР одна из его функциональных групп ковалентно связывается с тиольной группой фермента, который после этого довольно долго не может избавиться от «лже-субстрата». А теперь представим, что произойдет, если мы аналогичным образом заблокируем работу фермента, который, к примеру, окисляет в организме насекомого инсектицид, использующийся в качестве оружия против этого насекомого? Как результат, можно будет заметно уменьшить дозу отравляющего вещества без потери эффективности.
Применяя серосодержащие НР, можно измерить суммарную концентрацию в крови аминокислот и пептидов, содержащих тиольную группу, отклонения которой от нормы зачастую свидетельствуют о развитии в организме ряда патологий. Радикал количественно вступает в необратимую реакцию обмена с образованием другого радикала, поэтому величина парамагнитного сигнала от продукта реакции определяет искомую концентрацию. Аналогичным методом в растворе измеряют концентрации ионов металлов, образующих с НР комплексные соединения.
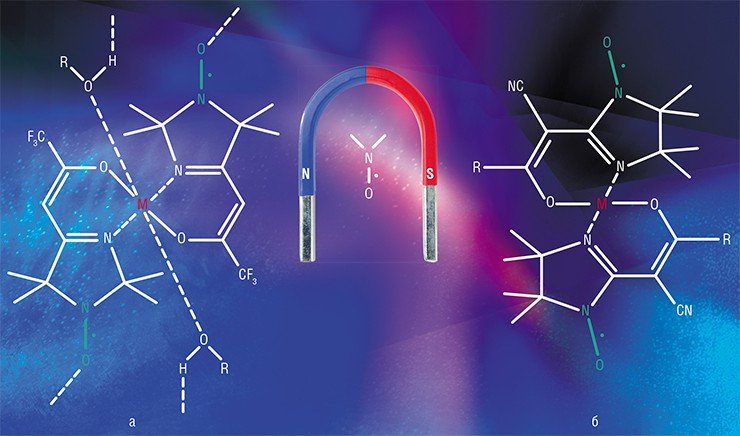
Кстати сказать, использование НР в качестве парамагнитных лигандов комплексных солей привело к еще одному очень важному результату: были синтезированы координационные соединения с ионами металлов, обладающие макромолекулярным магнетизмом. Эти соединения являются диэлектриками (по причине отсутствия свободных электронов), однако способны намагничиваться подобно металлам группы железа. Такие материалы получили название молекулярные магнетики.
На использовании НР базируется и один из наиболее чувствительных методов обнаружения супероксид анион-радикала O2– – одной из самых активных форм кислорода, циркулирующих в нашем организме. Эта частица обладает очень высокой реакционной способностью, вследствие чего и время ее жизни, и ее стационарная концентрация очень малы. Для ее исследования в объект вводят не сам нитроксильный радикал, а его предшественник, который исключительно быстро и легко взаимодействует с супероксид анион-радикалом с образованием стабильного радикала, концентрацию которого опять же легко измерить с применением спектроскопии ЭПР.
Реакционно дееспособен!
В молекуле стабильного НР парамагнитный центр (нитроксильная группа) во многих реакциях сохраняется неизменным. Тем не менее, он обладает реакционной способностью, просто при разработке стратегии синтеза НР этот факт учитывается. Однако придуманы и такие сценарии использования радикалов, в которых запланирована «гибель» нитроксильной группы, приводящая к полезным результатам.
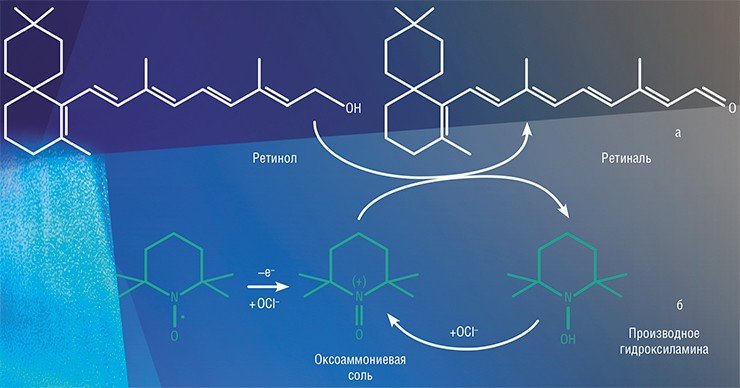
В таком качестве НР используют в тонком органическом синтезе. Например, альдегиды могут быть получены окислением спиртов. Однако образующийся альдегид подвержен дальнейшему окислению, и остановить реакцию на стадии его образовании не всегда удается. И здесь на помощь приходят нитроксильные радикалы. Так, для реакции окисления ретинола в ретиналь (всем известный витамин А) разработана схема, в которой продукт окисления НР выступает в роли катализатора, тем самым «смягчая» действие окислителя. Ряд подобных процессов в настоящее время уже внедрен в промышленную практику.
Нитроксильная группа легко взаимодействует с активными радикалами, например алкильными, с образованием неактивных молекул. Это позволяет использовать НР в качестве стабилизаторов, препятствующих протеканию свободно-радикальных цепных процессов. Таким образом нитроксильные радикалы можно заставить бороться с упомянутыми выше «не в меру активными» собратьями.
В русле реакционной способности радикального центра лежат и так называемые спиновые ловушки. Этот метод подразумевает использование веществ, которые при взаимодействии с активными радикалами образуют так называемые спиновые аддукты – продукты присоединения, обладающие значительно меньшей активностью. Поскольку большая часть нежелательных свободно-радикальных процессов протекает исключительно по цепному механизму, спиновая ловушка обрывает эти цепи, т.е. выступает в роли ингибитора процесса. С другой стороны, спиновые ловушки позволяют изучать кинетику образования и гибели активных радикалов, а в некоторых случаях даже их строение методами спектроскопии ЭПР.
Возникает законный вопрос: а что мешает непосредственному спектроскопическому изучению самих активных радикалов? Причина в еще одном атрибуте активных радикалов – очень короткое время жизни. Из-за этого концентрация таких радикалов в обычных условиях оказывается настолько мала, что их образование не удается зарегистрировать даже высокочувствительными методами ЭПР.
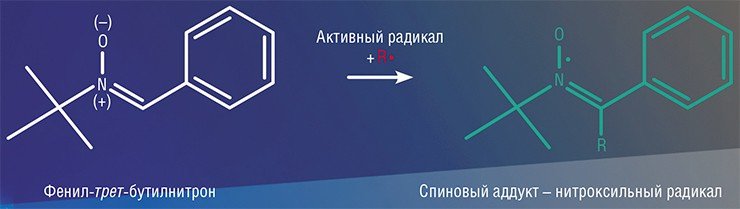
В этом отношении очень полезными оказались химические вещества, именуемые нитронами, которые достаточно легко взаимодействуют с активными радикалами с образованием спиновых аддуктов, являющихся, по сути, нитроксильными радикалами. Такие спиновые аддукты не всегда являются стабильными, но это и не важно: их активность, а значит, и время жизни несопоставимо больше, чем у исходных радикалов, и они легко могут быть обнаружены методами ЭПР.
В рамках сравнительно небольшой статьи практически невозможно рассмотреть все аспекты применения стабильных нитроксильных радикалов. Ведь возможности их применения практически безграничны – от изучения активных центров катализаторов до... интенсификации процесса нефтедобычи.
Известно, что нефть из скважины течет сама не всегда, очень часто приходится бурить дополнительные скважины и нагнетать туда воду. Вода поднимает давление в нефтеносном пласте – и нефть выходит наружу. А если вода вдруг начнет под землей смешиваться с нефтью, то нагнетательную скважину следует перекрыть и пробурить новую. Но если таких нагнетающих скважин несколько, как узнать, которую следует перекрыть?
Один из способов – «пометить» нагнетаемую воду. Сами нитроксильные радикалы для этой цели непригодны – недостаточно устойчивы. Но есть простые и устойчивые их предшественники – амины, которые и закачивают с водой под землю. Окисление аминогруппы в нитроксильную можно проводить непосредственно перед анализом в ампуле спектрометра ЭПР. Уже в конце 1980 гг., когда эта технология разрабатывалась, существовали простые и недорогие настольные спектрометры ЭПР, способные работать в полевых условиях. А амины тогда стоили существенно дешевле флуоресцентных красителей, которые используются для этой же цели.
Вторая причина, по которой невозможно «объять» все многообразие применения стабильных НР, проста: эти возможности на сегодня далеко не исчерпаны. Химики постоянно синтезируют новые НР, максимально приспособленные под решение конкретных задач. При этом часто оказывается, что возможности новых структур намного превосходят исходное «техзадание». Так возникают новые области применения, и конца этому процессу пока не видно.
Нужно заметить, что некогда в научной среде СССР обсуждались два принципиально разных подхода к решению научных задач. Первый формулировался как системный, и смысл его заключался в том, что исследователь ставил перед собой совершенно конкретную цель. Например, повысить «фуражность крупного рогатого скота» или «яйценоскость кур-несушек». Соответственно, все результаты, не ведущие к достижению этой цели, отбрасывались, как не имеющие ценности.
Второй подход мягко называли романтическим: исследователь в этом случае не имел четко сформулированной цели. Любой полученный результат заслуживал внимания, и в зависимости от своих научных пристрастий исследователь либо отбрасывал его, либо, напротив, тратил все силы на его понимание и дальнейшее изучение.
Сторонники первого подхода говорили, что их оппоненты «занимаются удовлетворением собственного любопытства за счет государства», а апологеты второго подхода утверждали, что самый интересный результат (не применительно к решению первоначально определенной задачи, а с гносеологической точки зрения) запланировать невозможно. Более того, кто может решить – является ли поставленная цель столь уж значимой, чтобы тратить ресурсы на ее достижение?
Кто из них был прав – этот вопрос сейчас, в эпоху «инновационного пути развития общества» кажется бессмысленным. Но все же история исследования стабильных нитроксильных радикалов свидетельствует, что без определенной доли романтичности, когда не исследователь ведет исследование, а «исследование – исследователя», многие научные результаты, определяющие стратегию развития целых научных направлений, возникнуть просто не могли.
Литература
Nitroxides: Applications in Chemistry, Biomedicine, and Materials Science / Edition 1 by Gertz Likhtenshtein, Jun Yamauchi, Shin’ichi Nakatsuji, Alex I. Smirnov, Rui Tamura. Wiley, John & Sons, Inc., 2008. 438 p.
Stable Radicals: Fundamentals and Applied Aspects of Odd-Electron Compounds / Ed. R. Hicks. Wiley, John & Sons, Inc., 2010. 606 p.
* Подробнее о тритильных радикалах – в статье В. М. Тормышева на с. 26—33.