Бета-клетки поджелудочной железы «из материала заказчика» – путь к безинсулиновой терапии
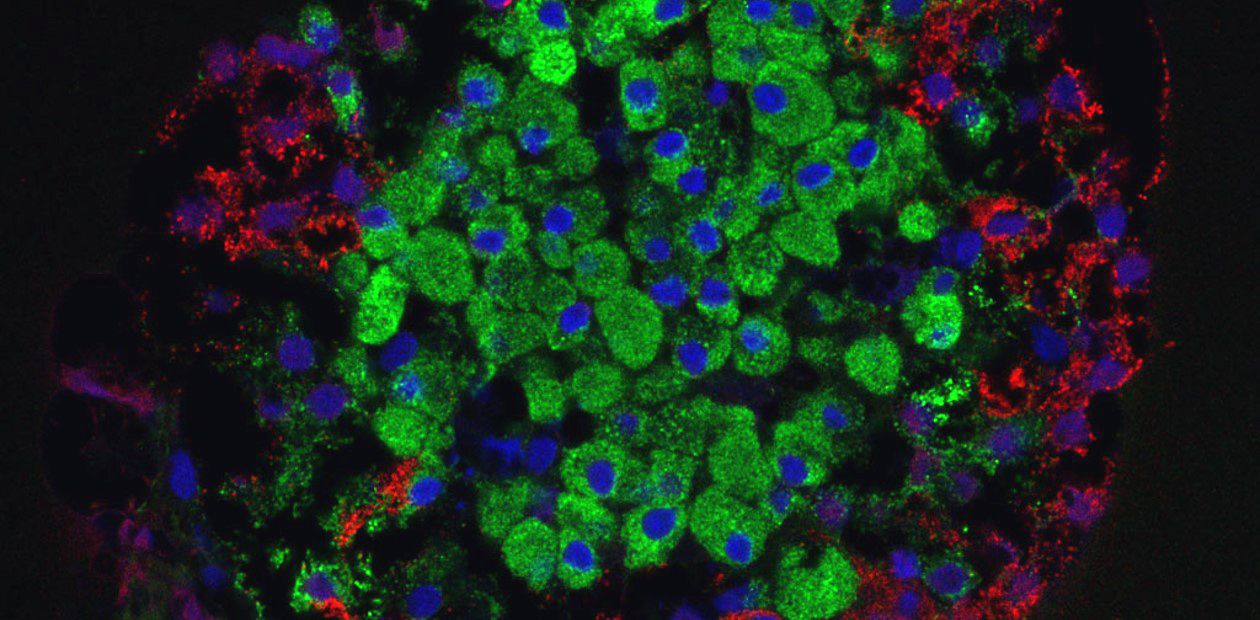
Сахарный диабет 1-го типа развивается в результате поражения бета-клеток поджелудочной железы, вырабатывающих инсулин. Недостаток инсулина, отвечающего за перенос глюкозы внутрь клеток, является причиной повышения уровня глюкозы в кровотоке. Практически единственный способ терапии этого заболевания – пожизненное введение инсулина – не гарантирует отсутствия осложнений, а иногда и вызывает их.
Во всем мире ведутся поиски альтернативных способов лечения этого аутоиммунного заболевания: от совершенствования лекарственных форм препаратов инсулина до технологий пересадки донорских бета-клеток.
Однако перспектива реакции отторжения при трансплантации донорского органа или ткани требует последующего пожизненного подавления иммунной системы. Поэтому ученые работают над созданием бета-клеток из собственных клеток пациента.
Исследователи во главе с Мартином Фассенеггером (Martin Fussenegger) из Швейцарской высшей технической школы Цюриха воспроизвели in vitro естественный процесс созревания бета-клеток поджелудочной железы. Для этого они взяли клетки жировой ткани донора и репрограммировали их в индуцированные плюрипотентные стволовые клетки. Затем ввели в эти клетки плазмиды, содержащие сложные генно-инженерные конструкции, – фактически, искусственно созданную генетическую программу, реализация которой должна точно воссоздавать природную динамику ключевых биохимических факторов, направляющих созревание бета-клеток.
Центральное место в процессе созревания бета-клеток занимают факторы роста Ngn3, Pdx1 и MafA. Изменение концентрации каждой из этих молекул происходит в соответствии с определенной закономерностью – например, MafA появляется только на четвертый день, затем его концентрация резко возрастает и остается на высоком уровне. Изменения концентрации Ngn3 и Pdx1 подчинены еще более сложным «сценариям».
До сих пор ученые побуждали клетки созревать в определенные типы, в том числе в бета-клетки поджелудочной железы, путем механического добавления к ним необходимых химических соединений и сигнальных молекул – с помощью пипетки.
Эффективность такого способа составляет около 25%: очень трудно добавлять правильные количества всех субстанций в нужное время с соблюдением всех динамических параметров, а клетка очень чувствительна к малейшим отклонениям от природной программы.
С помощью новой технологии удалось успешно трансформировать 75% клеток, которые так же, как «настоящие» бета-клетки, в присутствии глюкозы производят инсулин – хотя и в меньшем количестве.
Главной проблемой клинического применения таких клеток является проблема безопасности. Из-за риска развития опухоли во многих странах запрещено использование в медицинской практике индуцированных плюрипотентных стволовых клеток; запрещено и использование вирусных векторов, необходимых для перепрограммирования клеток, – из-за опасности возникновения рекомбинантных вирусов, способных размножаться.
Однако по мнению ученых, использование искусственных генетических программ снижает риски. В любом случае эта работа – еще один шаг к успеху развития клеточных технологий и регенеративной медицины в целом.
Фото: https://commons.wikimedia.org
Подготовила Мария Перепечаева