Новые надежды в онкологии: маленькие ингибиторы больших проблем
Раковые клетки убить достаточно просто, но сама опухоль может возрождаться даже после самого жесткого лечения, рикошетом поражающего здоровые клетки и ткани. «Благоприобретенная» лекарственная устойчивость и метастазирование – вот главные причины, от которых сегодня умирает практически каждый шестой человек. Но надежды не потеряны: автор статьи в новом выпуске журнала «НАУКА из первых рук» – известный американский специалист в создании противоопухолевых лекарств и первооткрыватель гена множественной лекарственной устойчивости И. Б. Ронинсон и его команда обнаружили универсальный механизм, позволяющий злокачественной опухоли выживать в стрессовых условиях. Химические ингибиторы этого процесса созданы и уже проходят клинические испытания
Проблем в борьбе с раком много. Опухолевые клетки – это не инфекционные агенты с чуждым метаболизмом, а все те же клетки организма, только «сбившиеся с пути». Поэтому радио- и химиотерапия, направленные на молекулярные мишени (например, на ДНК), необходимые для поддержания нормального клеточного цикла, будут неизбежно затрагивать и здоровые клетки. Более безопасны для пациента целевые (таргетные) препараты, действующие исключительно на клеточные мишени определенных видов опухолей, но такое лечение требует персонализированного подхода.
И самое главное – практически у всех пациентов, которых лечат любыми таргетными препаратами, и у большинства больных, подвергнутых традиционной химиотерапии, развивается лекарственная устойчивость. Однако о механизме, лежащем в основе этого явления, до недавнего времени знали немного.
Все началось в 1990-х гг., когда команда профессора Ронинсона обнаружила в некоторых опухолевых клетках, поврежденных теми или иными лекарствами, активацию гена, кодирующего белок, который отвечает за формирование множественной лекарственной устойчивости. Позже выяснилось, что многие раковые клетки, не «убитые» в результате обработки большим количеством лекарств, входят в особое состояние – они начинают стареть и перестают делиться. Одновременно в этих «постаревших» клетках активируется множество «спящих» генов и начинают синтезироваться белки, которые могут воздействовать как на сами эти клетки, так и на соседние, помогая опухоли выживать, расти и метастазировать.
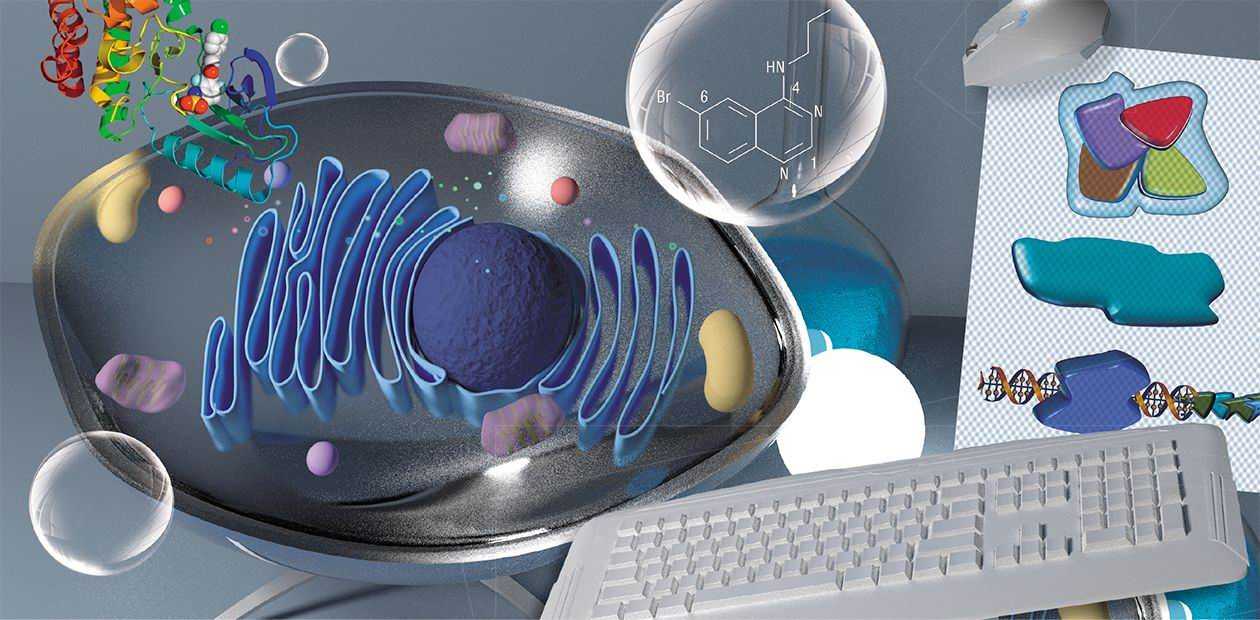
Так было открыто явление транскрипционного перепрограммирования раковых клеток в ответ на повреждение ДНК. Дело осталось «за малым»: понять, как воздействовать на ключевые элементы этого механизма. Применив систему высокопроизводительного скрининга, позволившую оценить более сотни тысяч различных химических соединений, команде Игоря Ронинсона удалось найти некие молекулы, подавляющие перепрограммирование опухолевых клеток. А затем были обнаружены и сами «герои» транскрипционного перепрограммирования раковых клеток – белки CDK8 (циклин-зависимая киназа 8) и родственный ему CDK19. Эти ферменты и стали мишенями для потенциальных лекарств.
В результате отбора и химической модификации исследователи получили для этих ферментов очень селективные ингибиторы, представляющие собой небольшие молекулы, которые достаточно просто синтезировать. Эти ингибиторы в комбинации с уже известными противоопухолевыми лекарствами практически во всех случаях рака предотвращали либо, в крайнем случае, замедляли возникновение лекарственной устойчивости. Они работали и самостоятельно при некоторых видах рака, в том числе редких (например, при острой миелоидной лейкемии). Последнее обстоятельство благодаря существующему в США законодательству о редких формах рака поможет ускорить процедуру одобрения препарата для использования в практической медицине.
Созданием CDK8/19-ингибиторов занимается основанная Игорем Ронинсоном американская компания Senex в тесном сотрудничестве с российской компанией «Биокад» (Санкт-Петербург). «Биокад» уже провел клинические испытания с первым лекарством-кандидатом, которое было разработано совместно с российскими учеными, и вскоре планируются клинические испытания его улучшенной версии. Применение подобных препаратов не будет означать отмену обычной противораковой терапии, но оно сможет многократно повысить ее эффективность.
Подробнее об ингибиторах транскрипционного перепрограммирования опухолевых клеток читайте в журнале «НАУКА из первых рук», 2019, № 3(83)