«Живые электроды» – безопасный посредник между мозгом и компьютером
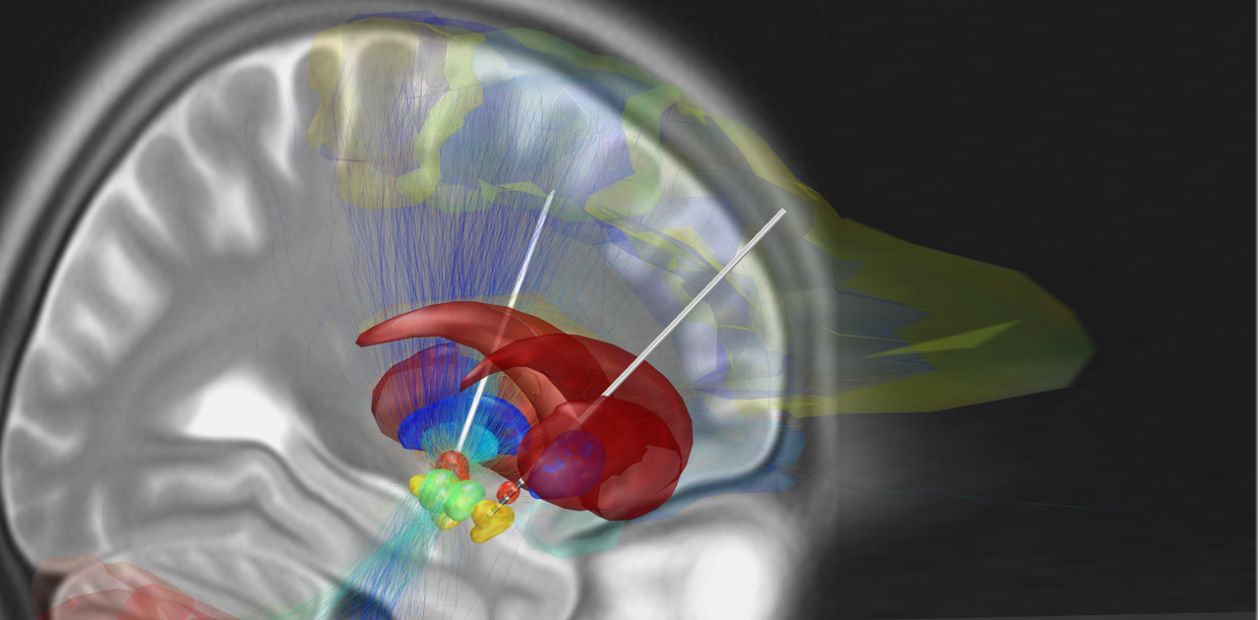
Для помощи людям с патологиями головного мозга уже сейчас довольно активно используются так называемые нейроинтерфейсы – системы для обмена информацией между мозгом и электронным устройством. Ими являются, к примеру, интерфейс «мозг–компьютер», позволяющий парализованному человеку управлять «силой мысли» бионическими протезами, и глубокая стимуляция мозга для лечения болезни Паркинсона и эпилепсии. Однако практически все подобные технологии требуют вживления в мозг электродов или электронных чипов. Одна из серьезных проблем такого вторжения – воспалительная реакция тканей, в результате которой прохождение электрического сигнала очень затрудняется. До сих пор ученым не удавалось создать материал для электродов, на который ткани мозга никак бы не реагировали.
Новая разработка исследователей из Пенсильванского университета (США) – «живые электроды» (официальное название micro-TENN – microtissue engineered neural networks). Эта конструкция содержит как небиологические компоненты (электронное устройство для управления активностью тех или иных участков мозга), так и живые нервные клетки (нейроны).
Неорганическая часть нейроинтерфейса с тканью мозга не соприкасается. В мозг же имплантируют нейроны вместе с их аксонами – длинными отростками, которые в организме играют роль «проводов», проводящих нервный импульс. Эти нейроны выращивают внутри микротрубочек толщиной с человеческий волос, заполненных гидрогелем специального состава. Так как в длину аксоны могут достигать нескольких сантиметров, этого достаточно, чтобы получить доступ к глубоко расположенным участкам мозга.
В мозг имплантируется вся «живая» конструкция целиком, но в течение нескольких недель после операции гидрогель, а также внешняя оболочка микротрубочек из карбоксиметилцеллюлозы полностью растворяются. При этом взаимодействие трансплантата с тканью мозга начинается сразу же после операции, так как один конец микротрубки открыт. Аксоны постепенно приживаются и образуют синаптические контакты с нейронами мозга, служащие для передачи нервного импульса, причем их можно «запрограммировать» на формирование синапсов со строго конкретными типами нейронов. Один аксон может сформировать множество синапсов, поэтому относительно небольшое количество вживленных аксонов может дать довольно существенный результат.
Использование живых нейронов решит проблему биосовместимости, если для этого использовать нервные клетки, полученные из индуцированных плюрипотентных стволовых клеток самого пациента. Важно, что «живые электроды» можно сделать из разных типов нейронов. Используя возбуждающие (например, глутаматергические) нейроны, можно усилить работу определенных зон мозга; тормозные ГАМКергические нейроны помогут, к примеру, притормозить излишнюю активность очага эпилепсии, а дофаминергические – бороться с болезнью Паркинсона. Это еще один большой плюс «живых электродов» – специфичность воздействия.
На сегодня ученые показали, что в мозге лабораторных крыс «живые электроды» хорошо приживаются и интегрируются в ткани, где выполняют нужные функции. Применение этой технологии на человеке, скорее всего, начнется с процедур глубокой стимуляции мозга, однако, по мнению исследователей, ее потенциал выходит далеко за эти рамки.
Фото: https://commons.wikimedia.org
Подготовила Мария Перепечаева