Папа, мама, мама и я
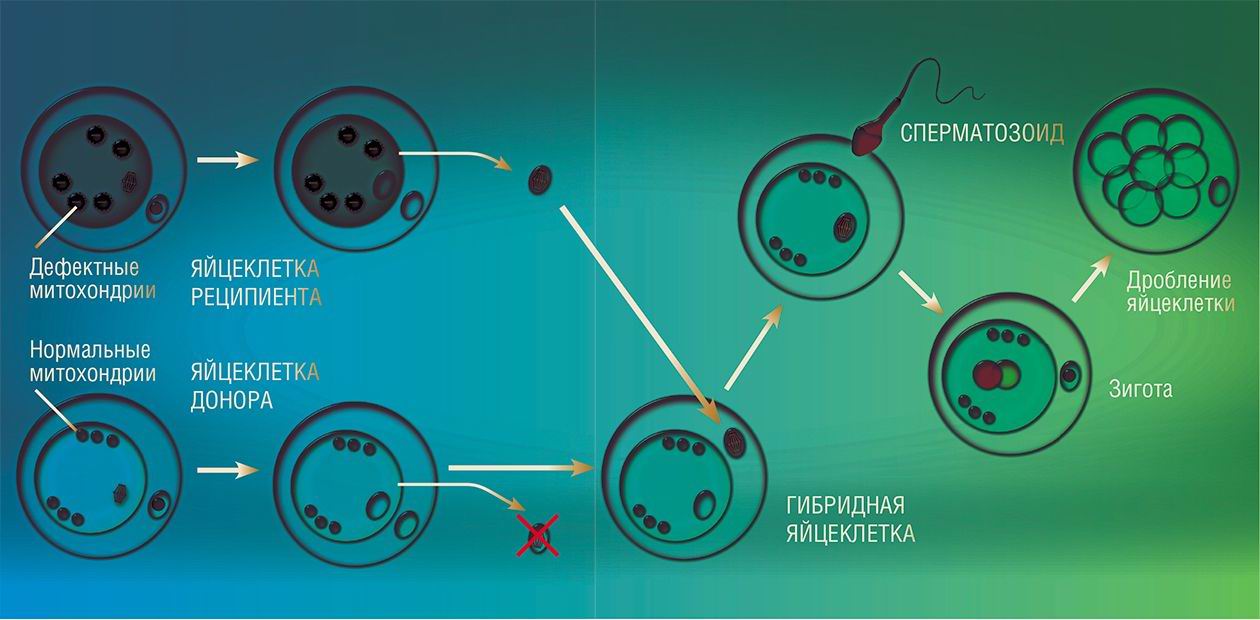
Весной 2016 г. произошло знаменательное событие: человечество пополнилось первым «ребенком от трех родителей». Это была первая успешная практическая реализация метода цитоплазматической замены у человека, когда пересаживаются не клетки, а только клеточные ядра. В данном случае клеточное ядро из яйцеклетки матери, страдающей синдромом Лея из-за «неядерных» генетических дефектов, было пересажено в «обезъядерную» яйцеклетку здорового донора. Этот метод до сих пор не применяли по этическим причинам
Среди многочисленных структур и органоидов живой клетки особое место занимают митохондрии, которые часто называют «энергетическими станциями»: их основная функция – синтез аденозинтрифосфата (АТФ), универсального соединения, служащего источником энергии для биохимических процессов. Число митохондрий в цитоплазме одной клетки варьирует от нескольких сотен до нескольких тысяч. Оно особенно велико в клетках, нуждающихся в большом количестве энергии, например, в нейронах или мышечных клетках.
Одной из интереснейших особенностей митохондрий является наличие у них собственного генома. Геном митохондрий человека сравнительно невелик и составляет всего около 16,5 тыс. пар нуклеотидов. Он содержит гены двух рибосомальных РНК, около 20 генов транспортных РНК и 13 генов белков-субъединиц ферментов, участвующих в функционировании митохондрий (для сравнения – в ядерном геноме человека содержится около 28 тыс. генов).
Как и ядерный, митохондриальный геном подвержен мутациям, которые могут приводить к развитию тяжелых наследственных болезней – митохондриальных заболеваний. Той или иной митохондриальной болезнью страдает примерно один из каждых 4 тыс. новорожденных, и проявляется такая патология обычно в самом раннем возрасте, при этом чаще всего поражается нервная система и мышцы. Среди митохондриальных болезней – синдром MELAS, наследственная оптическая невропатия Лебера, синдром Вольфа–Паркинсона–Уайта, синдром Лея и др.
Особенность наследования всех этих заболеваний в том, что они передаются только от матерей к детям, поскольку только у женской яйцеклетки есть цитоплазма, где и располагаются митохондрии, а у мужского сперматозоида ее нет. На сегодняшний день для большинства митохондриальных болезней не найдено эффективных методов лечения, что побуждает ученых для борьбы с ними искать новые, более изощренные подходы.
Один из таких подходов и был реализован в 2016 г. (Zhang et al., 2016). Матерью ребенка стала 36-летняя женщина, двое детей которой умерли в раннем возрасте от тяжелого митохондриального неврологического заболевания – синдрома Лея. Ученые из New Hope Fertility Center (Нью-Йорк, США) использовали метод пересадки ядерного генома пациентки в яйцеклетку женщины-донора со здоровыми митохондриями. Затем получившаяся яйцеклетка была оплодотворена сперматозоидом. Мальчик родился здоровым, без признаков развития синдрома Лея.
«Ребенок от трех родителей» породил множество споров научного и этического характера. Некоторые ученые склоняются к мысли, что эта технология не настолько отработана и безопасна, чтобы говорить о ее массовом применении. Ведь даже небольшое количество дефектных митохондрий, привнесенных в яйцеклетку вместе с ядром, может при развитии эмбриона размножиться (при этом доля дефектных митохондрий будет варьировать в различных типах клеток и тканей) и оказать свое губительное действие. Другие ученые указывают на тот факт, что в экспериментах на мышах было показано, что митохондрии от разных доноров по-разному влияют на многие процессы, включая функционирование самих митохондрий и накопление активных форм кислорода, а также степень ожирения и скорость формирования возрастных изменений у взрослых особей (Latorre-Pellicer et al., 2016).
По-видимому, в некоторых случаях митохондриальный и ядерный геномы действительно могут быть несовместимы. Однако любая технология требует доработки и совершенствования, сам же факт рождения здорового ребенка внушает осторожный оптимизм. Доводы противников этой технологии из-за ее этической составляющей тоже не совсем корректны. По сути, вносимые изменения касаются только митохондриального генома, содержащего небольшое число генов, задействованных в функционировании самих митохондрий. Кроме того, в случае рождения мальчиков донорские митохондрии вместе с их геномом не передаются следующему поколению, так что этот случай никак нельзя считать «бесцеремонным вторжением» в наследственность человека.
С этой точки зрения технологию рождения «детей от трех родителей» можно сравнить с пересадкой органов и тканей. Сегодня по всему миру проводятся тысячи операций по пересадке костного мозга, что фактически является пересадкой стволовых клеток, из которых формируются все клетки крови. Реципиент костного мозга становится, таким образом, практически химерным организмом, в котором нормально функционируют клетки другого человека с другим геномом. Однако эта технология эффективна и считается этически приемлемой. Будем надеяться, что и репродуктивные методики, основанные на использовании донорских яйцеклеток со здоровыми митохондриями, будут усовершенствованы и помогут тысячам семей иметь здоровых детей.
На слайдере: при «создании» новой яйцеклетки от двух матерей использовалась технология «перенос материнского веретена деления» (maternal spindle transfer, MST). Во время мейоза – клеточного деления, во время которого число хромосом уменьшается вдвое, на одной из стадий хромосомы яйцеклетки находятся в комплексе со специфической структурой из микротрубочек – шпинделем, или веретеном деления. Именно этот комплекс, образовавшийся в материнской яйцеклетке, и перенесли в яйцеклетку донора, из которой предварительно было удалено ядро. После оплодотворения получившуюся зиготу, которая начала делиться, формируя будущий эмбрион, имплантировали в матку женщины, которая родила здорового ребенка. По: (Zhang, et al., 2016)
Литература:
Zhang J., Liu H., Luo S. et al. First live birth using human oocytes reconstituted by spindle nuclear transfer for mitochondrial DNA mutation causing Leigh syndrome // Fertility and Sterility. 2016. V. 106. N. 3. P. 375—376.
Latorre-Pellicer A., Moreno-Loshuertos R., Lechuga-Vieco A. V. et al. Mitochondrial and nuclear DNA matching shapes metabolism and healthy ageing // Nature. 2016. V. 535(7613). P. 561—565.