Приручение древней молекулы
Однако можно безошибочно утверждать, что РНК из «бедного родственника» за последние четверть века превратилась в выдающегося представителя этой триады.
РНК всегда были в центре внимания исследователей Института химической биологии и фундаментальной медицины СО РАН (Новосибирск), даже когда он был лишь отделом биохимии в составе Новосибирского института органической химии. Сотрудники ИХБФМ внесли большой вклад в изучение транспортной РНК и рибосом, проверку гипотезы «мира РНК», создание новых методов химического синтеза молекул РНК, а также исследования РНК-ферментов (рибозимов). Задача у созданной в составе института на средства гранта Правительства РФ лаборатории под руководством Нобелевского лауреата С. Альтмана, открывшего каталитические свойства РНК, не из простых. Исследователи планируют с использованием многочисленных свойств РНК по направленному влиянию на клетки получить новые специфичные и безопасные препараты для лечения бактериальных, вирусных и протозойных инфекций
В начале было слово из трех букв. И слово это было – РНК…
Когда С. Альтман начал заниматься ферментом РНКазой P, которая в конце концов принесла ему Нобелевскую премию, в биологии бытовало совершенно однозначное мнение: все катализаторы в клетке – это белки. Мнение это было подкреплено Нобелевской премией (1946) американских биохимиков Д. Самнера, Д. Нортропа и У. Стэнли, ставшей эпохальным событием: американское трио доказало, что ферменты – это биологические катализаторы, т. е. представляют собой конкретные химические соединения. Тем самым была окончательно похоронена идея витализма, «жизненной силы», пронизывавшая всю биологию до XX в.
С тех пор белковая природа ферментов сомнению не подвергалась. Поэтому Альтман и его коллега Т. Чех, открывший каталитическую роль РНК в удалении из самой себя некодирующих участков (интронов), приложили очень большие усилия, чтобы опубликовать свои результаты, которые не вписывались в тогдашнюю парадигму. Но настоящая наука тем и отличается, что даже самые невероятно выглядящие результаты быстро превращаются в общепризнанные факты, если их в состоянии воспроизвести другие ученые. Признание к Чеху и Альтману пришло очень быстро: их пионерные статьи появились в 1982 и 1983 гг., а премия нашла своих героев в 1989 г. – по нынешним временам, практически мгновенно.
Работа Альтмана и его коллег вызвала всплеск интереса к РНК. Еще одна несокрушимая парадигма тех времен – так называемая «центральная догма молекулярной биологии», гласила, что РНК (а именно матричная РНК, мРНК) служит переносчиком информации между ДНК и белком. Были хорошо известны и некодирующие РНК: рибосомная и транспортная, играющие главные роли в процессе трансляции – синтеза белка по матрице РНК.
На этом функции РНК в клетке считались исчерпанными. Впрочем, уже тогда были известны короткие ядерные РНК с неясными функциями, но вряд ли кто-нибудь в то время ожидал от РНК каких-то сюрпризов. Однако и сам создатель цетральной догмы биологии Ф. Крик, и некоторые другие известные ученые, занимавшиеся происхождением жизни (Л. Оргелл, К. Вёзе), высказывали идею, что когда-то, на заре жизни, РНК могла играть большую роль, чем сейчас. Но эти теории основывались на очень косвенных соображениях. Например, что многие ферменты-белки работают только в присутствии «помощников» – коферментов нуклеотидной природы, – которые, возможно, представляют собой «ископаемые останки» предковых форм всего живого.
Открытие ферментов-РНК (далее мы будем использовать общепринятый термин «рибозим») перевернуло представление о том, что эта молекула может делать и чего не может. В 1986 г. еще один нобелевский лауреат У. Гилберт впервые произнес слова «мир РНК», подразумевая наш мир на самых ранних стадиях эволюции, когда не было еще ни ДНК, ни белков, и за «выживание» конкурировали между собой лишь самовоспроизводящиеся каталитические молекулы РНК.
С тех пор в пользу этой смелой гипотезы находятся все новые и новые подтверждения. Число известных рибозимов, как природных, так и искусственных, измеряется уже сотнями, а роль РНК проявляется во все новых и новых биологических системах. Забавный факт: в 1998 г. в Норвегии даже появилась рок-группа под названием «Ribozyme».
РНК тут, РНК там
И все же одного лишь открытия рибозимов было бы недостаточно, чтобы РНК из скромного промежуточного звена между главным хранителем генетической информации, ДНК, и главными исполнителями клеточных функций, белками, превратилась в центральный элемент, связующий воедино огромную долю процессов клеточной жизнедеятельности. В конце концов, по сравнению с белками число рибозимов очень мало, а функции их в природе ограничены. Но после работ Альтмана и Чеха РНК стала преподносить сюрпризы чуть ли не каждый год!
Какие же новые функции этой молекулы стали известны за пределами простой схемы Крика, в которой фигурировали только матричная, рибосомная и транспортная РНК? Начать можно, собственно, никуда от нее не уходя: оказывается, в такой сложной структуре, как рибосома (которая даже у бактерий состоит из трех цепей разных рРНК и нескольких десятков белков), главную реакцию – образование пептидной связи – катализируют не белки, а одна из молекул РНК!
Случаев, когда РНК выполняет каталитическую функцию, находясь в комплексе с белками, или организует сборку функционального РНК-белкового комплекса, сегодня известно очень много. Один из самых красивых и важных примеров такого комплекса – фермент теломераза, существование которого сначала «на кончике пера» предсказал советский ученый А. М. Оловников, а затем его открыли американские биологи Э. Блэкберн и К. Грейдер, удостоенные за это Нобелевской премии.
Как известно, у человека и всех эукариот хромосомы линейные, а синтез концов линейной ДНК представляет особую проблему: из-за особенностей механизма инициации синтеза ДНК каждый цикл клеточного деления теоретически должен сопровождаться утерей ее у самого конца. Однако особая структура концевых последовательностей ДНК (теломер) позволяет обойти эту проблему.
Впервые репликация теломеров была исследована Блэкберн и Грейдер у инфузории Tetrahymena, у которой в ядре соматической клетки имеется много тысяч линейных минихромосом. Теломеры состоят из большого числа консервативных коротких гексамерных повторов: у человека – TTAGGG, у Tetrahymena – TTGGGG. В активно делящихся клетках присутствует специальный фермент для репликации концов ДНК – теломераза, которая у инфузории содержит небольшую молекулу РНК, а в этой РНК имеется последовательность AACCCCAAC.
Нетрудно увидеть, что эта последовательность комплементарна полному гексамерному повтору и еще его половине. Теломераза связывает конец ДНК, достраивает шесть нуклеотидов GGGTTG по матрице своей РНК, а затем сдвигается опять же на шесть нуклеотидов так, чтобы повторить весь цикл. В этом случае все ферментативные функции выполняет белковая часть теломеразы, а РНК используется только как матрица для синтеза.
Подобных функциональных рибонуклеопротеинов в клетке предостаточно. Процесс сплайсинга (удаления из мРНК интронов) выше уже упоминался в связи с открытием Чехом рибозимов. Любопытно, что он открыл рибозимы для сплайсинга в той же инфузории Tetrahymena, так что этот скромный организм прочно вписал себя в историю молекулярной биологии.
Так или иначе, но у большинства организмов, в том числе и человека, сплайсингом занимаются не рибозимы в чистом виде, а так называемые малые ядерные рибонуклеиновые частицы, представляющие собой комплексы РНК с белками, в которых РНК играет и структурную, и каталитическую роль. Или другой, достаточно неожиданный пример: оказывается, что белки, секретируемые клеткой, при синтезе пересекают мембрану эндоплазматической сети, а для этого они взаимодействуют с так называемой «частицей, узнающей сигнал» (SRP) – рибонуклеопротеином, состоящим из одной молекулы РНК и шести белков.
В начале 2000-х годов были открыты и так называемые рибосвитчи – РНК-переключатели биохимических процессов. Это участки молекул мРНК, которые сами ничего не кодируют, могут, связывая какую-то сигнальную молекулу в клетке, менять свою структуру и тем самым влиять на процесс транскрипции. Например, тиаминовый рибосвитч, открытый российскими учеными из Института генетики и селекции промышленных микроорганизмов (Москва), связывается с тиаминпирофосфатом – производным витамина B1, что снижает трансляцию мРНК генов, участвующих в синтезе витамина B1. Раз этого витамина много, клетке можно не тратить силы на его производство.
Очень часто мы знаем, что в каком-то клеточном процессе участвует некодирующая РНК, но не можем пока определить механизм, по которому этот процесс происходит. Например, во всех клетках женского организма одна из двух X-хромосом сконденсирована и практически не принимает участия в синтезе белков. Для такой конденсации необходима некодирующая РНК Xist, множество копий которой как бы покрывает одну из X-хромосом. Как именно РНК Xist связывается с хромосомой, какая хромосома выбирается – до сих пор не очень понятно. Кстати, в исследование функций этой РНК внесли большой вклад новосибирские ученые из лаборатории С. М. Закияна Института цитологии и генетики СО РАН.
А для того чтобы в клетке человека началась репликация – удвоение генома, нужна так называемая Y-РНК, которая связывается с точками начала репликации. Но что происходит дальше, пока остается тайной.
Наконец, некодирующие РНК часто выступают как регуляторы активности генов по принципу комплементарности – эта идея, высказанная академиком Д. Г. Кнорре, оказалась востребована самой природой. Взять, например, феномен РНК-интерференции, обнаруженный в 1998 г. американцами К. Мелло и Э. Файером. Кстати сказать, оказалось, что у растений подобное являение наблюдали еще в 1920-х гг., но тогда не смогли правильно истолковать. Суть его в том, что линейные двуцепочечные, или шпилечные, РНК могут подавлять экспрессию генов, содержащих гомологичные им последовательности. Усилиями многих ученых был очень скоро установлен механизм этого процесса. Как правило, при наличии точного комплементарного соответствия мРНК и коротких интерферирующих РНК (киРНК) происходит деградация мРНК, а при неполном комплементарном соответствии трансляция мРНК просто блокируется. Однако молекулярные детали этих процессов полностью еще не выяснены. РНК-интерференция может также регулировать структуру и уровень конденсации хроматина.
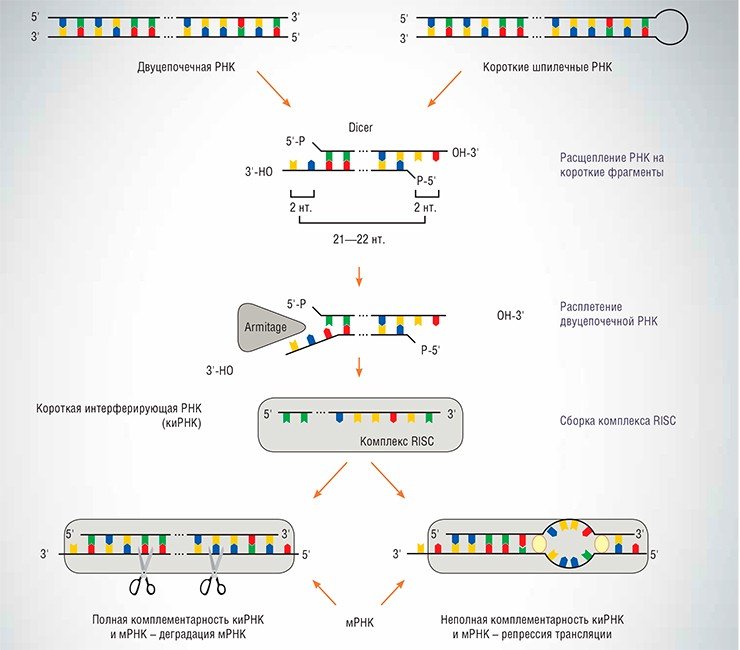
Когда механизм РНК-интерференции прояснился и стало понятно, что можно использовать ее для подавления экспрессии практически любого гена в клетке, ему начали придумывать разные полезные приложения. Сначала, разумеется, в лабораторной практике: подавление экспрессии гена при помощи РНК-интерференции, или нокдаун гена (по аналогии с нокаутом, т. е. удалением гена), прочно вошло в практику молекулярно-биологических лабораторий. Сейчас существуют даже специальные сервисы: вы даете им последовательность нужного гена, а они и интерферирующую РНК разработают и синтезируют генную конструкцию, которая будет эту РНК производить.
Но, конечно, лабораторными инструментами дело не ограничилось – на основе РНК-интерференции начали разрабатывать терапевтические средства. Первыми в клинических испытаниях стали исследовать интерферирующие РНК для обращения дегенерации сетчатки глаза и лечения инфекции респираторным синцитиальным вирусом, который вызывает больше всего заболеваний дыхательных путей у новорожденных и маленьких детей. Этим дело не ограничилось – сейчас готовятся к клиническим испытаниям и антивирусные РНК против герпеса, гепатитов A и B, вируса иммунодефицита человека, гриппа, кори и даже онкологичесих заболеваний.
РНК-интерференция нашла свое место даже в сельском хозяйстве. Так, известная биотехнологическая фирма «Монсанто» cейчас работает над сортами культурных растений, производящих инсектицидные интерферирующие РНК. А американские ученые вывели сорт хлопка, семена которого съедобны, потому что в них методом РНК-интерференции нарушено производство токсина госсипола.
К концу прошлого столетия оставался неясным один момент. Если в клетке есть специальный механизм, работающий с молекулами РНК, которые вводят в клетку исследователи, значит, это, наверное, неспроста? Иначе зачем клетке содержать несколько белков, которые выполняют скоординированную работу по использованию того, что «подсунули» ей ученые?
И вот, в начале 2000-х гг. прогремело новое открытие – микроРНК. Как обычно, оказалось, что первая такая РНК была обнаружена ранее в микроскопическом почвенном черве-нематоде Caenorhabditis elegans, модельном организме для генетики развития, но в то время сущность этого открытия не была понята.
МикроРНК в клетке образуются из РНК таким же способом, как и искусственно внесенные двуцепочечные РНК: сначала молеклы нарезаются на куски, а затем идет процесс, аналогичный РНК-интерференции. С тех пор были открыты сотни микроРНК: по всей видимости, они входят в число важнейших регуляторов активности генов человека.
Российские нуклеиновые кислоты
Задача у новосибирской лаборатории С. Альтмана, созданной на средства мегагранта, не из простых: создать новый вид соединений для лечения бактериальных, вирусных и протозойных инфекций. Микробы стали сейчас устойчивыми ко многим антибиотикам, и если смотреть правде в глаза, то становится ясным, что современное здравоохранение висит на волоске, ведь уже появились штаммы стафилококка и туберкулезной палочки, устойчивые практически ко всем известным антибиотикам. С другой стороны, бесконтрольное применение антибиотиков не только провоцирует развитие лекарственной устойчивости, но и опасно для самих больных, поскольку лекарства убивают не только болезнетворных бактерий, но и полезных обитателей нашего желудочно-кишечного тракта.
Так возникла идея использовать для борьбы с патогенами ген-направленные соединения, которые будут убивать только вполне определенный микроб и не трогать другие. Ведь если строение бактериального гена известно, можно синтезировать подходящий олигонуклеотид – цепочку РНК, ДНК или каких-то модифицированных нуклеиновых кислот, которая «прилипнет» именно к конкретной нуклеиновой кислоте. Если к этой направляющей части присоединить молекулу, которая будет поражать нуклеиновую кислоту-мишень, то мы получим ген-направленный реагент, который будет действовать только на целевой геном. Конечно, нужно еще научиться защищать такое лекарство от разрушения в организме, сделать его нетоксичным, а главное – «научить» его проникать внутрь клетки.
В работе по мегагранту с российской стороны участвуют и химики, которые синтезируют нуклеиновые кислоты, и микробиологи, испытывающие эти соединения на реальных мишенях. Некоторых целей уже удалось достичь – так, создан вариант олигонуклеотида, который не разрушается в крови.
А вот проблема доставки препарата в бактериальные клетки пока остается неприступной. Для ее решения специалисты ИХБФМ СО РАН испытывают природные переносчики в виде разнообразных пептидов.
Параллельно идет работа над олигонуклеотидным препаратом против вируса гриппа – это относительно простая задача, потому что вирусные нуклеиновые кислоты уже находятся в инфицированной клетке человека, куда попасть гораздо легче, чем в бактериальную, окруженную плотной белково-полисахаридной оболочкой. В общем новосибирские ученые одновременно просчитывают много вариантов, и вполне вероятно, что какой-то из них окажется выигрышным.
Новые трюки прирученной РНК
В институтской лаборатории нобелевского лауреата сейчас разворачивается и большой проект по «приручению» РНК для еще одной цели – клеточной терапии.
У этого направления есть своя занимательная и богатая история. Можно сказать, что она берет начало от овечки Долли, которую клонировал в 1996 г. из клетки вымени шотландец И. Вилмут. Для подобного клонирования – так называемого «переноса ядра соматической клетки» – требуется яйцеклетка, из которой удаляют ядро, и клетка-донор, из генетического материала которой потом развивается организм. На самых первых этапах развития клетки эмбриона, получившиеся в результате такого переноса, сохраняют свою плюрипотентность, т. е. способность превратиться в любую клетку взрослого организма.
После работ Вилмута перед человечеством замаячила довольно страшная, с этической точки зрения, перспектива: взрослый человек, который хочет подлечиться, создает свой клон, из которого изымаются либо клетки на ранней эмбриональной стадии, либо органы – на стадии более поздней. И это не беспочвенные страхи: в современной медицине известны случаи, когда родители специально рожали здорового ребенка, чтобы он стал донором костного мозга для старшего брата или сестры, страдающих от какой-нибудь редкой наследственной болезни.
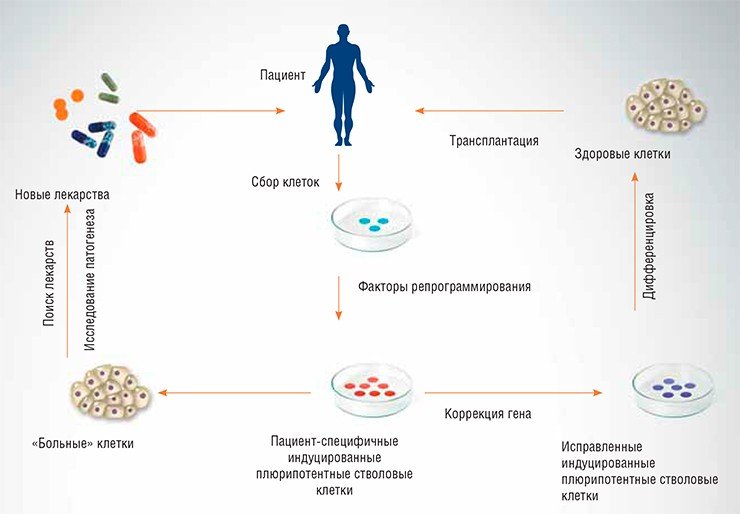
Гордиев узел этических проблем клонирования одним махом разрубил в 2006 г. японец С. Яманака, который нашел способ получать плюрипотентные клетки почти из любой клетки тела без необходимости создания и последующей разборки эмбриона. Оказалось, что для этого необходимо ввести в клетку активно работающие копии всего четырех генов-регуляторов: Sox2, Oct4, Klf4 и c-Myc. В результате клетка печени, например, превращается в индуцированную плюрипотентную стволовую клетку (ИПС-клетку), которую потом можно подтолкнуть к преобразованию хоть в клетку печени, хоть в нейрон, хоть в лейкоцит. В исследованиях на лабораторных мышах даже было показано, что из таких клеток могут рождаться мышата, вырастающие во вполне здоровых и плодовитых мышей.
Открытие Яманаки дало надежду, что скоро мы научимся лечить почти любую наследственную болезнь. В самом деле, если бы из пациента можно было взять клетки, сделать из них ИПС-клетки, исправить в них генетический дефект и затем пересадить обратно пациенту, это помогло бы справиться со многими генетически обусловленными недугами.
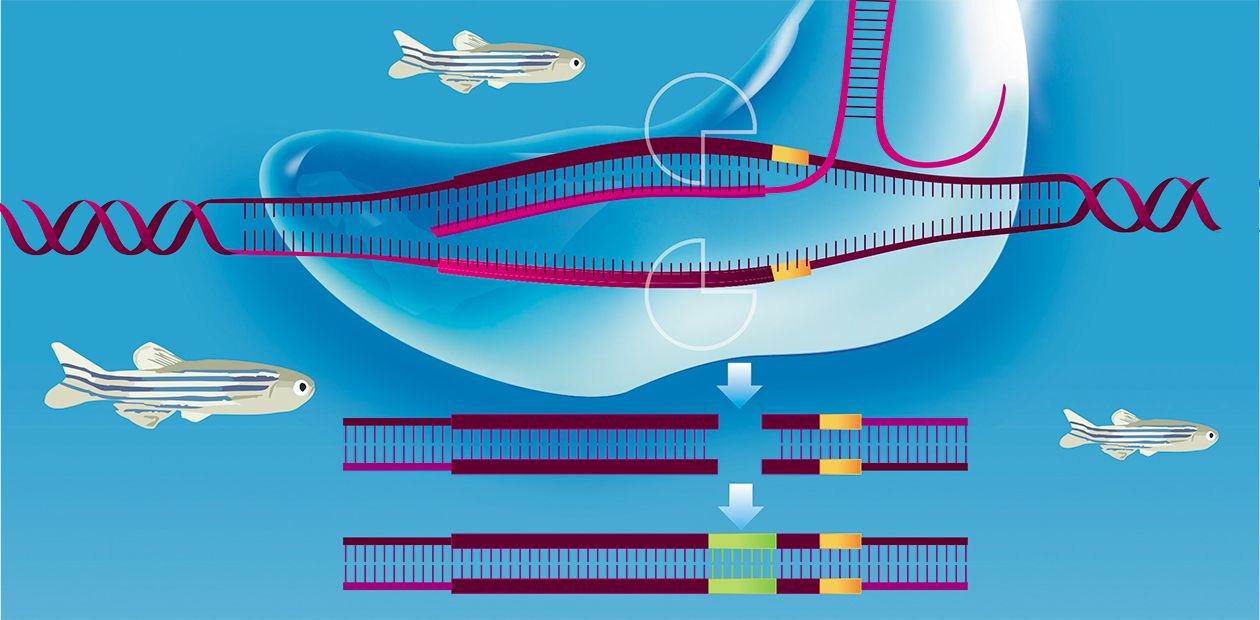
Остается один маленький неясный момент: как исправить геном клетки? В принципе биологи уже умеют это делать, используя процесс гомологичной рекомбинации (таким образом с конца 1980-х гг. получают трансгенных животных), но у этой процеруды слишком низкая эффективность. И опять решение пришло, откуда не ждали. Еще в 1987 г. в геноме бактерий были обнаружены многочисленные участки-повторы CRISPR, с которых синтезируются маленькие РНК. Оказалось, что бактерии используют их для защиты от вирусов-бактериофагов: с их помощью уничтожаются «вражеские» нуклеиновые кислоты, которые вирус впрыскивает в бактерию. Бактерии же умеют распознавать это вторжение и посылают небольшие кусочки РНК, чтобы они связались с нуклеиновой кислотой «агрессора». Эти РНК действуют не сами по себе, а в комплексе с белком Cas9, который расщепляет ДНК или РНК вируса.
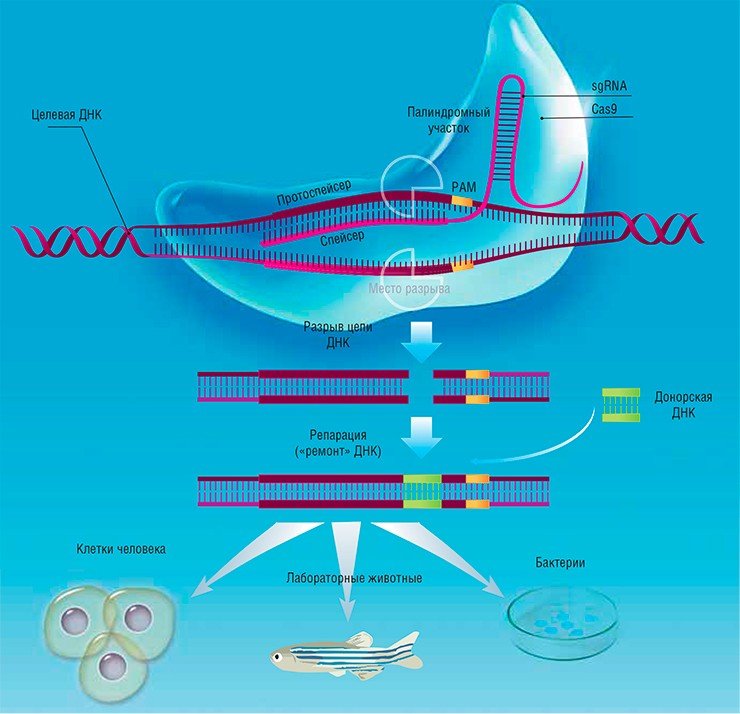
Но почему бы подобную систему использовать не только против вируса? Достаточно создать нужную нацеливающую РНК – и система CRISPR/Cas9 расщепит любую ДНК, какую мы захотим. А если в это же время ввести в клетку «донор» генетического материала (например, олигонуклеотид с исправленной последовательностью), то разрыв будет исправлен клеточными системами репарации ДНК. Таким образом, в геноме можно исправить любую мутацию. Справедливости ради стоит отметить, что это не единственный способ редактирования генома, но, по-видимому, система CRISPR/Cas9 является самой эффективной.
Разумеется, новосибирские ученые обратили внимание на такой многообещающий инструмент. С его помощью они собираются получить клетки, которые несут мутации, встречающиеся у пациентов с болезнью Альцгеймера, болезнью Паркинсона и некоторыми другими наследственными заболеваниями. Такие клетки очень нужны исследователям, занимающимся поиском новых лекарств, ведь только клетки человека могут дать наиболее правильные представления о том, как развивается болезнь. Эксперименты на животных здесь зачастую вообще неприменимы, например, болезни Альцгеймера не подвержены даже человекообразные обезьяны. И наоборот, из клеток больных наследственными заболеваниями с помощью этой системы можно делать нормальные, здоровые клетки. Для этого ученые ИХБФМ в сотрудничестве с Институтом патологии кровообращения им. Е. Н. Мешалкина выбрали синдром длинного интервала QT – одну из частых причин наследственных болезней сердца.
Но даже для для такого хорошего редактора геномов, как CRISPR/Cas9, эффективность процесса оставляет желать лучшего. Понятно, что способы его усовершенствования имеются, ведь первые работы по геномному редактированию с использованием этой системы вышли в свет только в 2013 г.
Узкое место процесса – репарация разрыва ДНК с использованием донорного олигонуклеотида в качестве матрицы, так как эта реакция проходит с не очень высоким выходом. Однако – такая удача! – репарация ДНК также входит в число основных научных интересов ИХБФМ.
Одно из подразделений института – группа взаимодействий биополимеров, занимается разработкой новых конструкций донорных олигонуклеотидов, которые должны резко повысить эффективность геномного редактирования. Более того, процесс репарации ДНК востребован и в конверсии обычных клеток в плюрипотентные, поэтому в группе также ведутся работы, поддержанные грантом Российского научного фонда, которые призваны значительно облегчить получение ИПС-клеток по сравнению с классической схемой Яманаки.
Представим теперь, что нам удалось исправить клетки и пересадить их обратно пациенту, где они начинают взаимодействовать со всем организмом. Читатель, не удивляйся – и здесь тоже замешана РНК! Совсем недавно было установлено, что клетки секретируют в кровь и другие биологические жидкости специальные частицы – экзосомы, состоящие из белка и РНК. Они, вероятно, представляют собой часть абсолютно нового механизма межклеточной сигнализации, при котором клетка передает часть генетического материала другим клеткам организма. Однако ни механизм образования экзосом, ни принципы, по которым отбираются для них белки и РНК, совершенно неизвестны. Но все эти вопросы также находятся в фокусе внимания новосибирских ученых.
Конечно, неправильно говорить, что РНК – это самая важная молекула жизни. Без ДНК и белков жизнь также была бы невозможна, а «мир РНК», скорее всего, давным-давно кончился бы, если бы природа не придумала современное разделение функций между ДНК, РНК и белком.
Однако можно безошибочно утверждать, что РНК из «бедного родственника» за последние четверть века превратилась в выдающийся член этой триады. Исследования, идущие в ИХБФМ СО РАН, призваны наилучшим образом использовать многочисленные функции РНК для направленного влияния на клетки, что позволит создать новые высокоэффективные технологии для медицины.
Литература
Власов В. В., Воробьев П. Е. Мир РНК: вчера и сегодня // Наука из первых рук. 2012. № 3 (45). С. 40–49.
Горман К., Файн Марон Д. Революция в мире РНК // В мире науки. 2014. № 6. С. 70–77.
Григорович С. Вначале была РНК? В поисках молекулы первожизни // Наука и жизнь. 2004. № 2.
Работа поддержана грантом РНФ 14-24-00093