Генетический паспорт действителен с рождения, или Гадание на генах
В течение всей истории человечества люди стремились предсказать свое будущее, начиная от гаданий на внутренностях жертвенных животных до ворожбы на картах и кофейной гуще. Открытие тайн генетического кода поставило некоторые из этих прогнозов на твердую научную основу. Оказалось, что здоровье и продолжительность жизни каждого из нас во многом предопределены уникальной комбинацией из определенных генных вариантов, доставшейся нам в «наследство» от родителей. К тому же, в отличие от роста, мышечной массы и шевелюры, генотип человека – это единственное, что остается неизменным на протяжении всей его жизни. И хотя конкретная реализация наследственного потенциала будет зависеть от внешней среды, результаты «гадания на генах» могут указать на скрытые подводные камни и помочь составить максимально безопасный маршрут в неспокойном житейском море
Идея, что разных людей нужно лечить по-разному, имеет тысячелетнюю историю: еще Гиппократ считал, что нужно «давать разные лекарства разным пациентам и то, что хорошо для одного, может не быть полезным для другого». Однако этот принцип не сразу прижился в привычной нам классической медицине, которая, в отличие от традиционной, не придавала большого значения индивидуальным особенностям пациента, таким как конституция, образ жизни, питание и физическая активность, а также характер протекания болезни.
Однако с конца прошлого века в литературе все чаще стал встречаться термин персонализированная медицина. Началось формирование новой модели организации медицинской помощи, в основу которой легло представление о пациенте как уникальном организме со своими генетическими, физиологическими и биохимическими характеристиками. И их надо обязательно учитывать, разрабатывая оптимальную схему диагностики, лечения или профилактики болезней для конкретного человека.
В персонализированной медицине сегодня можно выделить несколько важных составляющих. Среди них – индивидуальный мониторинг здоровья с помощью современных медицинских цифровых технологий, включая специальные приложения для мобильных устройств и компактные персональные анализаторы. Это позволяет любому человеку рутинно, не обращаясь к помощи здравоохранения, ежедневно контролировать важнейшие физиологические и метаболические параметры своего организма, а накопление такой информации может помочь в составлении индивидуальной программы лечения и поддержания здоровья.
Еще одна составляющая – клеточные технологии, основанные на использовании собственных стволовых клеток пациента, которые можно превращать в клетки различных органов и тканей. Такие технологии расширяют возможности регенеративной медицины, их можно использовать для создания индивидуальных вакцин против онкологических заболеваний и т. п. Клинические перспективы этого направления безграничны, однако применение их в медицинских целях сегодня имеет ряд этических и законодательных ограничений.
И все-таки решающим шагом в появлении современной персонализированной медицины стало развитие геномики и генодиагностики, которые легли в основу еще одного мирового тренда – предсказательной медицины.
Смысл этого подхода в том, чтобы на основе анализа ДНК выявить предрасположенность конкретного человека к тому или иному заболеванию, оценить особенности его метаболизма, адаптивные возможности и т. п. Безусловно, речь при этом обычно идет лишь о вероятности (риске), так как в развитии любой патологии огромную роль играют внешние факторы. Как показали исследования на близнецах, это относится и к таким мультифакторным заболеваниям, как сахарный диабет, бронхиальная астма, ишемия сердца, атеросклероз и т. д. Тем не менее генетический анализ дает возможность получить научно взвешенные рекомендации по поддержанию здоровья и внести необходимые коррективы в привычный образ жизни.
Как это работает
Сегодня термином «генетический паспорт» никого не удивишь. И это тем более поразительно, если вспомнить, что амбициозный международный проект по расшифровке первого генома человека, стартовавший в конце прошлого века, обошелся примерно в 3 млрд долларов. Еще в начале нашего столетия подобный анализ оценивался примерно в 300 тыс. долларов, так что медицинские перспективы генодиагностики в то время выглядели достаточно туманными. Однако появление высокотехнологичных систем секвенирования генома привело к настоящему обвалу цен, устремившихся к заветной цифре в одну тысячу долларов.
Кстати сказать, обычный индивидуальный генетический паспорт сегодня очень далек от полной инвентаризационной описи всего генома, и не только из-за его стоимости. Не менее важно то, что роль огромного числа генов в патогенезе болезней еще до конца не выяснена, а ряд редких генных мутаций функционально не описан.
Тем не менее исследования отдельных генов и генных локусов активно ведутся по всему миру, и соответствующая информация растет, как снежный ком. Когда обнаруживаются мутации, связанные с определенным заболеванием, проводят исследования частоты их встречаемости у здоровых и больных людей для оценки их прогностической значимости. На сегодня охарактеризовано уже несколько тысяч таких генных вариантов, связанных с риском возникновения внушительного ряда патологий. Среди них: сахарный диабет 2-го типа, сердечно-сосудистые заболевания, тромбофлебит, остеопороз, гормональные расстройства, репродуктивные нарушения… Известен и целый ряд мутаций, специфичных для онкологических заболеваний, и число их будет расти, так как в онкогенез могут вовлекаться десятки и сотни самых разных генов.
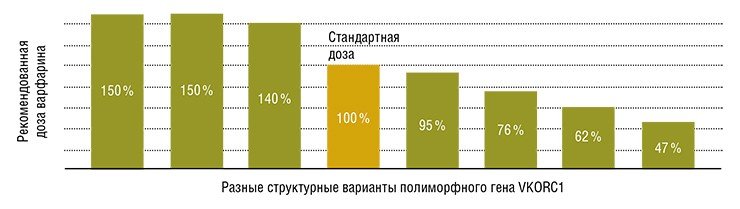
В Центре новых медицинских технологий (Новосибирск) любой человек может получить генетический паспорт с результатами генодиагностики по следующим направлениям: расширенный гемостаз, эндотелиальная дисфункция, артериальная гипертензия, липидный обмен, риск возникновения остеопороза, атопии, рака молочной железы и яичника, а также по нутригеномике и фармакогеномике. Стоимость полной генодиагностики по любому из направлений составляет на сегодня 25 тыс. рублейИзучение генетического профиля помогает подобрать более эффективную лекарственную терапию, так как для многих фармакологических препаратов уже найдены генетические маркеры чувствительности и безопасности. Например, установлено, что женщинам с генетически детерминированной склонностью к повышению вязкости крови нужно с осторожностью использовать гормональные контрацептивы, так как они повышают риск развития тромбозов. Как показали наши данные, в Новосибирске примерно пятая (!) часть больных тяжелыми сердечно-сосудистыми заболеваниями невосприимчивы к антиагрегантному препарату клопидогрелу, который они принимают по назначению врача.
 Как можно получить свой генетический паспорт? Сейчас такую услугу (платную) предоставляют ряд медицинских учреждений и клиник. Например, в нашем городе (Новосибирске) изучением роли генетических нарушений в патогенезе болезней и разработкой новых методов генетического анализа занимается лаборатория персонализированной медицины Центра новых медицинских технологий (ЦНТМ) Института химической биологии и фундаментальной медицины СО РАН, а уже апробированные решения внедряются в сети медицинских клиник центра. На сегодняшний день здесь предлагается более 50 генетических панелей, самая большая из которых включает более 200 генов – практически все известные маркеры потенциальных наследственных заболеваний и чувствительности к лекарствам. Все панели очень «широкие», поэтому результаты анализов позволяют дать достаточно целостную картину, а не отдельные разрозненные факты.
Как можно получить свой генетический паспорт? Сейчас такую услугу (платную) предоставляют ряд медицинских учреждений и клиник. Например, в нашем городе (Новосибирске) изучением роли генетических нарушений в патогенезе болезней и разработкой новых методов генетического анализа занимается лаборатория персонализированной медицины Центра новых медицинских технологий (ЦНТМ) Института химической биологии и фундаментальной медицины СО РАН, а уже апробированные решения внедряются в сети медицинских клиник центра. На сегодняшний день здесь предлагается более 50 генетических панелей, самая большая из которых включает более 200 генов – практически все известные маркеры потенциальных наследственных заболеваний и чувствительности к лекарствам. Все панели очень «широкие», поэтому результаты анализов позволяют дать достаточно целостную картину, а не отдельные разрозненные факты.
Сама процедура прохождения теста очень проста: нужно сдать обычный образец крови из вены. Результаты генетических анализов поступают к нашим терапевтам и генетикам, которые и дают заключение. Для этого используются специальные интерпретирующие программы для подготовки отдельных блоков информации, которые затем проверяются и объединяются специалистом. Эти программы создавались в течение нескольких лет на основе изучения огромного числа литературных источников, чтобы аккумулировать все научные результаты, имеющиеся в мире по тому или иному вопросу.
Пациент и его лечащий врач получают индивидуальное заключение в виде развернутого описания персональных особенностей. Но на этом их взаимодействие не заканчивается: пациент всегда может получить дополнительную очную или заочную консультацию своего лечащего врача или врачей-генетиков. Такая практика выгодно отличает наш центр (ЦНМТ) от других организаций, которые предлагают своим клиентам просто стандартные наборы рекомендаций для разных генотипов.
Есть ли у вас «право» это съесть?
В последние годы одним из приоритетных направлений лаборатории персонализированной медицины ЦНМТ является нутригенетика, изучающая генетические предрасположенности к заболеваниям с учетом потребления тех или иных питательных веществ. На самом деле речь идет об определении рисков, которые лежат на пути к здоровому телу и высокому качеству жизни, и возможностей достичь этих целей.
ЗАПРОГРАММИРОВАННАЯ ЗАВИСИМОСТЬ? В известной психобиологической модели индивидуальности Р. Клонингера черты темперамента соотносятся с определенными биохимическими системами мозга (Разумникова, 2005).Люди с высокими значениями по шкале «избегание ущерба» характеризуются тревожностью, застенчивостью, страхом перед опасностью и неизвестностью и не склонны к необдуманным поступкам, связанным с высоким риском. Такое поведение Клонингер связал с серотониновой системой мозга. Исследования показали, что ген, кодирующий рецептор серотонина – белок HTR 2A, действительно имеет полиморфный локус, влияющий на активность передачи сигнала.
Высокие оценки по шкале «поиск новизны» получают импульсивные, раздражительные индивидуумы, склонные нарушать мешающие им правила. Оценки по этому критерию обычно выше у больных с различными формами патологических зависимостей (наркоманией, алкоголизмом, игроманией). Выраженность этих проявлений зависит в том числе от унаследованной версии гена DRD 2, кодирующего рецептор к дофамину – «гормону удовольствия». Носители «патологического» варианта гена (около 5 % популяции) с низким уровнем этого гормона могут начать переедать в стрессовых ситуациях при отсутствии чувства голода, что приводит к появлению лишнего веса. Схожим эффектом обладает полиморфный ген опиоидного рецептора OPRM1 (van den Wildenberg, 2007)
В этой области мы также предлагаем ряд генетических панелей. Самая короткая (11 генетических маркеров) программа дает людям, стремящимся быстро снизить вес и поддерживать здоровый образ жизни, базовое представление о выборе диеты, интенсивности физических нагрузок, риска таких вредных привычек, как курение, и т. п. Есть «промежуточные» программы исследований, призванные отвечать на конкретные вопросы, касающиеся, к примеру, индивидуальной переносимости физической нагрузки. А самая большая панель нутригенетических тестов включает уже 79 параметров, и заключение с рекомендациями, которое получает пациент, занимает 60—70 страниц.
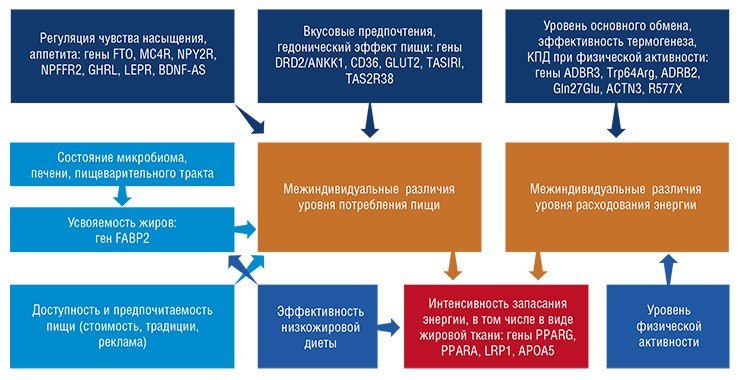
Многих к таким программам привлекает простое желание «похудеть», но на самом деле главное здесь – это сохранение и улучшение здоровья. Дело в том, что избыточная масса тела и ожирение – это не только эстетическая проблема, но и значимый фактор риска развития атеросклероза, артериальной гипертонии и других многофакторных заболеваний. Избыточный вес негативно влияет и на эндокринную систему, провоцируя развитие сахарного диабета II, а также может стать причиной женского и мужского бесплодия.
Все эти признаки – абдоминальное ожирение, устойчивость тканей к инсулину, повышение уровня глюкозы и липидов, рост артериального давления – объединены в понятие метаболический синдром. Свой вклад в развитие этой «болезни века», помимо погрешностей в питании и малоподвижного образа жизни, вносят генетические факторы.
Избыточный вес у многих людей возникает в силу особенностей пищевого поведения: позднего насыщения, раннего возникновения чувства голода, склонности к частым перекусам. Исчезновение чувства голода после приема пищи связано в том числе и с нейроэндокринными реакциями – выделением активных веществ, влияющих на центр насыщения головного мозга. При разных вариантах генов, влияющих на эти процессы, скорость возникновения чувства сытости также может различаться.
КОФЕ: ПИТЬ ИЛИ НЕ ПИТЬ? Один из важнейших компонентов кофе – кофеин, обладающий тонизирующим эффектом, поэтому кофе кратковременно улучшает внимание, особенно когда человек утомлен. А его систематическое употребление может улучшить чувствительность к инсулину и снизить риск развития сахарного диабета 2-го типа. Есть данные, что кофе также значительно снижает риск развития цирроза печени и рака молочной железы. К нежелательным эффектам кофеина относят способность влиять на количество сердечных сокращений (может вызвать тахикардию) и сосудосуживающий эффект. Кроме того, кофеин способствует выведению костного кальция, а дубильные вещества кофе не показаны при язвенной болезни и обострении хронического гастрита.Польза и вред этого любимого напитка миллионов людей часто служит предметом спора не только среди простых обывателей, но и ученых. Но, может быть, в данном случае важнее не «что», а «кому» и «сколько»?
Кофеин выводится из организма печенью. Скорость его метаболизма, как и многих других соединений, определяется особым ферментом – цитохромом CYP1A2. Ген, кодирующий этот фермент, имеет 3 разных варианта, связанных с разной скоростью метаболизма кофе: «F» – быстрый, «С» – медленный, «A» – промежуточный. Так как у каждого человека гены представлены двумя копиями – от отца и матери, среди людей, соответственно, встречается 6 генетических комбинаций.
Носителям варианта «F» употребление кофе не противопоказано, а в некоторых случаях даже желательно. И, напротив, кофе не рекомендуется при генотипе «С», так как повышает риск развития сердечно-сосудистых заболеваний. Важно, что фермент CYP1A2 играет ключевую роль в метаболизме не только кофе, но и эстрогенов – женских половых гормонов. Повышенное (свыше 2 чашек в день) потребление кофе у женщин – носителей «быстрого» варианта гена – конкурентно ингибирует метаболизм эстрогенов и снижает их проканцерогенный эффект. Это было подтверждено более поздним развитием болезни у пациенток с раком молочной железы (Bageman et al., 2008).
Интересно, что индивидуальное восприятие вкуса кофе также генетически детерминировано. Речь идет о вкусовых рецепторах, воспринимающих «горечи», в том числе антиоксидантные вещества кофе с горьковатым привкусом. Например, ген, кодирующий рецептор TAS 2R 38, встречается в нескольких вариантах. Носители варианта AVI/AVI чаще демонстрируют любовь к кофе, чем люди с генотипом PAV/PAV, которые обычно добавляют в кофе молоко, сахар и другие добавки для снижения ощущения горечи. А носители варианта AVI/AVI чаще употребляют брокколи и другие виды капусты. Эти «любители кофе и брокколи» характеризуются более низким уровнем в крови глюкозы и С-реактивного белка – маркера воспалительных заболеваний (Mikołajczyk-Stecyna et al., 2017)
Например, мутации в генах FTO и MC 4R определяют разную восприимчивость к лептину – гормону, концентрация которого во время приема пищи возрастает и который влияет на чувство насыщения через регуляцию аппетита в головном мозге. Людям с неблагоприятными вариантами этих генов трудно контролировать объем съеденного, что и определяет склонность к перееданию.
Возникновение чувства голода – это сложный процесс, регулируемый в том числе и уровнем особых орексогенных белков, таких как грелин. Один из вариантов полиморфного гена GHRL, кодирующего этот белок, отвечает за высокий уровень грелина, что провоцирует появление «раннего» чувства голода. Другие варианты этого гена ассоциированы с отдельными компонентами метаболического синдрома, включая высокий уровень холестерина, систолическое кровяное давление и др.
Как известно, провоцирующим фактором развития сердечно-сосудистых заболеваний и появления избыточной массы тела служит высокое потребление насыщенных («твердых») жиров (сливочного масла, животных жиров и др.). В этом случае высокий риск развития гиперлипидемии (повышения уровня липидов в крови) имеют носители определенных вариантов генов, кодирующих белки аполипопротеины, которые стимулируют расщепление жиров, ингибируют синтез липидов в печени, участвуют в производстве и утилизации холестерина. Носителям таких генов особенно важно ограничить потребление гидрогенизированных жиров, входящих в состав маргарина и нарушающих транспорт питательных веществ через клеточные мембраны.
Подобных примеров очень много: «генетические корни» обнаруживаются в 40—70 % случаев избыточного веса. Поэтому контроль за содержанием в рационе веществ, вредных или полезных с точки зрения генетической предрасположенности, – один из подходов для профилактики и лечения метаболического синдрома.
Большой плюс генетических исследований в том, что их можно проводить в любом возрасте. Более того, сегодня мы рекомендуем пройти тесты на наследственные заболевания всем потенциальным родителям. Генетическая экспертиза показана и детям в случае, если есть отклонения в здоровье. Серьезно же подойти к этой проблеме стоит после 25 лет, потому что болезни в наше время быстро «молодеют», и с наступлением зрелого возраста человек уже должен жить осознанно, соблюдая превентивные меры безопасности. Таким образом можно отодвинуть на 10—15 лет реализацию даже выраженной наследственной предрасположенности к той или иной болезни.
СПОРТ И ГЕНЫ Генетическая предрасположенность к формированию спринтерских и стайерских качеств обусловлена наличием в мышце разных мышечных волокон. Белые волокна рассчитаны на высокую скорость и силу сокращения, но при этом они не могут сокращаться долго. Важным их компонентом является белок альфа-актин‑3. Ген, кодирующий этот белок, встречается в разных вариантах, и при наличии варианта «Х» белок вообще не образуется. Исследование на олимпийских спортсменах показало, что аллель «Х» чаще встречается у стайеров, а вариант «ХХ» вообще не был обнаружен у спринтеров.Результативность физических нагрузок в целях снижения веса также имеет генетическую подоплеку, связанную с рецепторами к гормону адреналина. При физических нагрузках мышцам требуется больше кислорода и энергии для активного сокращения, что и достигается работой адренергической системы. Адреналин и норадреналин, связываясь со своими рецепторами, стимулируют повышение частоты сердечных сокращений, а также мобилизуют «запасы» жиров и углеводов. Разные варианты этих рецепторов обеспечивают разнообразие эффектов, наблюдаемых при физической нагрузке. В зависимости от генотипа человека можно отнести к «энергозатратному» или «энергосберегающему» типам. В первом случае добиться сжигания излишних энергетических запасов можно с помощью обычных физических упражнений, во втором же случае потребуются более интенсивные тренировки
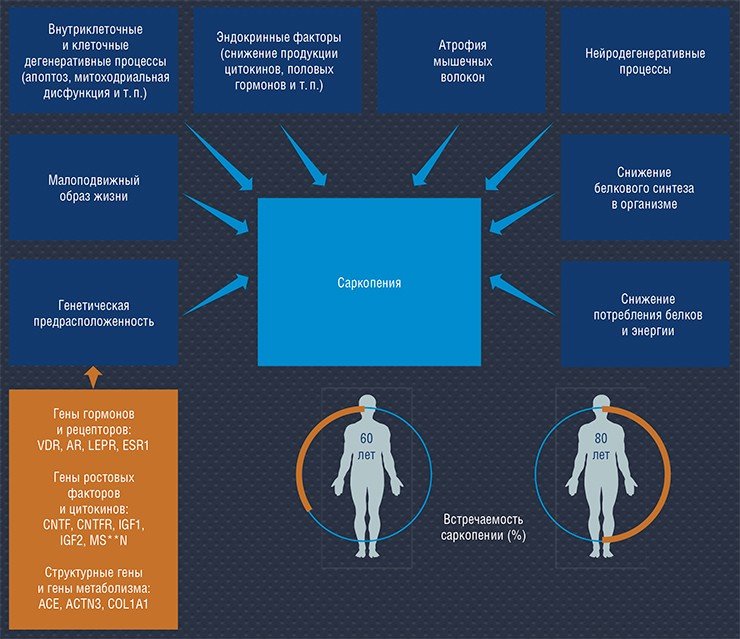
Одна из наших последних идей, которая еще находится в разработке, – создание генетического теста по выявлению предрасположенности к раннему старению, которым мы занимаемся совместно с нашими коллегами из новосибирского Технопарка. Речь идет о выявлении генетических маркеров, которые позволят оценить потенциальную скорость накопления возрастных изменений у конкретного человека.
Сейчас уже известны подобные генетические программы для косметологов, с помощью которых можно определить потенциальную скорость старения кожи. Но, как все понимают, это лишь верхушка айсберга. Ведь стареет не только кожа, но и мозговые структуры, мышцы, кровеносные сосуды. Стареют клетки и белки… Процесс старения – это генеральная финишная линия развития организма.
Первый внятный совместный продукт, посвященный генетическим аспектам старения, должен появиться уже к концу текущего года. Мы надеемся, что в результате этой работы любой желающий сможет узнать свои шансы стать здоровым долгожителем, а в случае выявления предрасположенности к раннему старению – получить персональные рекомендации по продлению активной, полноценной жизни.
Литература
Кох Н. В., Слепухина А. А., Лифшиц Г. И. Артериальная гипертония: молекулярно-генетические и фармакологические подходы // Фармакогенетика и фармакогеномика. 2015. № 2. С. 4—8.
Кох Н. В. и др. Сравнение эмпирического и фармакогенетического подхода в оценке антикоагулянтной терапии // Кардиология. 2015. Т. 55. № 4. С. 57—60.
Кох Н. В., Лифшиц Г. И., Воронина Е. Н. Возможности анализа полиморфизма генов липидного обмена для выявления факторов риска атеросклероза // Российский кардиологический журнал. 2014. Т. 114. № 10. С. 53—57.
Лифшиц Г. И., Филипенко М. Л. Лечить не болезнь, а больного // НАУКА из первых рук. 2012. Т. 44. № 2. С. 58—65.
Лифшиц Г. И., Новикова Я. В. Терапия: персональная доза // НАУКА из первых рук. 2010. Т. 32. № 2. С. 97—99.