Терапия: персональная доза
Большинство препаратов, попадая в наш организм, претерпевают ряд сложных химических преобразований, в результате чего реализуется их лечебный эффект. Затем лекарство переходит в неактивную форму и выводится из организма. Понимание механизмов влияния генетических, внешних и индивидуальных факторов на систему биотрансформации лекарств позволит индивидуально подходить к назначению препаратов, что уменьшит количество побочных воздействий, и добиться максимального эффекта от медикаментозной терапии
Процесс биотрансформации и выведения лекарственных средств из организма осуществляется через сложную систему механизмов, тесно связанных между собой. Он проходит в несколько стадий: всасывание в кишечнике, изменение структуры препаратов, образование конъюгатов с веществами эндогенного (внутреннего) происхождения и, наконец, сама экскреция – выведение.
Эффективность и безопасность лекарственных средств зависит от характера функционирования участников всех этапов биотрансформации, которыми являются белковые образования, служащие различными ферментами и модуляторами. И если в структуре гена, кодирующего определенный белок, который принимает участие в метаболизме лекарства, имеется мутация, то строение и функция этого белка могут также измениться. Соответственно, изменения могу коснуться и активности процессов биотрансформации лекарственного средства на той или иной стадии.
Такие «измененные» гены называют полиморфными. Полиморфный ген представлен в популяции несколькими разновидностями (аллелями), что обусловливает разнообразие признаков внутри вида. Медикам важно учитывать то, что различия в строении ферментов, участвующих в биотрансформации препарата, а также белков-мишеней могут стать причиной значительных различий в реакции разных пациентов на один и тот же препарат, включая развитие осложнений.
Фармакогенетика – наука, изучающая влияние наследственности на индивидуальную чувствительность к лекарственным средстам. Эта дисциплина позволяет выявить определенные гены, кодирующие белки, которые участвуют в метаболическом пути лекарства. Однако изучение одних лишь генетических особенностей метаболизма не может дать полного представления о процессах биотрансформации лекарственного средства в организме.
В решении этой проблемы способна помочь метаболомика, целью которой в данном случае является систематизация, идентификация и количественное определение всех метаболитов лекарственного препарата в отдельно взятом организме или биологическом образце. Этих данные позволяют выявить взаимосвязи между различными генетическими вариантами (полиморфизмами) и скоростью метаболизма лекарства. При этом значимые генетические полиморфизмы становятся маркерами, которые уже могут использовать клиницисты для подбора лекарственной терапии при различных заболеваниях.
Все дело в дозе
Наиболее активно технологии фармакогенетики и метаболомики применяют для изучения биотрансформации непрямых антикоагулянтов – группы лекарственных препаратов, которые понижают свертываемость крови и препятствуют тромбообразованию. Важный представитель этой фармакологической группы – варфарин, антагонист витамина К – необходимого звена в процессе свертывания крови. Этот препарат жизненно необходим пациентам с нарушениями сердечного ритма, с венозными тромбозами, тромбоэмболиями различной локализации, а также после кардиохирургических операций.
Варфарин назначают на длительный срок, иногда пожизненно, при этом прием лекарства чреват развитием различных осложнений, в первую очередь малых и больших кровотечений. Кроме того, в некоторых случаях эффект от лечения варфарином отсутствует, несмотря на увеличение дозы препарата.
Известен ряд факторов, влияющих на степень безопасности и эффективность лечения данным препаратом. К факторам первой группы относятся пол, возраст, масса тела пациента, особенности его питания (например, вегетарианство), сопутствующие заболевания, прием других лекарственных препаратов и т. п. Однако по имеющимся на сегодня данным, эти факторы лишь на 17 % объясняют взаимосвязь вариабельности терапевтической дозы варфарина и индивидуального ответа пациента (Caldwell et al., 2008). Что касается роли факторов второй группы – генетических, то оценить ее не так-то просто: для этого нужны данные о метаболизме варфарина в организме пациента.
Под угрозой осложнений
Как и многие другие лекарственные средства, варфарин метаболизируется в печени. В виде неактивных метаболитов он выводится вместе с желчью и попадает в желудочно-кишечный тракт, где всасывается в кровь и затем выводится с мочой.
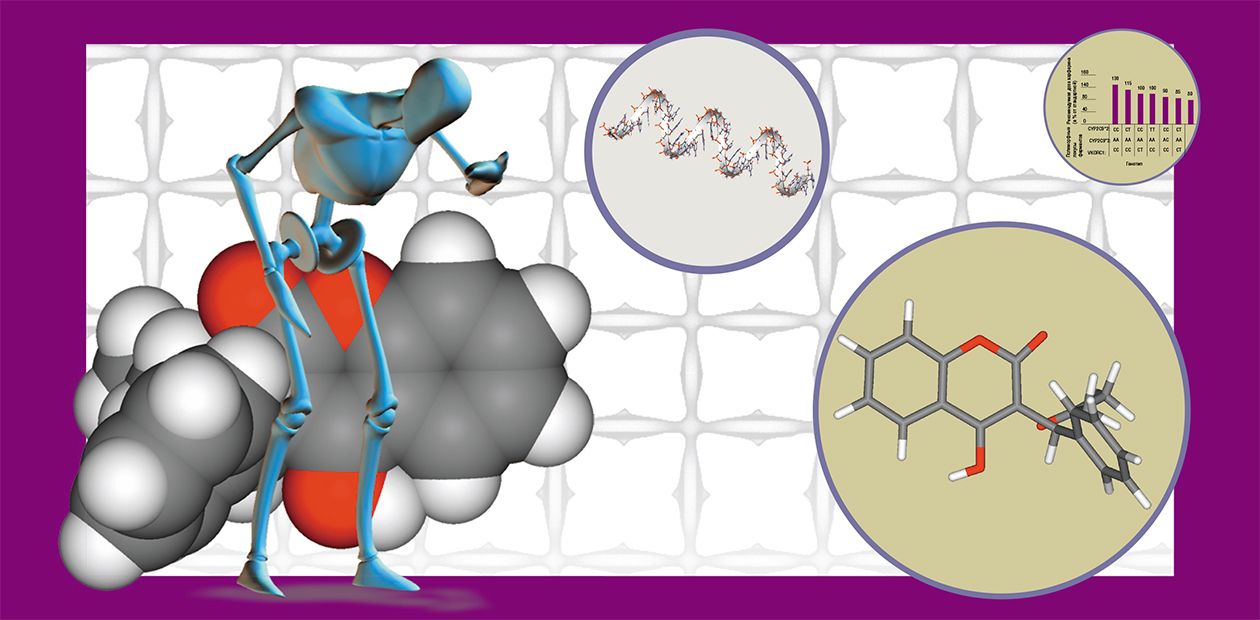
Основными белками-ферментами, участвующими в процессе метаболизма варфарина, являются печеночные цитохромы системы Р 450 (CYP). Сам препарат состоит из двух изомеров (молекул одинакового химического состава, но отличающихся пространственным расположением атомов), при этом терапевтическая активность s-варфарина намного выше. Основным катализатором метаболизма для него является цитохром CYP2C9: изменение в его активности может значительно влиять на чувствительность пациента к лечению варфарином.
Кроме того, индивидуальная чувствительность к варфарину зависит еще от одного небольшого белка, локализованного внутри печеночных клеток – витамин-К эпоксид редуктазного комплекса VKORC1. Его функция заключается в реактивации витамина К, и именно этот белок и является мишенью для варфарина при осуществлении последним лекарственного воздействия.
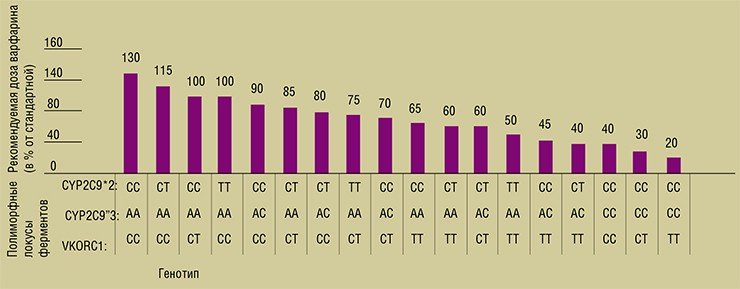
Для генов, кодирующих данные белки, известны полиморфизмы, влияющие на скорость метаболизма варфарина и степень чувствительности к нему пациентов. Как правило, изменения в этих генах сопровождаются снижением скорости утилизации лекарства из организма, следовательно, соответствующий рост его концентрации в плазме крови может приводить к возникновению кровотечений.
Рецепт для генов
В Институте химической биологии и фундаментальной медицины СО РАН и Центре новых медицинских технологий в Академгородке с 2008 г. проводится широкое изучение фармакогенетики и фармакокинетики варфарина у пациентов, вынужденных длительное время принимать антикоагулянты. Из лейкоцитов пациентов выделяют ДНК, в которой определяют полиморфные варианты генов CYP2C9 и VKORC1. На основании полученных данных можно с уверенностью утверждать, что более половины обследованных являются носителями измененных генов. Это означает, что дозу варфарина для таких пациентов необходимо корректировать относительно стандартно рекомендуемой. Здесь возникает проблема дозировки.
Чтобы точно определить необходимую дозу препарата для конкретного пациента, сначала нужно с помощью масс-спектрометрии определить уровни метаболитов лекарства в организме через равные промежутки времени после приема, а затем построить фармакокинетическую кривую. Однако подобное исследование – сложная и трудоемкая задача, выполняемая обычно только в научно-исследовательских целях.
Доступными методами для использования в повседневной медицинской практике могут служить генетические тесты. Для этого необходимо изучить количественные взаимоотношения между генетическими полиморфизмами и скоростью метаболизма варфарина на группе пациентов с различными генетическими вариациями нужного гена. Подобные исследования проводились ранее среди европейской популяции, но в Сибири они проводятся впервые.
Результаты работы по варфарину с привлечением методов метаболомики и генетики служат примером наиболее эффективного и перспективного подхода в медицине – персонализированного. Подобные исследования помогают подобрать дозу лекарства пациенту с учетом его генетических особенностей, что дает возможность сократить количество побочных эффектов, оптимизировать и минимизировать фармакотерапию и снизить расходы на лечение, а значит, существенно улучшить качество жизни людей.
Литература
Семиголовский Н. Ю. Непрямые антикоагулянты в кардиологии (впечатления о применении варфарина) // Трудный пациент. 2007. № 3. С. 31—37.
Сироткина О.В., Вавилова Т.В., Кадинская М.И. и др. Определение индивидуальной чувствительности к варфарину методом молекулярно-генетического анализа гена цитохрома Р450 2С9: Руководство для врачей. СПб.: Издательство СПбГМУ, 2006.
Сычев Д. А. Лечить не болезнь, а больного, или фармакогенетика в действии // Вестн. Моск. городского науч. о-ва терапевтов. 2007. № 14.
Gardiner S. J., Begg E. J. Pharmacogenetics, drug-metabolizing enzymes, and clinical practice // Pharmacol. Rev. 2006. V. 58. P. 521—590.
Wysowski D. K., Nourjah P., Swartz L. Bleeding complications with warfarin use: a prevalent adverse effect resulting in regulatory action // Arch. Intern. Med. 2007. V. 167. P. 1414—1419.