Мелатонин – при диабете и ожирении показан
Верно говорят: мал золотник, да дорог. Гормон мелатонин представляет собой очень маленькую молекулу и синтезируется в организме из аминокислоты триптофана в очень малом количестве. Однако эта древнейшая сигнальная молекула принимает участие в регуляции множества сторон жизнедеятельности нашего организма, включая сон, кровообращение, работу эндокринной и лимфатической систем и иммунитет. Последние исследования говорят о том, что мелатонин можно успешно использовать не только в качестве снотворного средства при нарушениях суточного ритма, но и для лечения ожирения и сахарного диабета 2-го типа. И одним из самых перспективных препаратов для этой цели может стать инновационная разработка новосибирского НИИ клинической и экспериментальной лимфологии
Французский философ и ученый Рене Декарт недаром называл этот маленький, размером с горошину орган головного мозга «седалищем души». Функции эпифиза еще во многом остаются загадкой, хотя мы знаем, что эта эндокринная железа действительно влияет на эмоциональное, психическое состояние человека и животного.
Функциональная роль эпифиза связана с его основным гормоном – мелатонином. Эпифизарный мелатонин поступает в кровь и разносится по всему организму, где участвует в регуляции самых разных биологических процессов. К примеру, он индуцирует процессы торможения в центральной нервной системе и способствует наступлению сна, регулирует суточный ритм температуры тела, активирует иммунную систему, повышает функцию антиоксидантной системы организма и т. д. Снижение продукции мелатонина с возрастом может быть фактором повышенного окислительного повреждения клеток у пожилых людей, что способствует развитию таких «возрастных» заболеваний, как болезни Альцгеймера и Паркинсона (Peschke, 2008).
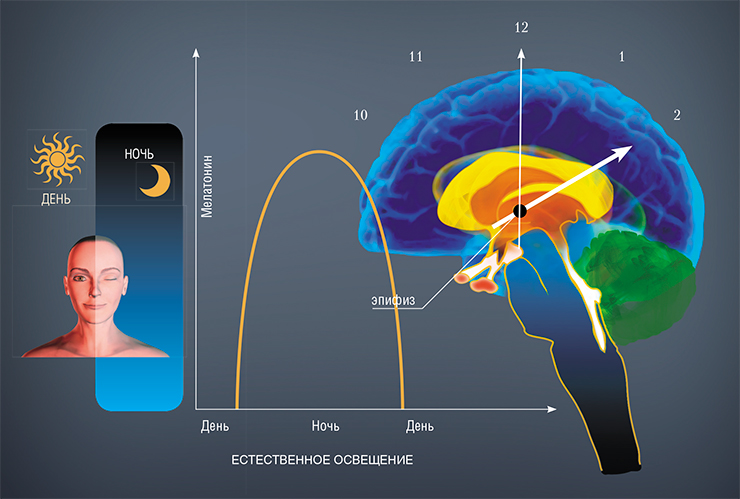
До 80 % мелатонина в сыворотке крови имеет эпифизарное происхождение. Но мелатонин вырабатывается не только в эпифизе, но и в периферических тканях, в первую очередь в желудочно-кишечном тракте, включая кишечник, поджелудочную железу и печень. Так, в слизистой оболочке толстой кишки синтезируется в 400 раз больше мелатонина, чем в эпифизе, при этом его содержание регулируется в основном приемом и характером пищи, а не чередованием света и темноты (Мелатонин: перспективы применения в клинике, 2012).
Биологическое действие внеэпифизарного мелатонина реализуется, по-видимому, непосредственно там, где он синтезируется. Учитывая необыкновенную распространенность гормона в организме, можно предполагать, что он играет ключевую роль в местной координации клеточных функций. Такое широкое распространение мелатонина отражает его важную роль как межклеточного нейроэндокринного регулятора и координатора многих сложных и взаимосвязанных биологических процессов
Важная особенность эпифизарного мелатонина заключается в том, что его продукция имеет суточный ритм, достигая пика в темное время суток, а в светлое синтез мелатонина блокируется.
Так как самым очевидным эффектом этого «ночного» гормона является его снотворное действие, препараты мелатонина часто назначают при различных нарушениях сна из-за рассогласования биологических ритмов. Последнее случается в самых разных жизненных ситуациях: при сменной и ночной работе, дальних перелетах, работе в Арктике и Антарктике, неправильном режиме дня, а также сне при включенном свете. Кроме того, так как мелатонин обладает свойствами антидепрессанта, его назначают для улучшения настроения.
Но в этой статье мы остановимся на гораздо менее известных эффектах мелатонина, связанных с его влиянием на углеводный и жировой обмен, лимфатическую и иммунную системы, процессы жизнедеятельности и смерти клеток.
Регулятор обмена веществ
 В инструкциях по применению мелатонина среди противопоказаний указано такое заболевание, как сахарный диабет. Но это верно лишь для диабета 1-го типа, аутоиммунного заболевания, при котором дефицит гормона инсулина возникает на фоне повышенного синтеза мелатонина в эпифизе (Коненков и др., 2013). Однако далеко не все знают, что применение мелатонина показано в случае широко распространенного сахарного диабета 2-го типа, связанного с нарушением чувствительности клеток к инсулину и дисфункцией бета-клеток поджелудочной железы, вырабатывающих этот гормон.
В инструкциях по применению мелатонина среди противопоказаний указано такое заболевание, как сахарный диабет. Но это верно лишь для диабета 1-го типа, аутоиммунного заболевания, при котором дефицит гормона инсулина возникает на фоне повышенного синтеза мелатонина в эпифизе (Коненков и др., 2013). Однако далеко не все знают, что применение мелатонина показано в случае широко распространенного сахарного диабета 2-го типа, связанного с нарушением чувствительности клеток к инсулину и дисфункцией бета-клеток поджелудочной железы, вырабатывающих этот гормон.
Мелатонин воздействует на функцию этих клеток через мембранные рецепторы (MT1 и МТ2), которые также имеются у клеток в некоторых структурах мозга и во многих периферических органах. Таким образом происходит синхронизация производства инсулина и чередования светлого и темного времени суток. Кроме того, установлено, что мелатонин способствует воспроизводству бета-клеток в поджелудочной железе, улучшает чувствительность тканей к инсулину и уменьшает окислительный стресс в экспериментальных моделях сахарного диабета 2-го типа (Peschke et al., 2006; Peschke, 2008).
Мелатонин воздействует на клетки через мембранные рецепторы МТ1 и МТ2, активность которых снижается при ночном освещении, а также через рецепторы в ядре клеток, влияя таким образом на уровень активации ряда генов, в том числе в органах, определяющих суточные ритмы организма (эпифизе, сетчатке глаза, гипоталамусе и др.). И сам гормон, и его метаболиты (6-гидроксимелатонин) могут также беспрепятственно проникать в цитоплазму клетки через клеточную мембрану, где связывают свободные радикалы кислорода, защищая от оксидативного повреждения макромолекулы (белки, жиры, ядерную и митохондриальную ДНК) во всех субклеточных структурах (Carpentieri et al. 2012; Bouroutzika et al. 2020)Таким образом, этот гормон играет важную роль в регуляции уровня глюкозы в крови и секреции инсулина, поэтому неудивительно, что и сахарный диабет 2-го типа, и сопутствующие ему патологии – алиментарное (первичное) ожирение и метаболический синдром – развиваются на фоне нарушения/снижения продукции мелатонина (BährI et al., 2012; Hardeland, 2012). У больных сахарным диабетом 2-го типа нормальный циркадный ритм мелатонина, как правило, отсутствует, а его уровень в целом понижен.
Причина подобных нарушений может быть различной. С одной стороны, возникновение такой патологии может быть связано с определенными вариантами генов, кодирующими рецепторы мелатонина, из-за чего чувствительность к этому гормону падает (Tosini et al., 2014). С другой стороны, сахарный диабет 2-го типа часто начинается на фоне рассогласования суточных ритмов из-за ночного освещения, что приводит к частичной или полной блокаде синтеза мелатонина в эпифизе.
Сейчас во всем мире, особенно в развитых странах, наблюдается буквально эпидемия сахарного диабета 2-го типа и связанных с ним сердечно-сосудистых осложнений, смертность от которых выше, чем от онкологических болезней. Согласно данным Минздрава РФ, риск развития диабета сегодня угрожает каждому десятому россиянину. И мелатонин может занять свое место в ряду эффективных фармакологических средств для борьбы с подобными нарушениями.
Печень Прометея
Нашим первым шагом по выяснению механизмов действия мелатонина при сахарном диабете 2-го типа стало изучение его влияния на печень, которая играет основную роль в поддержании постоянства внутренней среды организма. Именно печень выполняет функции «метаболического мозга», координируя потоки разнообразных соединений и адаптируя метаболизм к текущим потребностям нашего организма, и она же является одним из главных органов-мишеней для любых метаболических нарушений.
Развитие метаболического синдрома и сахарного диабета 2-го типа также сопровождается нарушениями функций печени. Мы изучили эти изменения на модельном объекте – лабораторных мышах линии BKS.Cg-Dock7m+/+Leprdb/J, генетически предрасположенных к развитию ожирения и диабета, для которых характерен пониженный уровень секреции эпифизарного мелатонина.
У взрослых животных этой линии были обнаружены отчетливые структурные перестройки, свидетельствующие о развитии у них неалкогольной жировой болезни печени. Микроскопические исследования выявили накопление в клетках печени жира и гликогена («животного крахмала»), нарушение клеточных структур, ответственных за синтез белка, и митохондрий – «клеточных электростанций», а также застой лимфы, особенно у самцов (Michurina et al., 2016).
На последнее стоит обратить особое внимание, так как лимфатическая система, сосуды которой пронизывают все органы и ткани, – это тот дренаж, по которому идет отток жидкости из межклеточного пространства. С этой жидкостью из ткани выводятся продукты обмена веществ, в том числе токсические. Застой лимфы свидетельствует о значительной нагрузке на эту систему и способствует развитию кислородного голодания тканей печени, что наряду с повреждением митохондрий приводит к усилению программируемой гибели (апоптозу) клеток.
Может ли дополнительный прием мелатонина повлиять на все эти структурные изменения? Известно, что мелатонин улучшает состояние митохондрий (Srinivasan et al., 2011); под регулирующим влиянием этого гормона находятся и транспортные пути для лимфы и лимфоидных клеток. Таким образом, можно обоснованно предположить, что при ожирении и сахарном диабете препараты мелатонина позволят добиться коррекции печеночной патологии.
Мелатонин и иммунная система
Еще одна важнейшая система организма, которая страдает при сахарном диабете 2-го типа, – иммунная. Основными рабочими элементами этой системы являются иммунные клетки (макрофаги, дендритные клетки, различные типы лимфоцитов, включая Т-киллеры), которые образуются и созревают в красном костном мозге и тимусе. Попадая в кровь, такие клетки разносятся по всем органам и тканям, где осуществляют надзор за состоянием внутренней среды организма, уничтожая чужеродные молекулы, патогенные вирусы и бактерии, а также злокачественные клетки.
 В качестве модельного объекта для оценки влияния мелатонина на состояние иммунной системы мы использовали лабораторных крыс с ожирением, которое служит важным фактором риска развития сахарного диабета 2-го типа. Ранее уже было показано, что этот гормон улучшает иммунный статус таких животных, стимулируя дифференцировку лимфоцитов, участвующих в формировании иммунного ответа организма (Arushanian et al., 2006).
В качестве модельного объекта для оценки влияния мелатонина на состояние иммунной системы мы использовали лабораторных крыс с ожирением, которое служит важным фактором риска развития сахарного диабета 2-го типа. Ранее уже было показано, что этот гормон улучшает иммунный статус таких животных, стимулируя дифференцировку лимфоцитов, участвующих в формировании иммунного ответа организма (Arushanian et al., 2006).
В нашем эксперименте крыс содержали на диете, в которую входили продукты с высоким содержанием жира, что привело к увеличению у них массы тела, повышению содержания триглицеридов и общего холестерина в сыворотке крови, а также жира в печени.
Заметно пострадала и иммунная система упитанных животных. В их селезенке изменилась численность иммунных клеток, в том числе понизилось содержание антигенпрезентирующих клеток и активированных лимфоцитов, обеспечивающих быстрый иммунный ответ на конкретные патогены. Количество активированных лимфоцитов упало и в лимфоузлах печени, а в крови увеличилось число лейкоцитов. В лимфоцитах крови изменился баланс активности окислительно-восстановительных ферментов, что говорит о нарушении энергетического обмена и снижении функциональной активности этих клеток.
Инъекции мелатонина животным в течение двух недель привели к нормализации практически всех этих показателей, включая вес тела.
Комплекс М – «продвинутый» мелатонин
Таким образом, все имеющиеся на сегодня данные говорят о том, что, хотя в лечении сахарного диабета 2-го типа и ожирения мелатонин пока не используется, это новое терапевтическое направление имеет полное право на существование. При этом результаты экспериментальных работ в этой области, когда мелатонин применялся в «чистом виде», до сих пор неоднозначны и противоречивы, несмотря на их многочисленность. Может быть, это связано с тем, что мелатонин, введенный путем инъекции или с пищей, быстро выводится из организма, тогда как эпифиз выделяет гормон постепенно, в течение темного времени суток.
В новосибирском НИИ клинической и экспериментальной лимфологии – филиале ФИЦ ИЦиГ СО РАН разработан и синтезирован новый препарат мелатонина – «Комплекс М». Он представляет собой оригинальную композицию из носителя – пористого оксида алюминия с преимущественным размером пор 10–100 нм, кремнийсодержащего полимера полиметилсилоксана, относящегося к силиконовым соединениям, и гормона мелатонина, содержание которого в препарате составляет 0,15 % (Патент № 2015100920 /05(001238) от 11.01.2016).
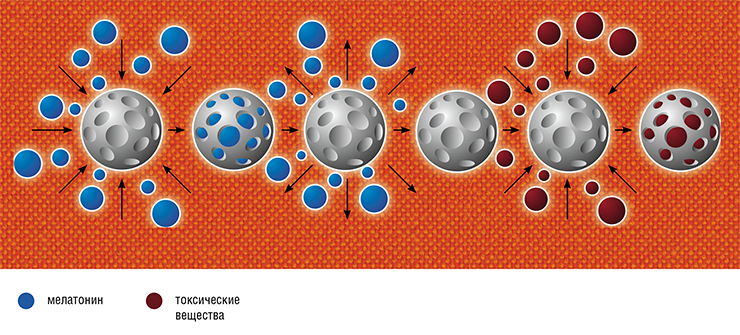
Как известно, сорбенты могут фиксировать на своей поверхности различные молекулы, поэтому сорбционная терапия традиционно применяется для выведения токсических продуктов из организма. Однако ее можно использовать и для целевой доставки лекарственных средств. Сорбент не разрушается при прохождении по желудочно-кишечному тракту, поэтому удерживаемый на поверхности носителя фармацевтический агент выходит из него постепенно, в течение длительного времени (Бородин и др., 2014). Это позволяет избежать передозировки, а также снижает риск побочных эффектов и интоксикаций.
Разработки новых препаратов в НИИКЭЛ базируются на сырье отечественного производства, при котором используются технологии получения безопасных для человека пористых материалов, исключающие применение высоких температур и органических растворителей
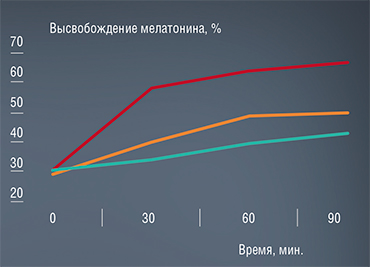
Поверхность пор носителя характеризуется набором как гидрофильных участков за счет матрицы из оксида алюминия, так и гидрофобных за счет полиметилсилоксана. Это создает условия, способствующие многоточечному связыванию на их поверхности различных средне- и высокомолекулярных соединений. Благодаря таким физико-химическим особенностям препарата мелатонин высвобождается из него постепенно, что позволяет добиться эффекта «протезирования» мелатонин-продуцирующей функции эпифиза.
С другой стороны, на пористом носителе могут адсорбироваться различные токсические соединения. Благодаря достаточно высокой сорбционной емкости препарат проявляет детоксицирующий эффект, а также противоотечный за счет регуляции баланса тканевой жидкости.
Во время доклинических испытаний при содержании мышей С57Bl/6J при круглосуточном освещении, которое подавляет синтез мелатонина в эпифизе, были получены обнадеживающие результаты. В этом случае введение «Комплекса М» можно рассматривать как своего рода заместительную терапию.
Так, ежедневное введение водной суспензии «Комплекса М» самцам мышей этой линии уже через неделю привело к значительному увеличению мышечной силы и выносливости животных. В то же время прием обычного мелатонина в аналогичной дозе не оказал такого эффекта. Эти результаты говорят о перспективности применения «Комплекса М» у людей, чья деятельность связана с тяжелыми физическими нагрузками: спортсменов, военнослужащих, вахтовиков и др.
Также выяснилось, что препарат благоприятно влияет на состояние селезенки – многофункционального органа, выполняющего кроветворные, иммунные и обменные функции, а также депонирующего кровь. Усиление кровотока в венозных сосудах и ряд структурных изменений этого органа в ответ на прием «Комплекса М» свидетельствуют об активации его иммунных функций. Кроме того, введение этого препарата повышало корково-мозговой индекс тимуса (вилочковой железы), что может указывать на стимуляцию дифференцировки T-клеток иммунной системы.
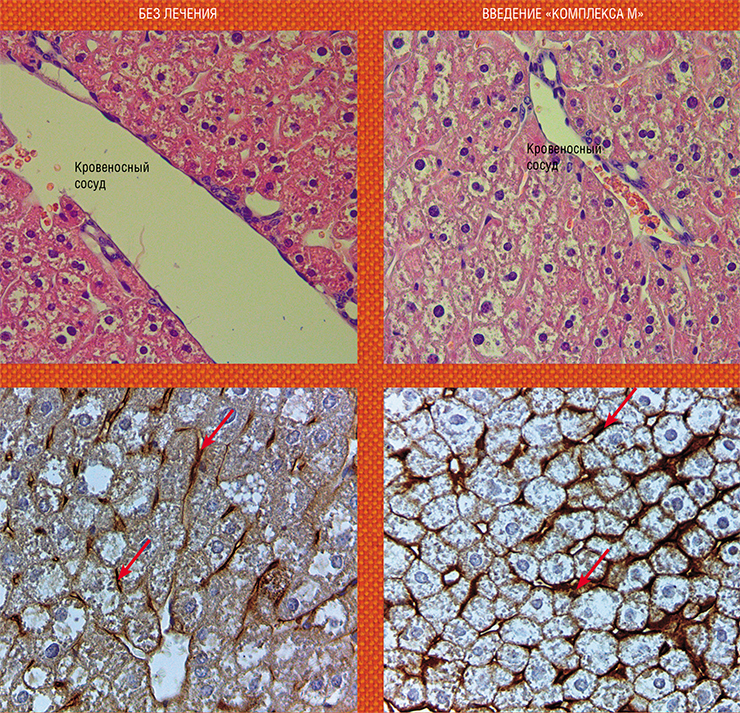
Успешным оказалось и лечение мышей с генетически детерминированным развитием ожирения и сахарного диабета, о которых говорилось выше. Внутрижелудочное введение «Комплекса М» взрослым особям привело к нормализации у них структурно-функциональных показателей циркуляции крови и лимфы, а также к улучшению состояния клеток печени и усилению регенеративного потенциала этого органа.
Наглядной иллюстрацией положительного действия «Комплекса М» на таких животных могут служить молекулярные особенности запрограммированной гибели клеток печени. Как уже говорилось выше, плохое снабжение клеток кислородом у мышей этой линии негативно сказывается на структуре и функциях митохондрий – основных внутриклеточных участников апоптоза. Изучение ультраструктурного состояния этих внутриклеточных органелл и динамики продукции двух белков, регулирующих клеточное «самоубийство», – антиапоптотического Bcl‑2 и проапоптотического Bad – показало, что у взрослых самцов активируется так называемая митохондриальная «ветвь» апоптоза. Введение «Комплекса М» привело к преобладанию «защитника» Bcl‑2 над «клеточным убийцей» Bad, что говорит о восстановлении клеточной защиты в печени (Мичурина 2019; Michurina et al., 2016).
Таким образом, можно утверждать, что как сам мелатонин, так и новый препарат мелатонина «Комплекс М» обладают мощными антиоксидантными, иммуномодулирующими, лимфотропными, гепатопротекторными и гиполипидемическими свойствами. И в этом смысле они являются перспективными средствами для коррекции нарушений липидного обмена и иммунного статуса при ожирении и нарушении светового режима, а также в комплексном лечении сахарного диабета 2-го типа.
При этом «Комплекс М» обладает более выраженным терапевтическим действием по сравнению с обычными препаратами мелатонина. Он не только безопасен, но и проявляет детоксикационные свойства за счет пористой структуры носителя.
Препарат, разработанный новосибирскими специалистами, успешно прошел лабораторно-экспериментальные испытания. Однако трудно сказать, когда он появится на прилавках аптек. Официальные доклинические и клинические испытания нового лекарственного средства – процедура всегда дорогостоящая, а в мире к тому же идет пандемия нового вирусного заболевания. И это, кстати, лишний повод напомнить о роли мелатонина в поддержании здоровья больных сахарным диабетом 2-го типа, так как такие пациенты входят в группу риска.
Литература
Арушанян Э. Б., Наумов С. С. Противовоспалительные возможности мелатонина // Клиническая медицина. 2013. Т. 91, № 7. С. 18–22.
Арушанян Э. Б., Щетинин Е. В. Мелатонин как универсальный модулятор любых патологических процессов // Патологическая физиология и экспериментальная терапия. 2016. Т. 60, № 1. С. 79–88.
Бородин Ю. И., Труфакин В. А., Мичурина С. В., Шурлыгина А. В. Структурно-временная организация печени, лимфатической, иммунной, эндокринной систем при нарушении светового режима и введении мелатонина. Новосибирск: Изд. дом «Манускрипт», 2012. 208 с.
Коненков В. И. КлимонтовВ. В., Мичурина С. В и др. Мелатонин при сахарном диабете: от патофизиологии к перспективам лечения // Сахарный диабет. 2013. № 2. С. 11–16.
Мичурина С. В., Васендин С. В., Ищенко Ю. И. Физиологические и биологические эффекты мелатонина: некоторые итоги и перспективы изучения // Российский физиологический журнал им. И.М. Сеченова. 2018. Т. 104, № 3. С. 257–271.
Мичурина С.В., Летягин А. Ю., Шурлыгина А. В. и др. Гепато-иммуно-эпифизарная ось межсистемных взаимодействий. Мелатонин и структурно-функциональные изменения печени и иммунной системы при ожирении и сахарном диабете 2 типа. Новосибирск: Изд. дом «Манускрипт», 2019. 304 с.