Аптамеры – продвинутое ДНК-оружие против SARS-CoV-2
В своей борьбе с COVID-19 человечество сейчас больше полагается на профилактическое «оружие» – прививки, а среди терапевтических средств – на препараты нейтрализующих человеческих антител, блокирующих вирусным частицам доступ в клетки. Но коронавирус постоянно мутирует, что снижает эффективность иммунотерапии, сами антитела отличаются низкой биодоступностью и высокой стоимостью, а их разработка и производство требует времени. Однако альтернатива иммунным белкам существует, и недавно с помощью инновационного метода исследователи разработали новый подход к созданию устойчивых молекул – ДНК-аптамеров, для борьбы с существующими и будущими штаммами SARS-CoV-2 и других патогенных вирусов
Нуклеиновые кислоты – ДНК и РНК – пользуются широкой известностью как носители наследственной информации, обеспечивающие преемственность всего живого. Однако далеко не все знают, что их функции в клетке, как и потенциальные возможности, много шире – эти молекулы можно смело назвать «мастерами на все руки».
В частности, оказалось, что РНК, которой первоначально отводилась достаточно скромная роль «посредника» между ДНК и «фабриками белка» (рибосомами), может обладать свойствами фермента. Ранее считалось, что такая способность катализировать протекание химических реакций присуща только белкам. Структуры РНК, действующие подобно ферментам, назвали рибозимами по аналогии с энзимами, белками-катализаторами. Особенно широко используют рибозимы вирусы и другие простые инфекционные агенты для манипулирования своими РНК. Позднее методами молекулярной селекции были созданы и ДНКзимы, способные расщеплять РНК.
Нуклеиновые кислоты также могут образовывать высокоспецифичные комплексы с белками. Такие искусственные короткие одноцепочечные ДНК и РНК, прочно и избирательно связывающиеся с конкретными молекулярными мишенями, назвали аптамерами (от лат. aptus – подходить, соответствовать). Они имеют огромные перспективы в медицине в качестве ингибиторов различных клеточных белков: ферментов, рецепторов и регуляторов активности генов, а также для диагностических целей.
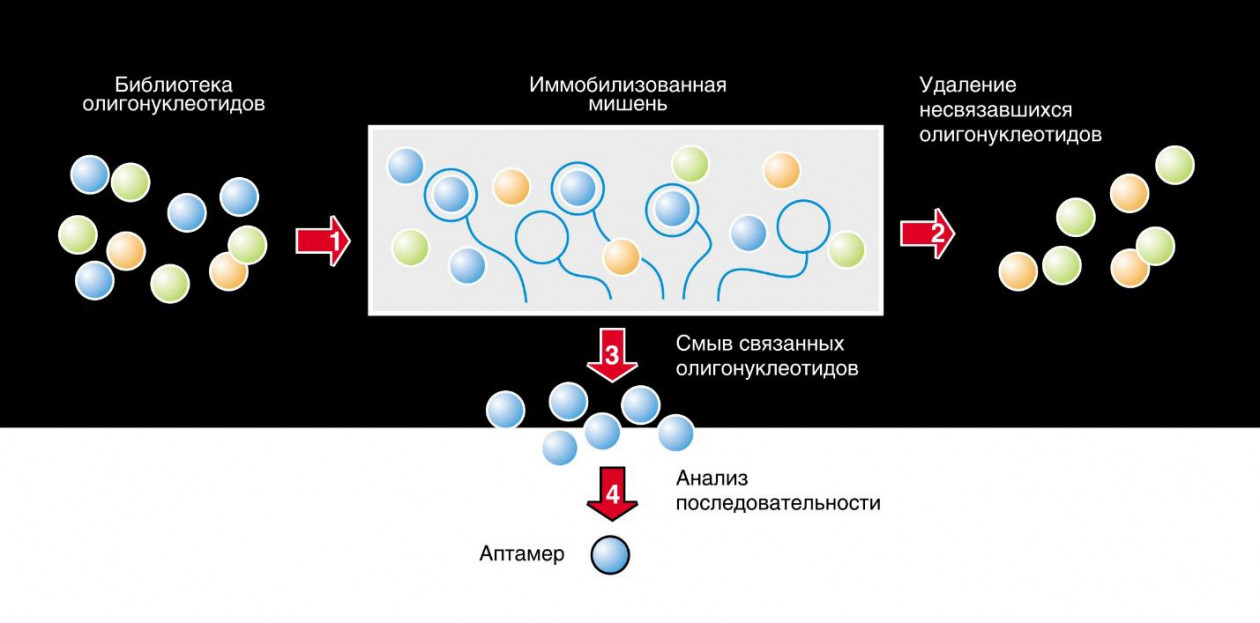
Создание искусственных РНК и ДНК с заданными свойствами стало возможным благодаря появлению метода ПЦР, позволяющего размножать нуклеиновые кислоты в неограниченных количествах (именно этот метод используется при тестировании на коронавирусную инфекцию), а также технологий молекулярной селекции.
Суть технологии в том, что сначала химико-ферментативными методами создаются так называемые молекулярные библиотеки небольших случайных последовательностей нуклеиновых кислот (олигонуклеотидов), содержащие огромное множество разнообразных молекул РНК или ДНК. Затем из этого множества по способности специфично взаимодействовать с целевой молекулой отбирают нужные последовательности и нарабатывают их в необходимом количестве, при этом искомая последовательность может быть представлена в составе библиотеки в единственном числе
Уже сейчас на основе аптамеров разрабатывается целый ряд терапевтических средств, которые могут составить конкуренцию классическим лекарственным препаратам. Примером может служить первый терапевтический аптамер – макуген для лечения заболеваний сетчатки глаза, который уже используется в клинической практике. А множество других препаратов (антикоагулянты, лекарства против аутоиммунных и онкологических заболеваний) проходят клинические испытания.
Аптамеры обладают высоким потенциалом в диагностике, терапии и системах доставки лекарств, но их также можно использовать в качестве противовирусных препаратов во время вспышек инфекций. Сегодня с помощью методов молекулярной селекции можно создать аптамеры, которые смогут блокировать функцию любого белка – например, шиповидного S-белка SARS-CoV-2, который коронавирус использует для проникновения в клетку хозяина. Этот вирусный белок считается основной мишенью при разработке противовирусных препаратов и вакцин, и в случае аптамеров механизм их взаимодействия с мишенью будет аналогичен механизму действия нейтрализующих антител, направленных против этого белка.
Международная группа ученых из России, Финляндии, Италии, Китая, Тайваня и Канады, включая исследователей из Красноярского научного центра СО РАН, разработала новую методику дизайна аптамеров для определения или «обезвреживания» патогенных вирусов. С ее помощью они создали новый ДНК-аптамер длиной в 31 нуклеотид, способный блокировать рецептор-связывающий домен (RBD) шиповидного белка коронавируса.
Традиционно аптамеры выбирают в лабораторных условиях из так называемых молекулярных библиотек, и такая селекция – очень сложный и трудоемкий процесс. Новый подход виртуального дизайна аптамеров SIBDD (Structure and Interaction Based Drug Design, или дизайн лекарств на основе структуры и взаимодействия) позволяет ускорить и повысить результативность этого процесса.
Сначала с помощью методов компьютерного моделирования с использованием суперкомпьютеров ведется поиск последовательностей нуклеотидов, ответственных за селективное присоединение к мишени. Результаты молекулярного дизайна, основанного на виртуальном скрининге готовых библиотек аптамеров ДНК и направленном мутагенезе для увеличения соответствия структуре белка-мишени, постоянно оцениваются с помощью трехмерного молекулярного моделирования процесса взаимодействия мишени и аптамера, а также определения квантово-механической устойчивости полученных комплексов.
Сейчас с помощью новой технологии исследователи создали модифицированный аптамер Apt31, высокоспецифичный к белку-шипа коронавируса. Эффективность соединения Apt31 с мишенью была доказана с использованием трех различных экспериментальных методов, а сейчас проводится экспериментальная проверка его противовирусных свойств.
Новое соединение является многообещающим кандидатом в качестве противовирусного средства, предотвращающего проникновение вируса в клетки человека, а также диагностического – для выявления вирусных частиц в биологических жидкостях.
Вирус SARS-CoV-2 хорошо изучен, однако сама методология SIBDD в принципе ориентирована на случаи с ограниченной информацией о цели, например, для быстрого реагирования на новые опасные инфекции, когда доступ к образцам ограничен. В такой ситуации первоначальный набор аптамеров к молекулярной мишени может быть получен уже на основе данных лишь о первичной структуре (последовательности) белка. Впоследствии этот набор можно улучшать по мере поступления новых экспериментальных данных, а также адаптировать к новым мутациям патогенов.
По мнению одного из авторов работы, д.б.н. А.С. Кичкайло, заведующей лабораторией цифровых управляемых лекарств и тераностики КНЦ СО РАН и руководителя лаборатории биомолекулярных и медицинских технологий Красноярского государственного медицинского университета, «разработанный подход для создания аптамеров может способствовать созданию диагностических и терапевтических средств для других вирусов семейства коронавирусов или их мутировавших вариантов. А учитывая высокую универсальность аптамеров, компьютерный дизайн молекул предлагает многообещающие возможности для разработки диагностических и терапевтических инструментов и для других заболеваний».
В публикации использованы материалы пресс-релиза ФИЦ КНЦ СО РАН