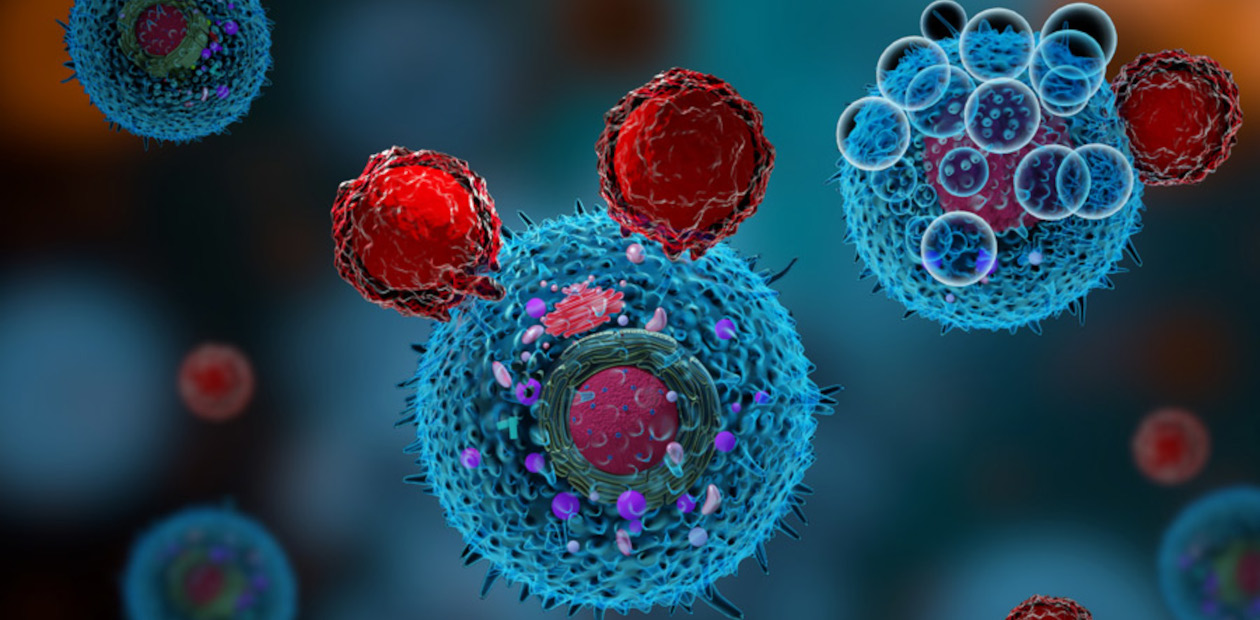
Чтобы выжить, раковые клетки заставляют Т-киллеры «кусаться», а не убивать
Первые попытки рекрутировать на борьбу с раковой опухолью иммунную систему относят к началу прошлого века, а сегодня «иммунотерапия рака» активно используется в практической медицине, хотя ее эффективность пока оставляет желать лучшего. Недавно ученые раскрыли еще один механизм, с помощью которого клетки опухоли могут обходить как естественный иммунный ответ, так и терапевтические стратегии
Иммунная система человека защищает его от как от внешних угроз, таких как патогенные микробы, так и «внутренних», уничтожая поврежденные и переродившиеся собственные клетки организма. Мутации, способные привести к злокачественному перерождению, возникают постоянно, и клетки иммунной системы (Т- и В-лимфоциты, макрофаги, дендритные клетки) обычно с ними успешно справляются.
Но иногда противораковые механизмы дают сбой, в чем не последнюю роль играют сами опухолевые клетки, которые активно «прячутся» от иммунной системы. В частности, эти клетки секретируют разнообразные молекулы, препятствующие их уничтожению цитотоксическими Т-лимфоцитами, которых недаром называют Т-киллерами.
Изучение этих механизмов позволило разработать комплекс терапевтических стратегий, известных как иммунотерапия рака. Самый известный метод – CAR T-терапия, при котором собственные Т-клетки пациента модифицируют «в пробирке», специфически нацеливая их на клетки конкретной опухоли человека, а затем вводят обратно в организм. Однако подводных камней в этом методе лечения много, поскольку механизмы взаимодействия иммунитета и опухоли выяснены лишь частично.
Недавно группа ученых под руководством специалистов из Университета Пенсильвании (США) исследовали, как опухоль стимулирует Т-клеточный трогоцитоз (от греч. trogo – «грызть» или «жевать»).
В норме процесс уничтожения раковых клеток начинается с того, что Т-киллеры распознают находящиеся на поверхности таких клеток специфические молекулы-антигены. Но иногда случается так, что Т-клетка лишь «откусывает» часть клеточной мембраны с опухолевым антигеном и начинает сама презентировать его на своей поверхности.
По причинам, которые не до конца понятны, такая Т-клетка становится менее активной. Более того: она становится «овцой в волчьей шкуре», и другие Т-клетки могут опознать ее как раковую и уничтожить. При этом сама раковая клетка не только не гибнет, но превращается в «невидимую» для других Т-клеток.
Как же раковая клетка «заставляет» Т-клетку трогоцитировать? Как выяснилось, вещества, выделяемые опухолью, вызывают в иммунных клетках повышение продукции белкового фактора транскрипции ATF3, который подавляет продукцию фермента, участвующего в синтезе 25-гидроксихолестерина. А снижение в клетке запасов этих молекул ведет к нарушениям процесса слияния клеточных мембран, что повышает вероятность событий трогоцитоза.
Ученые доказали этот вывод в эксперименте, где к трогоцитирующим Т-клеткам добавили 25-гидроксихолестерин, – процесс «откусывания» мембран остановился. А полное удаление из среды молекул ATF3 предотвращало сам трогоцитоз и восстанавливало способность Т-киллеров убивать клетки опухоли.
Полученные результаты открыли возможность улучшить эффективность иммунотерапии с помощью CAR-Т-клеток. И действительно, когда исследователи при модификации Т-клеток добавили в их геном ген, кодирующий холестерин-25-гидроксилазу, то такие клетки лучше справлялись с опухолью у мышей, служащих животной моделью рака.
Так что хотя трогоцитоз характерен лишь для небольшой части Т-клеток, этот процесс явно недооценивается, когда речь идет о противораковом иммунитете, когда важна каждая опознанная и уничтоженная злокачественная клетка. В будущем этот механизм должен быть детально изучен, что, возможно, позволит не только улучшить эффективность CAR-Т терапии, но и разработать новые иммунотерапевтические стратегии.
Фото: https://researchoutreach.org