Еще один шаг к клеточной терапии сахарного диабета
В основе сахарного диабета 1-го типа лежит аутоиммунное поражение бета-клеток поджелудочной железы, вырабатывающих гормон инсулин. Недавно ученые сделали еще один шаг, чтобы снизить зависимость таких больных от ежедневных инъекций инсулина, – провели очередные клинические испытания экспериментального метода терапии этой болезни с помощью имплантации устройств со стволовыми клетками поджелудочной железы
Сахарный диабет 1-го типа обычно диагностируется уже в детском или подростковом возрасте. Ключевой аспект заболевания – недостаточная выработка гормона инсулина поджелудочной железой. Этот гормон критически важен для углеводного обмена, поэтому человеку требуется ежедневное введение инсулина.
Больных диабетом 1-го типа в мире относительно немного: согласно данным ВОЗ, в 2017 г. их насчитывалось 9 млн человек. Это тяжелое заболевание требует непрерывного контроля за состоянием организма, так как количество введенного инсулина не всегда соответствует потребности в нем, которая меняется и определяется внутренними факторами, работающими по механизму обратной связи.
Обычно тяжелых осложнений болезни удается избежать, однако «неадекватная» на данный момент доза лекарства может привести к опасным для жизни состояниям даже у пациента, тщательно выполняющего все указания врача.
Есть примеры и более физиологичного лечения инсулинозависимого диабета. Это либо трансплантация донорской поджелудочной железы человека, либо внутрипеченочная трансплантация островков Лангерганса, где содержатся бета-клетки, полученные из поджелудочной железы донора. Таким способом примерно в половине случаев можно практически избавиться от инъекций инсулина. Однако нехватка донорского материала и необходимость постоянного приема иммуносупрессоров для предотвращения отторжения трансплантата ограничивает такие вмешательства.
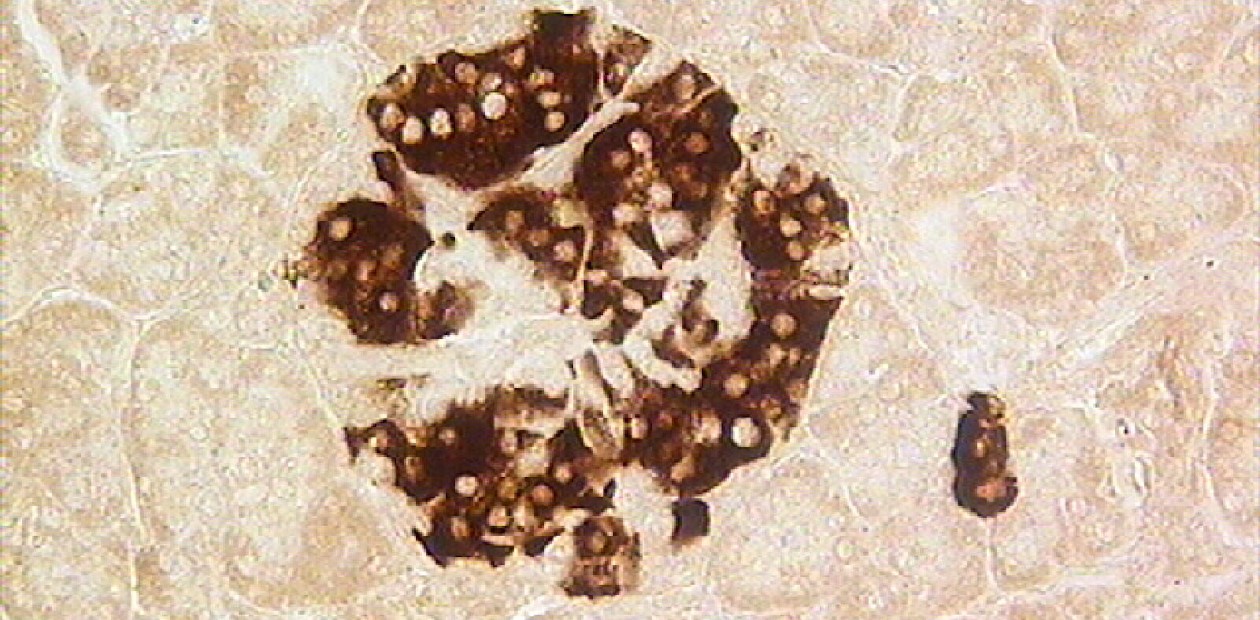
Теоретически проблему можно решить имплантацией бета-клеток, полученных из индуцированных плюрипотентных стволовых клеток донора, которые затем подвергают направленной дифференцировке в клетки поджелудочной железы. Изначальной была идея каким-то образом изолировать пул таких клеток от тканей организма пациента, чтобы защитить как самого реципиента, так и донорские клетки, которым угрожают иммунные клетки больного. Кроме того, в таком случае имплант при необходимости можно легко удалить из организма.
Такой имплант удалось разработать ученым из Университета Британской Колумбии (Канада) и биотехнологической компании ViaCyte (США) на основе культуры эмбриональных стволовых клеток человека CyT49. Устройство, получившее рабочее название VC-02, похоже на кусочек пластыря и помещается под кожу пациента. Предполагается, что содержащиеся в нем бета-клетки обеспечат стабильную, физиологически регулируемую подачу инсулина, по сути воссоздавая функции здоровой поджелудочной железы.
Пару лет назад такие импланты были успешно опробованы, что доказало принципиальную возможность использовать их для производства инсулина в организме человека. В новом исследовании его участникам имплантировали сразу несколько устройств, чтобы увеличить количество вырабатываемого инсулина. А саму конструкцию обновили: благодаря небольшим отверстиям теперь в имплантат могли врастать кровеносные сосуды, что способствует выживаемости клеток.
Две первые фазы клинических испытаний были проведены на площадках Канады, Бельгии и США. Десяти больным было установлено до 10 имплантатов каждому, и в течение года исследователи мониторили их состояние и биохимические маркеры углеводного обмена. Так как имплант потерял герметичность, что открыло доступ в него клеткам иммунной системы реципиента, испытуемые принимали иммуносупрессивную терапию.
Испытания показали, что выработка инсулина и в таком модифицированном варианте пока недостаточна для формирования клинического эффекта. Но по ряду параметров результаты оказались обнадеживающими.
Так, через полгода после имплантации (и до конца испытаний) у четверых больных было отмечено повышение уровня маркеров выработки инсулина. У всех этих людей уровень глюкозы стал ближе к норме, а дополнительные дозы инсулина снизились. Но даже у испытуемого-«рекордсмена» параметры углеводного обмена не дотягивали до уровня, достигаемого внутрипеченочными имплантами поджелудочной железы.
Оказалось, что бета-клетки просто не слишком хорошо выживают в таких условиях, и в дальнейшем следует повышать их жизнеспособность, а не увеличивать число имплантов у больного. При этом выяснилось, что в более успешных случаях бета-клетки собирались в кластеры вокруг проросших в имплант капилляров, образуя подобие характерной секреторной единицы. Ученые предполагают, что разница в эффективности имплантов может быть обусловлена разным «рисунком» перфораций их стенок. Очевидно, в будущих исследованиях ученые будут тестировать разный рисунок отверстий, нащупывая оптимальный.
Фото: https://www.freepik.com, https://www.medicalgraphics.de, https://en.wikipedia.org