Митохондриальный стресс: все, что не убивает живую клетку, делает ее сильнее
В древности и во времена средневековья люди, опасавшиеся отравителей, практиковали длительный прием ядовитых веществ в малых дозах. Как позже выяснилось, феномен привыкания организма к действию токсинов существует – сейчас его называют «гормезисом». Суть его в том, что в ответ на действие относительно безвредных количеств заведомо опасных веществ или небольших «доз» других стрессоров в организме формируются адаптивные стресс-реакции, позволяющие потом без последствий переносить более серьезную дозу. И хотя времена Борджиа прошли, сам гормезис сегодня можно рассматривать как потенциальный механизм, способный повышать стрессоустойчивость клеток и целого организма
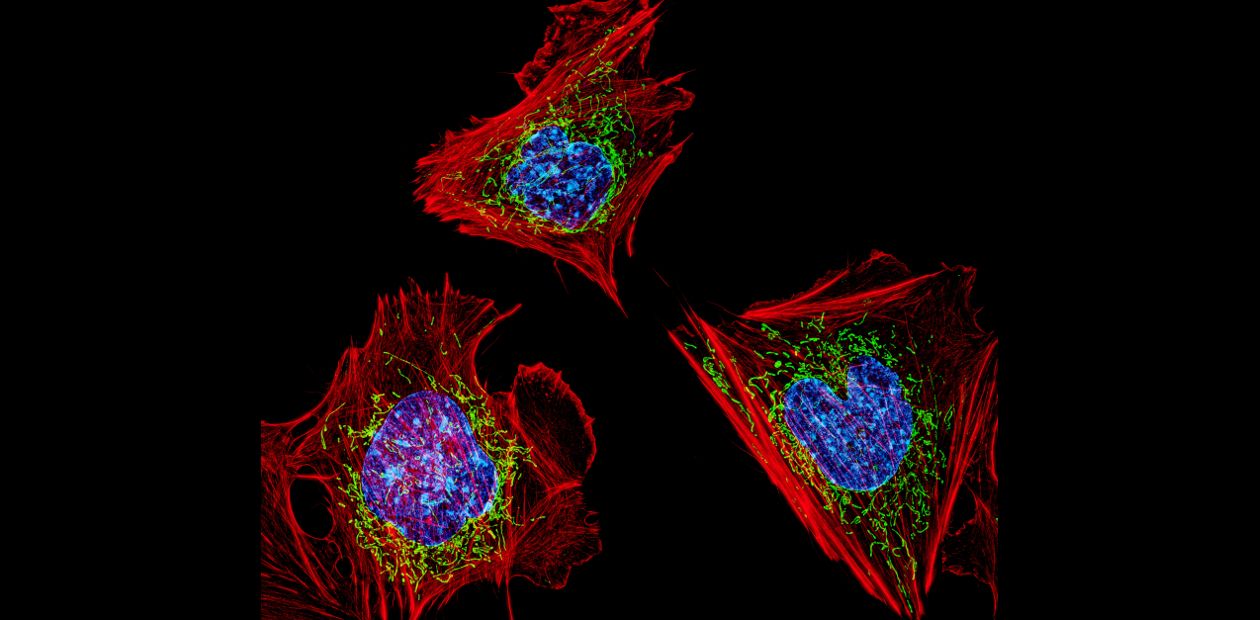
Митохондрии – это клеточные органеллы, производящие молекулы АТФ, которые служат универсальным источником энергии для всех биохимических процессов организма. Но хотя роль митохондрий как «энергетических станций» клеток чрезвычайно важна, их функции оказались много шире. Например, существует митохондриальный путь запуска процесса апоптоза («клеточного самоубийства»), который активируется в результате действия на клетку различных повреждающих факторов. Также есть мнение, что «здоровье» митохондрий влияет на ход процессов старения, и сегодня на него пытаются влиять, например, с помощью изменений в диете.
Так называемый митохондриальный стресс, который развивается в результате неправильного свертывания митохондриальных белков либо воздействия токсинов и других негативных факторов, может запускать цепочки молекулярных событий, приводящие к изменению работы различных генов. Мягкий митохондриальный стресс позволяет реализовать эффект гормезиса: клетки «обучаются» адаптивно реагировать на стрессовые условия, в результате чего, к примеру, у червей нематод увеличивается продолжительность жизни.
Сами митохондрии, кстати сказать, являются основным внутриклеточным источником активных форм кислорода, которые можно «погасить» с помощью веществ-антиоксидантов. Но если баланс между продукцией активных форм кислорода и их разрушением будет нарушен, разовьется окислительный стресс. Еще несколько лет назад считалось, что окислительный стресс – это всегда плохо, поэтому антиоксиданты рассматривались чуть ли не как панацея от множества заболеваний. Однако, как выяснилось, умеренный окислительный стресс может быть полезен организму.
Недавно ученые под руководством специалистов из Института биологических исследований Солка (США) исследовали, как влияет на организм митохондриальный окислительный стресс, «пережитый» во время эмбрионального развития.
Используя способность малых РНК регулировать активность генов, они создали генетически модифицированных мышей, у которых можно обратимо отключать фермент супероксиддисмутазу 2 с помощью антибиотика доксорубицина. Этот антиоксидантный фермент, располагающийся внутри митохондрий, превращает высокореактивный супероксидный радикал в перекись водорода и кислород. Животные, у которых супероксиддисмутаза 2 «выключена» полностью, гибнут через несколько дней после рождения.
В эксперименте ученые «выключали» фермент только на несколько дней во время эмбрионального развития животных, а потом «включали» обратно. Все экспериментальные мыши успешно появились на свет, выросли и, на первый взгляд, практически не отличались от контрольных.
Различия проявились при исследовании образцов печеночной ткани. Оказалось, что в клетках мышей, переживших во время внутриутробного развития митохондриальный стресс, уровень антиоксидантов был существенно выше, а уровень супероксидного радикала – ниже. У них была выше даже численность самих митохондрий, чем у мышей, не испытавших стресса.
Сходные результаты были получены и на культурах клеток мышей: клетки, которые подвергали стрессу, приобретали к нему большую устойчивость. Также ученые «вычислили» молекулярные механизмы, изменения в работе которых влияют на стрессоустойчивость клеток.
Эту конкретную работу вряд ли можно назвать прорывной, но она служит несомненным шагом на пути к пониманию, можно ли использовать эффект гормезиса для предотвращения развития возраст-зависимых заболеваний и даже увеличения самой продолжительности жизни.
Фото: https://www.flickr.com
Подготовила Мария Перепечаева