Таинственные абзимы
Слова «иммунитет» и «антитело», как и понятие «фермент», безусловно, знакомы всем. Но многие ли слышали об уникальных белках, производимых нашей иммунной системой, которые умеют катализировать самые разные реакции? Сопровождая неизлечимые аутоиммунные заболевания, эти многофункциональные молекулы могут быть нашими врагами, но могут стать и настоящей находкой для биотехнологии и медицины...
Что такое иммунитет? Этим модным ныне словом обозначают один из главных механизмов защиты человека от вредных факторов окружающей среды (immunis на латыни означает «чистый, свободный от чего-либо»). Из множества защитных систем многоклеточных организмов к иммунитету относятся лишь те, в которых участвуют особые клетки-лимфоциты. Уникальная черта этих клеток — способность распознавать огромное (около1018!) количество разнообразных потенциально вредных объектов (бактерий, вирусов, чужеродных молекул и т. д.), включая и такие, с которыми жизнь за миллиарды лет существования на Земле еще не сталкивалась.
Лимфоцитарный иммунитет — достаточно новое эволюционное приобретение: им обладают не более полутора процентов видов многоклеточных организмов, начиная с челюстных рыб. Представители этих видов оставляют сравнительно малочисленное потомство, поэтому выживание каждой особи существенно для сохранения вида. О важности иммунитета в нашей жизни говорит хотя бы тот факт, что каждая десятая клетка тела взрослого человека — лимфоцит!
Лимфоцитарным иммунитетом обладают лишь те виды многоклеточных организмов, у которых выживание каждой особи имеет значение для сохранения видаИммунитет предназначен для защиты не только от внешних «интервентов» разного типа и калибра, но и от собственных поврежденных клеток. Любая молекула, которая, попав в организм, может вызвать иммунный ответ, называется антигеном.
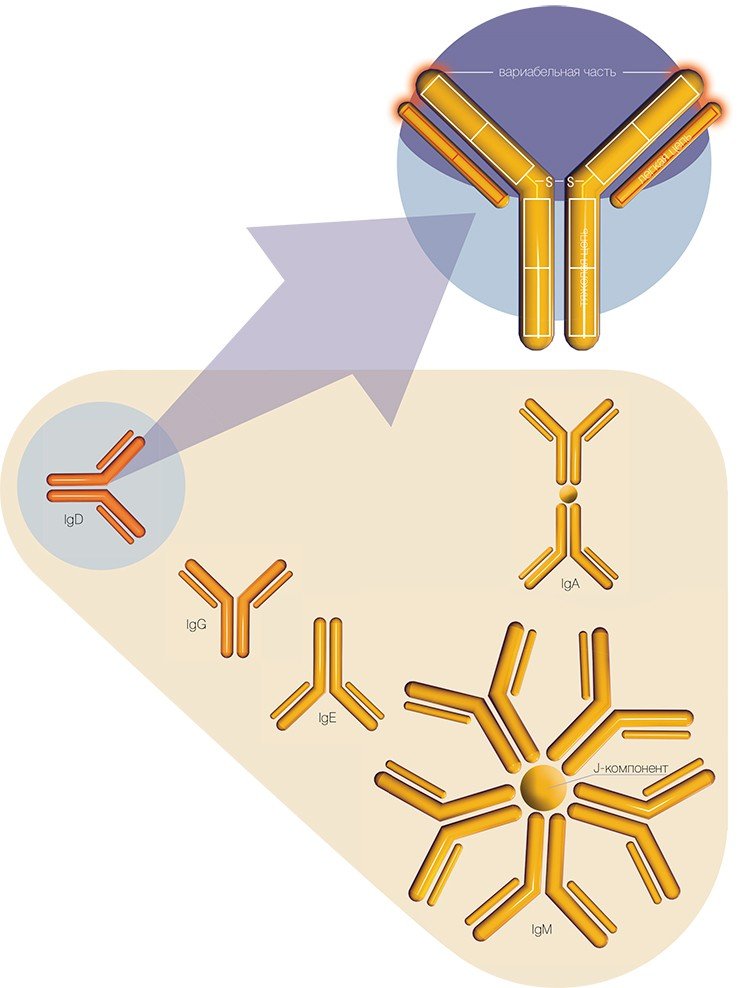
Вообще иммунитет бывает двух типов. Иммунная система первого типа обеспечивает так называемый гуморальный ответ. При нем в организме в ответ на попадание антигена вырабатываются специальные белковые молекулы — антитела (или иммуноглобулины, Ig), которые узнают антиген, связывают и нейтрализуют его. Иммунный ответ второго типа называется клеточным — его обеспечивают специальные клетки, лимфоциты-киллеры, распознающие чужеродные антигены после их связывания с особыми собственными клетками организма.
Родословная лимфоцита
Рассмотрим иммунную систему первого типа. Антитела, образующиеся при гуморальном ответе, вырабатываются особым классом лимфоцитов — В-лимфоцитами. Как и другие клетки крови, они происходят из стволовой, т. е. недифференцированной, кроветворной клетки костного мозга в результате многоступенчатой специализации. Зрелые неиммунные лимфоциты (их называют наивными, потому что они еще не специализированы для выполнения определенных функций) циркулируют через кровь между различными органами и тканями организма.
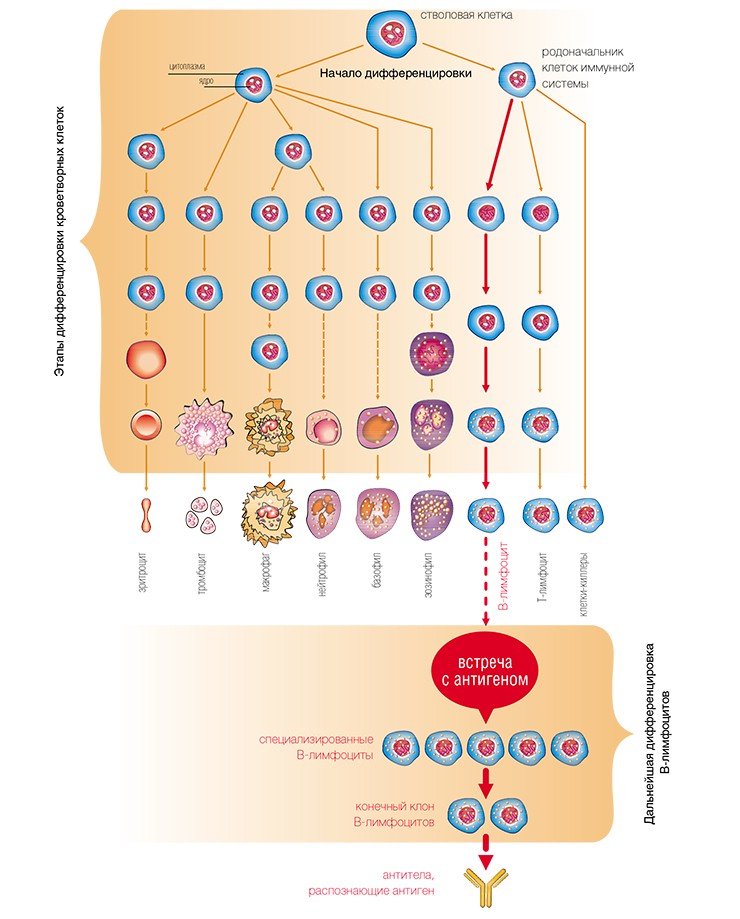
В процессе дифференцировки лимфоцитов формируется все огромное разнообразие генетических кодов для вариабельных (различающихся у разных лимфоцитов) участков будущих антител, ответственных за распознавание и связываение антигена: в каждом лимфоците происходит своя, уникальная перегруппировка генетического материала, унаследованного от стволовой клетки.
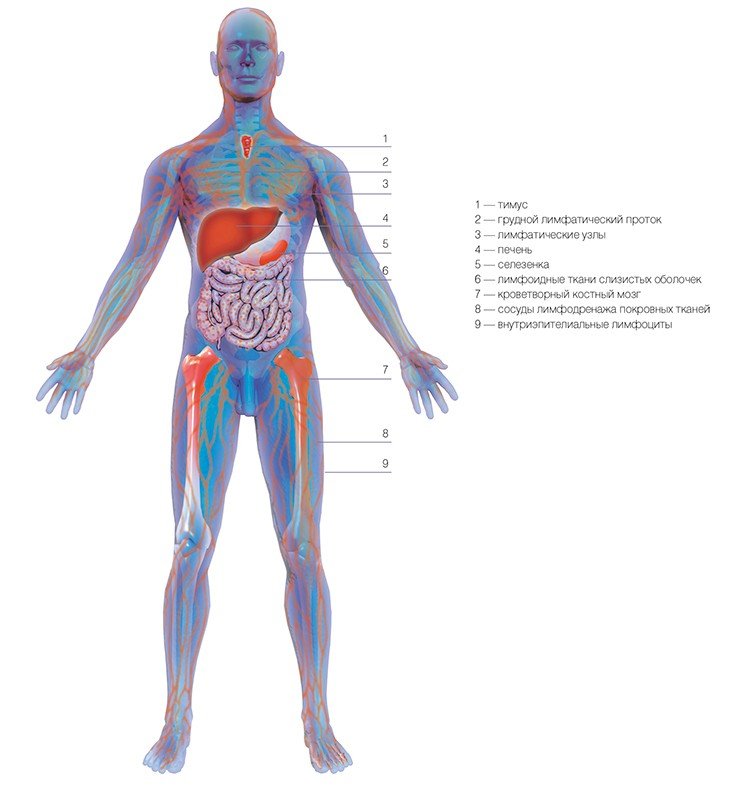
В периферических лимфоидных органах (лимфатических узлах, селезенке, лимфоидной ткани органов пищеварительной, дыхательной и мочеполовой систем) наивные лимфоциты «знакомятся» с разными антигенами. После встречи с конкретным антигеном те лимфоциты, которые смогли его распознать, начинают активно размножаться и дополнительно перестраивать структуру генов, кодирующих вариабельную часть антител. Так получается новый клон B-лимфоцитов, синтезирующих антитела, способные высоко специфично связываться и, в конечном итоге, разрушать именно этот антиген.
На один и тот же антиген иммунная система может в принципе выработать до 106 вариантов дифференцированных В-лимфоцитов (и соответствующих им вариантов антител), но реально их меньше. В конечном итоге от этого множества остается лишь несколько процентов клеток, вырабатывающих наиболее продуктивно работающие антитела. А изначальное перепроизводство — необходимая плата за точность и эффективность будущего иммунного ответа.
Кстати, если наивный лимфоцит случайно «познакомится» не с чужеродным антигеном, а с белком своего организма, то он обычно погибает. Именно поэтому наш иммунитет не убивает нас самих.
Сбои в иммунитете
Способность отличать «свое» от «чужого» — важнейшее свойство иммунной системы. К сожалению, в этой системе могут случаться сбои, когда в организме начинают активно размножаться «запрещенные» клоны лимфоцитов — настоящие «подрывные элементы», производящие антитела против молекул собственного организма. Несколько десятков аутоиммунных заболеваний, возникающих в результате таких сбоев, представляют собой важную медицинскую проблему современного общества — ведь ими страдает множество людей, в том числе молодого и среднего возраста.
Как возникают эти болезни? Установить причину в каждом конкретном случае затруднительно, но известно, что этому способствуют генетическая предрасположенность, гормональный дисбаланс, неблагоприятные условия окружающей среды (радиация, инфекции, токсины, нездоровый климат и т. д.) и другие факторы. В результате таких воздействий в организме накапливаются аутоантитела — антитела к собственным антигенам. В случае всем известной бронхиальной астмы антигеном служит небольшой белок — вазоактивный интестинальный пептид; при рассеянном склерозе — белки миелина (белково-липидной оболочки нервных волокон). Аутоиммунными реакциями сопровождаются и некоторые вирусные заболевания, как, например, СПИД и вирусный гепатит, при которых нарушается иммунитет.
Принято считать, что антигены — это в основном белки и полисахариды, однако такие свойства могут проявлять и другие молекулы, в том числе и главный носитель наследственной информации — ДНК. Интересно, что в крови больных многими аутоиммунными заболеваниями повышена концентрация и самой ДНК, и антител к ней. Особенно в этом плане примечательна системная красная волчанка.
Долгое время бытовало мнение, что антитела могут нейтрализовать антигены только путем прочного связывания с ними с последующим выведением из организма. Но оказалось, что это не единственно возможный способ. И вот здесь нужно сделать отступление и рассказать о других белках — ферментах.
Новая наука — абзимология
Из школьного курса все знают, что ферменты — это белки, катализирующие самые разные химические реакции. Молекула фермента связывается с молекулой вещества (субстрата) и превращает его в другое вещество (продукт); протекает эта реакция в специальном участке фермента — активном центре.
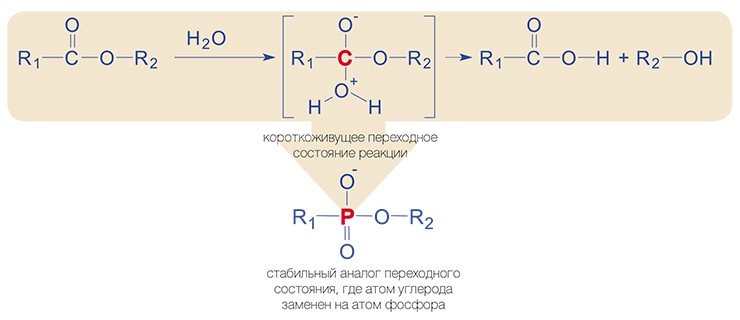
На заре биохимии считали, что структура активного центра фермента точно соответствует структуре субстрата — подходит к нему, как ключ к замку. Однако в 1940-х годах будущий нобелевский лауреат Л. Полинг показал, что активные центры комплементарны не субстратам и продуктам, но некоторым промежуточным структурам — так называемым переходным состояниям вещества, которые образуются в ходе реакции.
Из своей гипотезы Полинг сделал довольно интересный вывод: если бы иммунная система умела вырабатывать антитела против переходных состояний, то такие антитела обладали бы свойствами ферментов. Как мы видели, иммунная система производит невообразимое количество самых разных антител, и среди них всегда найдется такое, которое будет соответствовать даже самому экзотическому антигену.
Однако схему Полинга в чистом виде невозможно реализовать технически — переходные состояния существуют очень короткое время. Поэтому позже В. Дженкс предложил использовать стабильные ¬молекулы с похожей структурой, чтобы получить антитела на них.
Эта идея получила первое экспериментальное подтверждение в 1986 г. Такие антитела, обладающие каталитической активностью, назвали абзимами (от английских слов antibody enzyme — антитело-фермент). Известные на сегодня абзимы катализируют более ста различных реакций, причем даже такие, для которых природных ферментов не существует.
Можно считать, что возникла целая новая отрасль биохимии — абзимология. В числе ее последних достижений — создание новых лекарственных средств, например, абзимов, расщепляющих наркотики в крови. Открываются перспективы получения новых белковых катализаторов с самыми разнообразными свойствами для научных исследований, и, что немаловажно, для биотехнологии и медицины.
Но этими замечательными достижениями история абзимологии не исчерпывается: успешные эксперименты по дизайну разнообразных искусственных абзимов стимулировали новый виток изучения антител в организме, в результате чего были открыты природные абзимы.
Природные абзимы
Первые природные абзимы, обнаруженные американской группой С. Паула в крови больных бронхиальной астмой, не только эффективно связывали вазоактивный интестинальный пептид, но и катализировали его гидролиз (разложение водой). Вскоре после этого московские ученые под руководством А. Г. Габибова выделили из крови больных системной красной волчанкой антитела, гидролизующие ДНК.
Затем в лаборатории ферментов репарации НИБХ СО РАН автором этой статьи был открыт целый ряд природных антител, которые могут расщеплять ДНК, РНК, АТФ, белки и полисахариды. Такие абзимы есть в крови больных системной красной волчанкой, аутоиммунным тиреоидитом, полиартритом, рассеянным склерозом, вирусным гепатитом и СПИДом, но отсутствуют в крови здоровых доноров, а также больных другими, не аутоиммунными заболеваниями.
Как появляются абзимы у аутоиммунных больных? При этих заболеваниях, как известно, активно идет гибель клеток, из-за чего в крови повышаются концентрации всех клеточных компонентов (белков, ДНК и т. д.), а также самых разных их комплексов. Поэтому абзимы могут нарабатываться двумя путями. Во-первых, они могут возникать как антитела непосредственно против продуктов клеточного распада — собственных антигенов, структура которых, когда они находится в комплексе с другими компонентами крови, имитирует структуру переходного состояния реакции.
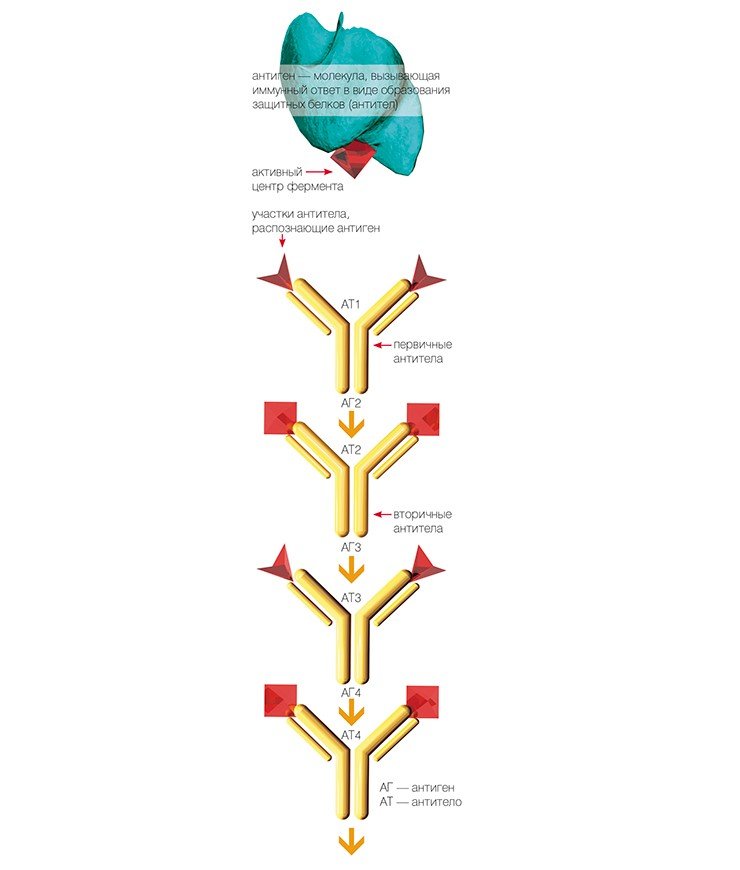
Второй путь сложнее. Согласно теории нобелевского лауреата Н. Эрне, против какого-либо антигена в организме сначала образуются первичные (идиотипические) антитела, которые, будучи сами белками, тоже могут играть роль антигенов, против которых могут образоваться вторичные (антиидиотипические) антитела и т. д. Как и исходный фермент, все антитела более высокого порядка могут проявлять каталитическую активность. По данным новосибирских ученых, в крови больных аутоиммунными заболеваниями обычно находится «коктейль» из абзимов с разными свойствами, образовавшихся разными путями.
Истории болезней
Появление абзимов часто является самым ранним признаком развития аутоиммунных процессов, поэтому тестирование их активности является исключительно перспективным подходом как для ранней диагностики, так и для предсказания обострения хронически текущей болезни и оценки эффективности лечения теми или иными препаратами.
Рассеянный склероз, например, обычно удается распознать только на поздних стадиях, когда в мозге больных возникают характерные бляшки, обнаруживаемые с помощью томографии. Наиболее обоснованная теория возникновения этой болезни отводит главную роль аутоиммунным воспалительным процессам, ведущим к нарушению передачи нервных импульсов. У больных рассеянным склерозом нами обнаружены антитела, которые разрушают основной белок миелина. С помощью анализа на активность этих абзимов можно обнаружить заболевание на ранней стадии.
Общего рецепта для лечения аутоиммунных заболеваний пока нет: сейчас можно продолжительное время поддерживать жизнь такого больного, но вылечить его еще никому не удавалось — скорее всего, потому, что причина этих болезней до сих пор точно неизвестна. Многие данные говорят за то, что развитие аутоиммунных заболеваний связано с нарушениями в скорости роста и дифференцировки стволовых клеток костного мозга.
В нашей лаборатории ведутся исследования на лабораторных мышах особой линии, у которых спонтанно развивается болезнь, аналогичная системной красной волчанке человека. Еще до появления каких-либо внеш¬них симптомов у этих животных заметно меняется характер деления и специализации стволовых клеток. На этой стадии болезни абзимы в крови уже можно «увидеть». Остальные параметры, по которым обычно ставится диагноз, меняются гораздо позже, при переходе предболезни в патологию.
Еще одно наше исследование, которое можно назвать успешным, связано с аутоиммунным тиреоидитом — наиболее часто встречающимся заболеванием щитовидной железы. Известно, что антитела таких больных гидролизуют белок тиреоглобулин, из которого образуется гормон тироксин. Кроме того, у 65 % больных аутоиммунным тиреоидитом были обнаружены антитела с ДНК-гидролизующей активностью, уровень которой коррелировал с диагностическими показателями, стандартными для этой патологии.
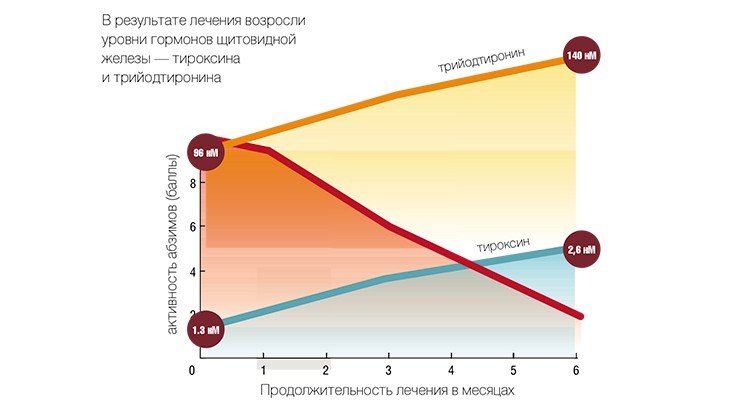
Таких пациентов обычно лечат тироксином, однако это дает лишь временное улучшение, не влияя на глубину протекания самих аутоиммунных процессов. Мы предложили группе из тридцати пациентов экспериментальное лечение плаквенилом. Этот препарат долгие годы использовали в борьбе с малярией, а потом случайно обнаружили, что он эффективно подавляет многие аутоиммунные реакции. При лечении плаквенилом уровень ДНК-гидролизующих абзимов в крови пациентов стал резко снижаться, одновременно и другие показатели также стали приходить в норму: в крови уменьшилась концентрация тиреоглобулина и антител к этому белку, а концентрации тироидных гормонов восстановились практически до нормы (при том, что гормональная терапия не проводилась). В результате у больных нормализовалась функция щитовидной железы, улучшилось общее состояние.
Абзимы — враги и друзья
Абзимы, вероятно, играют отрицательную роль и при других аутоиммунных болезнях, помимо рассеянного склероза и тиреоидита. Например, иммунизация мышей абзимами, гидролизующими вазоактивный интестинальный пептид, провоцирует у них астму, так как разрушение этого белкового гормона приводит к затруднению дыхания.
Абзимы из крови больных системной красной волчанкой, гидролизующие ДНК, оказались цитотоксичными, т. е. тормозящими рост клеток. Такой же способностью обладают некоторые белки-цитокины — природные регуляторы роста многих клеток (один из таких белков, фактор некроза опухолей, очень важен для предохранения организма от рака). При этом цитотоксичность абзимов иногда была даже выше, чем у самих цитокинов. В отличие от обычных антител, такие абзимы каким-то образом могут проникать в ядро клетки через все мембраны, связываться с ДНК, расщеплять ее и таким образом приводить клетку к гибели. Есть основания считать, что появление абзимов на ранних стадиях аутоиммунных заболеваний может стимулировать дальнейшее развитие болезни.
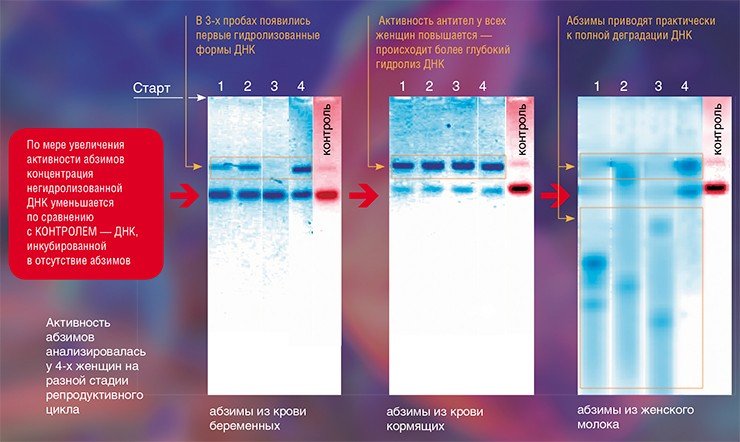
Но абзимы оказались не только врагами: в 1990-х годах новосибирские ученые совершенно неожиданно в изобилии обнаружили абзимы в крови совершенно здоровых людей, а именно — беременных женщин. Более того, оказалось, после родов эти абзимы попадают в материнское молоко!
Почему это происходит? Дело в том, что особенно¬стью реорганизации иммунной системы беременной женщины является включение у нее своеобразной иммунной «памяти», в которой во время беременности аккумулируется информация о всех вредных факторах окружающей среды. В случае млекопитающих это приводит к тому, что в результате иммунизации будущей матери различными антигенами за 1—3 месяца (но не более) до появления потомства ее молоко будет содержать антитела к этим антигенам в очень больших количествах. При этом не важны ни путь попадания антигена в организм матери (через кровь или с пищей), ни его природа (будь это компоненты пищи, белки бактерий или вирусов).
Иммунные процессы с началом лактации запускаются в соответствии с информацией, накопленной в иммунной «памяти», чтобы грудное молоко содержало все антитела, необходимые для защиты новорожденного. Это обеспечивает последнему пассивный иммунитет, поскольку его собственная иммунная система начинает активно развиваться лишь в возрасте 4—6 месяцев.
Молоко рожениц оказалось на редкость богатым источником абзимов, гидролизующих ДНК и РНК, полисахариды, молочный белок казеин и другие вещества. Каталитическая активность этих антител оказалась еще выше, чем у антител из крови больных аутоиммунными заболеваниями. В грудном молоке присутствуют и уникальные абзимы, катализирующие не разрушение субстратов, а их модификацию: они могут фосфорилировать липиды, белки и полисахариды — прикреплять к определенным их частям остаток фосфата.

Абзимы молока, очевидно, играют положительную роль, заключающуюся в усилении защитного действия пассивного иммунитета за счет гидролиза и модификации чужеродных молекул вирусов, бактерий, компонентов пищи и т. д. И здесь мы можем отметить следующий интересный факт: все указывает на то, что беременность стимулирует у женщин процессы, очень похожие на те, что наблюдаются у больных аутоиммунными заболеваниями.
Однако в женском организме они заканчиваются с окончанием лактации, а у больных носят хронический характер. Ответ на вопрос, каким образом у женщин происходит выключение в нужный момент потенциально опасных аутоиммунных реакций, может дать ключ к лечению до сих пор неизлечимых аутоиммунных болезней.
Перекуем мечи на орала
Абзимология — наука молодая, и проблем перед ней стоит много. Пожалуй, самая фундаментальная из них следующая: образуют ли абзимы млекопитающих резервную систему ферментов, работающую в экстремальных ситуациях с активностью, которой нет у обычных ферментов, или это все-таки побочный продукт работы иммунной системы?
Материнское молоко содержит все антитела, необходимые для защиты новорожденного, в том числе и абзимыВ любом случае скрытый потенциал организма в производстве разнообразных абзимов, бесспорно, велик. И когда в 2005 г. в издательстве Wiley-VCH вышла первая в мире монография, посвященная каталитическим антителам, то вступлением к ней стали известные слова пророка Исайи: «Перекуем мечи на орала», очень уместные в данном случае.
Кто знает, может быть, дальнейшее изучение этих необычных многофункциональных белков действительно приведет к новым удивительным открытиям в медицине и фармакологии, и наши вчерашние «враги» превратятся в особо эффективные лекарства нового поколения? Кто знает — ведь история абзимологии только начинается…