Биочипы: диагноз — дело техники!
Что такое биочипы? Этим модным словом сегодня называют миниатюрные приборы для определения специфических взаимодействий биологических макромолекул. Зондами в таких чипах могут служить нуклеиновые и рибонуклеиновые кислоты (в том числе фрагменты геномной ДНК), белки и другие молекулы. За короткое время биологические микрочипы выделились в самостоятельную область анализа, имеющую массу приложений: от практических — в медицине, фармакологии, экологии, судебно-медицинской экспертизе до фундаментальных — в области молекулярной биологии и молекулярной эволюции...
Точнее всего сущность биочипов определяет их английское название — microarrays, — что означает «организованное размещение молекул на специальном носителе-платформе». В качестве платформы чаще всего используют пластинку из стекла или пластика (а иногда и из других материалов, например из кремния). В этом смысле чипы биологические близки к чипам электронным, которые изготовляются на кремниевых пластинах.
 Поскольку величина микрочипа, как правило, мала, — в его английском названии присутствует элемент micro. Тем не менее, несмотря на размер биочипа, на его площади можно разместить огромное количество различных молекул-зондов. После взаимодействия чипа с тестируемыми молекулами, информация, содержащаяся на этой площади, считывается с помощью специального устройства.
Поскольку величина микрочипа, как правило, мала, — в его английском названии присутствует элемент micro. Тем не менее, несмотря на размер биочипа, на его площади можно разместить огромное количество различных молекул-зондов. После взаимодействия чипа с тестируемыми молекулами, информация, содержащаяся на этой площади, считывается с помощью специального устройства.
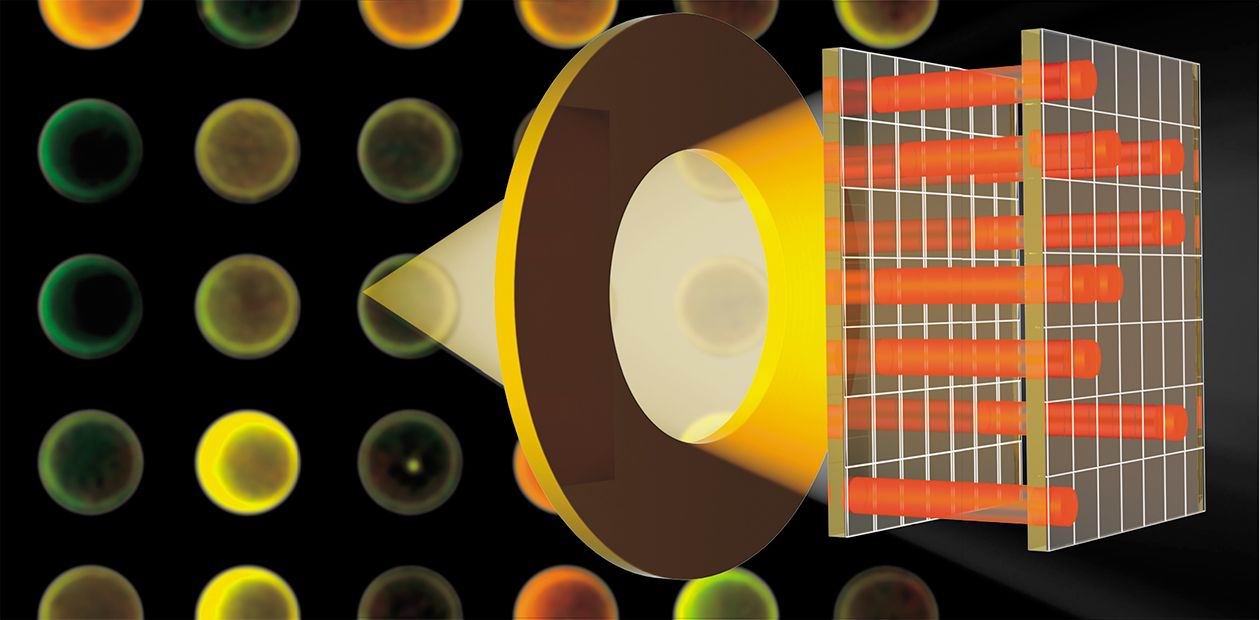
Микрочиповая диагностика основана на установлении факта так называемого лиганд-рецепторного взаимодействия. Один из взаимодействующих партеров — лиганд, или рецептор, — иммобилизуется на небольшой, но строго определенной, поверхности микрочипа, которую называют спот. (Поверхность микрочипа в ряде случаев может быть структурирована, например, микроячейками (нанопланшеты) или микроэлектродами.)
Каждый спот состоит из идентичных молекул. При анализе исследуемый образец наносится на микрочип, а затем фиксируется факт его взаимодействия с молекулами, содержащимися в определенных спотах микрочипа. Результатом этого взаимодействия является характерная модель (паттерн) взаимодействия образца с микрочипом.
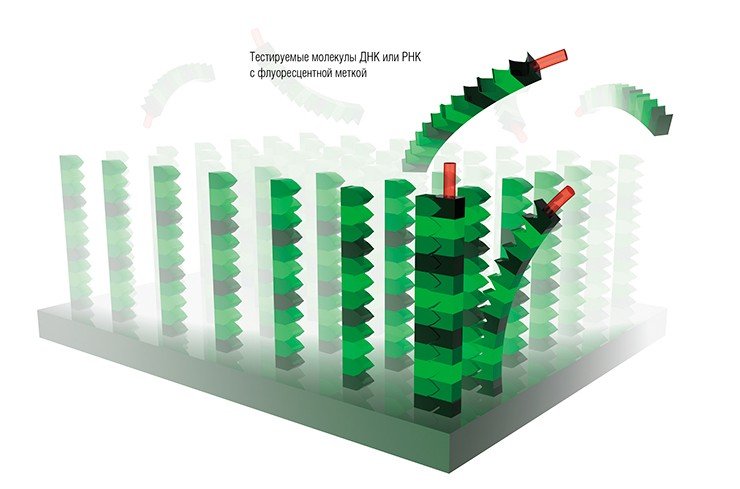
Нередко для фиксирования факта взаимодействия рецептора с лигандом используется флуоресценция. Для этого еще до инкубации с микрочипом анализируемый образец метится флуоресцентной меткой. После инкубации микрочип сканируется лазерным сканером, чтобы можно было получить картину распределения интенсивности флуоресценции на его поверхности. Подобным образом выявляются споты, молекулы-зонды которых вступили в реакцию с молекулами исследуемого образца.
Если условия молекулярной комплементарности, необходимые для возникновения соответствий между иммобилизованными молекулярными зондами и мечеными анализируемыми молекулами в растворе, являются подходящими, то образующиеся комплексы будут наиболее термодинамически устойчивы. В результате при определенных температурах этих комплексов будет больше, чем тех, которые образованы с нарушением условий комплементарности, и им будет отвечать более сильный сигнал флуоресценции.
Изучаем профили... экспрессии
Наиболее разработанной на сегодняшний день можно назвать технологию олигонуклеотидных* биочипов, массовое применение среди которых получили так называемые экспрессионные чипы.
Чтобы понять принцип их работы, обратимся к рассмотрению регуляции жизнедеятельности наших клеток. Процессами внутреннего метаболизма клеток, их делением и дифференцировкой управляет сложная сеть молекулярных взаимодействий, которая и определяет уровень экспрессии (функционирования) различных генов. Показателем последней служит концентрация соответствующей матричной РНК (мРНК), которая синтезируется на ДНК — носителе наследственной информации. Динамика изменения концентрации определенной мРНК указывает на включение или выключение конкретного гена, а значительные отклонения этого показателя от нормы могут свидетельствовать о наличии различных заболеваний.
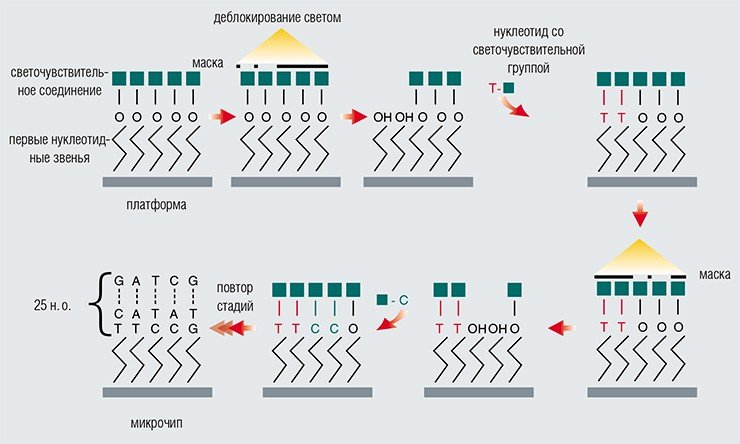
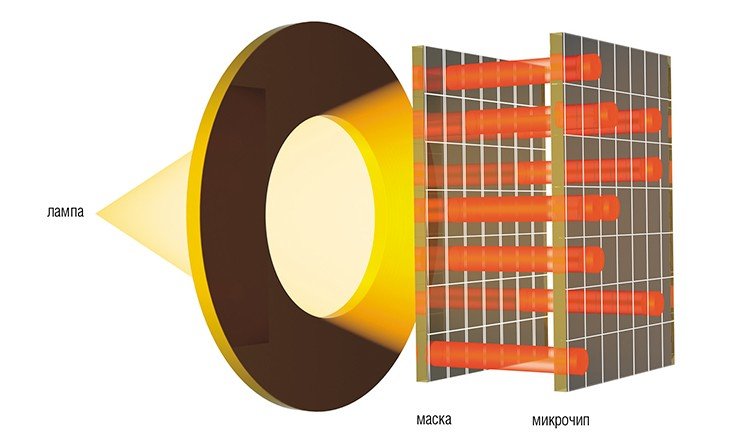
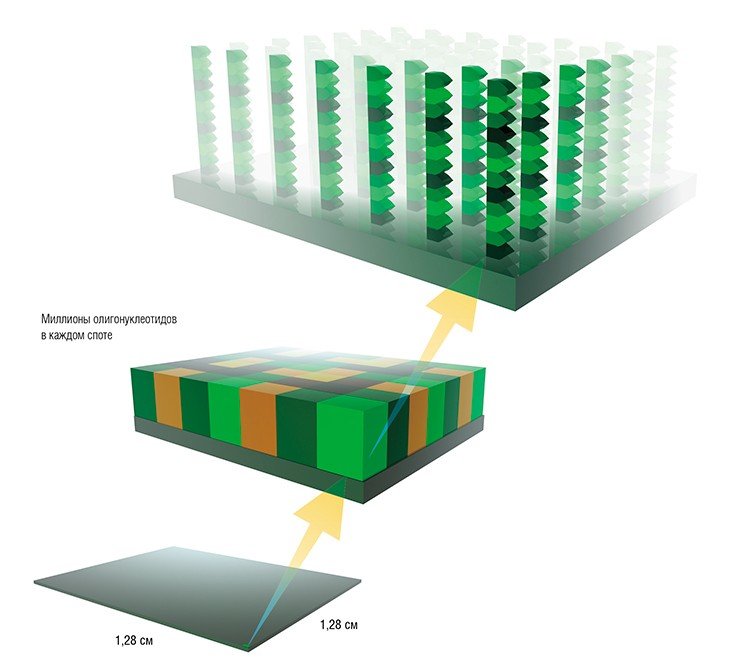
Одна из крупнейших фирм по производству биочипов — американская компания Affymetrix — применяет для производства биочипов способ конструирования, созданный для электронных чипов. Чипы Affymetrix готовятся на стеклянной пластинке-платформе методом фотолитографии с использованием специальных микромасок. Применение хорошо отработанных методов электронной промышленности позволило добиться впечатляющих результатов: на одном таком чипе могут располагаться миллионы различных спотов (участков, содержащих одинаковые молекулы-зонды) размером всего лишь в несколько микрон
Существующее в профилях генной экспрессии разнообразие находится в фокусе внимания ученых по причине его биологического и клинического значения. И в этом смысле возможности технологии микрочипов оказались очень полезными при исследовании такого сложного заболевания, как рак. Эта технология позволяет одновременно отслеживать экспрессию десятков тысяч генов, создавая, таким образом, своеобразный молекулярный «портрет» клетки. Уже сегодня, изучая профили генной экспрессии в клетке, можно ставить диагноз, определять группу риска и давать прогноз развития многих видов раковых заболеваний.
В настоящее время для постановки диагноза больным раком требуется проведение совместной экспертизы специалистов-практиков: онкологов, патологов и цитогенетиков. Однако окончательные выводы могут значительно варьироваться в зависимости от таких субъективных факторов, как уровень квалификации экспертов и примененные ими методологические подходы. Используя же микрочипы, можно и вовсе отказаться от услуг многих специалистов, намного повысив точность постановки диагноза и определения прогноза.
В существующих экспрессионных биочипах используется иммобилизованная ДНК двух типов: во-первых, относительно короткие синтетические фрагменты ДНК длиной 20—60 нуклеотидов, которые соответствуют определенным участкам конкретного гена (при этом каждый ген характеризуется 20—40 спотами с различными зондами); во-вторых, крупные фрагменты кодирующей ДНК длиной 100—600 нуклеотидов, получаемые ферментативным способом (так называемые кДНК-микрочипы).
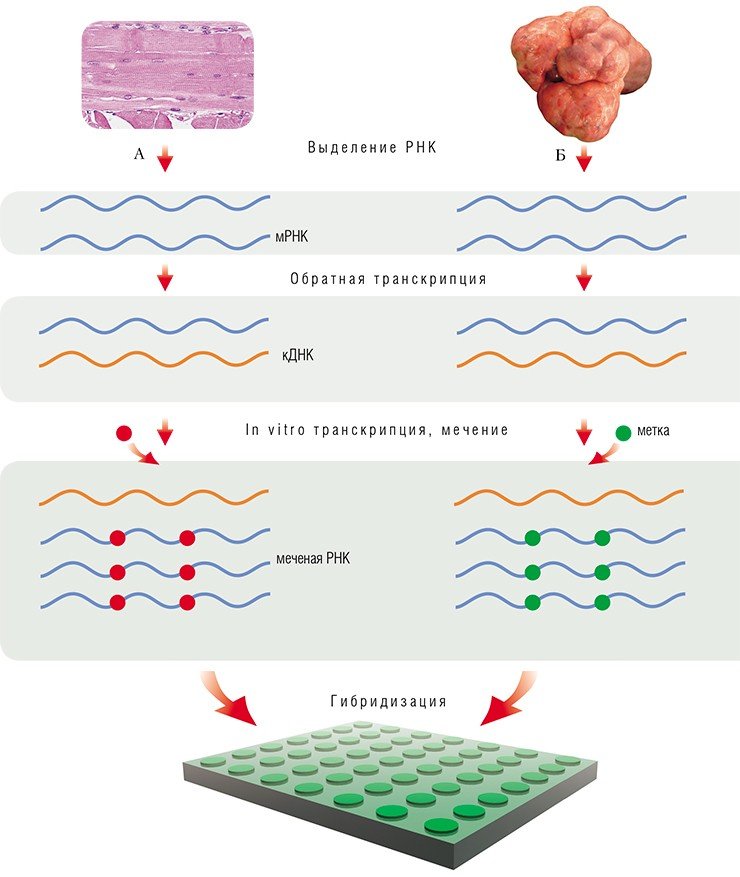
Процедура подготовки образца для анализа на микрочипах включает в себя выделение суммарной РНК, на основе которой посредством реакции обратной транскрипции синтезируют цепи кодирующей ДНК. Из каждой молекулы такой кДНК с помощью фермента Т7 РНК-полимеразы можно получить множество копий РНК. Как правило, образующися молекулы РНК при этом одновременно метятся флуоресцентной меткой (для этого при синтезе используются меченые нуклеотиды).
В работе с олигонуклеотидными микрочипами для мечения образца получаемой РНК часто употребляют флуоресцентную метку одного типа, а уровни экспрессии генов определяют, сравнивая получаемые флуоресцентные сигналы с сигналами внутренних контрольных точек микрочипа.
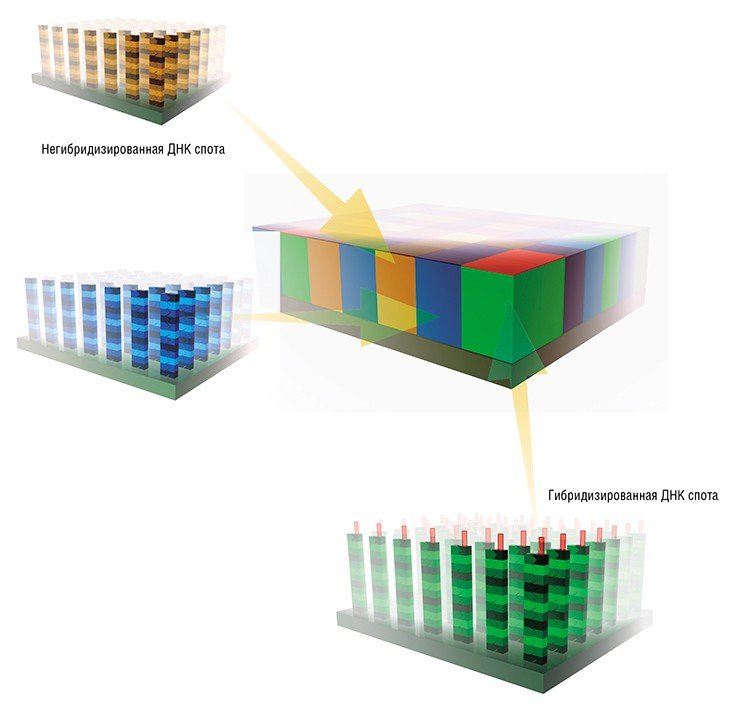
При работе же с микрочипами на основе кДНК, как правило, необходимы две метки: контрольный образец (взятый из нормальных клеток) метят одним флуоресцентным красителем, исследуемый образец (взятый, например, из раковой опухоли) — другим; далее их смешивают и гибридизуют с одним микрочипом. По соотношению сигналов от двух разных меток в каждой ячейке микрочипа судят о повышении или понижении уровня экспрессии данного гена при заболевании.
Болезнь, эволюция, преступление...
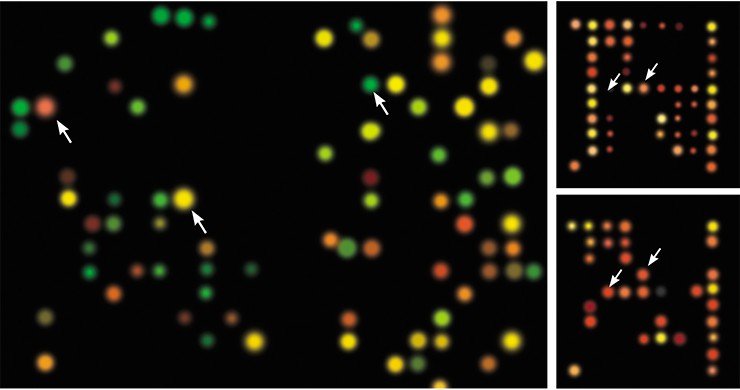
В каждом эксперименте с биочипами можно получить данные относительно уровня экспрессии десятков и сотен тысяч генов. Для обработки такого объема информации используется довольно сложный математический аппарат, и в первую очередь кластерный анализ.
По результатам подобного анализа выявляются группы генов, изменение в уровне экспрессии которых является свидетельством наличия конкретного заболевания. В дальнейшем для диагностики пациентов применяется анализ деятельности именно этих генов. При этом может выясниться, что болезнь, ранее диагностированная как определенный вид рака, на самом деле представляет собой сразу несколько одновременно протекающих заболеваний.
Используя экспрессионные микрочипы, можно не только изучать молекулярные механизмы различных заболеваний, но и проверять воздействие лекарственных соединений на человека (причем показания и противопоказания по применению препаратов можно определить для каждого индивидуума отдельно), а также оценивать отклик организма на влияние самых разнообразных внешних факторов.
Кроме того, олигонуклеотидные микрочипы находят широкое применение при анализе геномного полиморфизма (разнообразия). Известно, что геномные последовательности ДНК для конкретных живых организмов, как правило, несколько отличаются от тех, которые приведены в базах данных. Эти различия обусловлены, прежде всего, точечными мутациями, вставками и делециями (потерей) нуклеотидов и т. п. Подобные различия в носителе наследственной информации приводят, в свою очередь, к внутривидовому различию организмов, а их накопление — к расхождению видов. Таким образом, изучение геномного полиморфизма с помощью микрочипов может способствовать раскрытию одного из важнейших механизмов молекулярной эволюции.
Еще одна область приложения технологии биочипов — изучение мутаций в геноме патогенных агентов, позволяющее точно определить вид бактерий или вирусов. Для этого протяженные фрагменты геномной ДНК или РНК патогена гибридизируют с микрочипом, содержащим специальные олигонуклеотидные зонды.
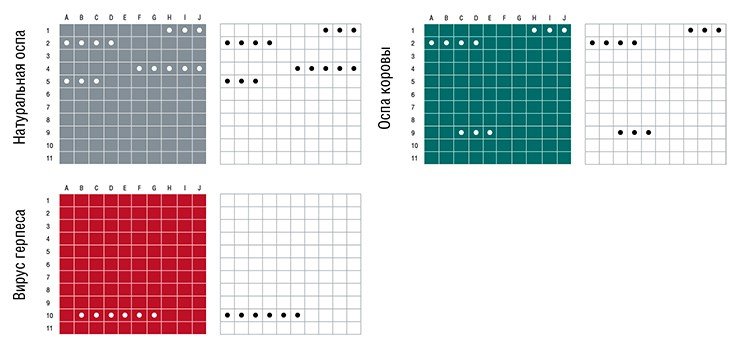
Например, наша лаборатория совместно с Лабораторией разработки методов (Вашингтон) предложила микрочиповый метод обнаружения и классификации опасных для человека ортопоксвирусов. К наиболее опасным для человека ортопоксвирусам принадлежат вирусы натуральной оспы и оспы обезьян. Менее опасны для человека вирусы оспы коров, верблюдов и осповакцины, но и они также способны вызывать заболевания. Несмотря на то что вирус натуральной оспы был искоренен в 70-е гг. прошлого столетия, существует вероятность его нового появления в человеческой популяции: источником возбудителя инфекционных заболеваний могут быть либо вскрытые могильники, либо биотеррористы, которые распространяют его целенаправленно. Поскольку большая часть населения планеты сейчас не имеет иммунитета к этому вирусу, заражение натуральной оспой привело бы к катастрофическим последствиям.
Разработанный нами микрочип способен диагностировать опасные для человека виды ортопоксвирусов. Кроме того, клиническая картина больных ортопоксвирусами очень сходна с клинической картиной больных, пораженных герпесвирусами 1, 2 и 3 типов. Наш микрочип способен отличить тех, кто заражен ортопоксвирусами, от тех, кто поражен вирусами герпеса. Это очень важно, поскольку заболевания, о которых идет речь, несмотря на внешнее сходство клинических проявлений требуют разного лечения.
В Глазном центре Келлога при Мичиганском университете был создан микрочип для диагностики пигментного ретинита — сложного заболевания глаз, которое приводит к слепоте. А с помощью микрочипа arRP-1, разработанного в том же центре, можно выявить 180 мутаций в нуклеотидных последовательностях 11-ти генов, вызывающих дегенерацию сетчатки при этом заболевании.
Отдельный интерес представляют собой исследования мутаций в геномах болезнетворных бактерий, способствующих появлению устойчивости к антибиотикам. Так, по данным ВОЗ, в настоящее время в России ежегодно туберкулезом заболевает примерно 100 тыс. человек (а всего в мире от этой болезни умирает около 3 млн человек в год), при этом особо опасным представляется быстрое распространение среди населения форм туберкулеза, устойчивых к лечению стандартными антибиотиками типа рифампицина.
Вот почему так важно провести раннюю диагностику туберкулеза и выявить устойчивые к антибиотикам формы туберкулеза. С этой целью в Институте молекулярной биологии им. Энгельгардта были созданы диагностические варианты биочипов, которые позволяют осуществлять экспресс-диагностику туберкулеза и вместе с тем обнаруживать его лекарственно-устойчивые формы. Время анализа при этом существенно понижается: с 60 (стандартный анализ) до 1 дня. Это позволяет оперативно назначать резервные терапевтические средства тем больным (а их число среди больных превышает 10 %), у которых обнаружены устойчивые к лекарствам формы туберкулеза.
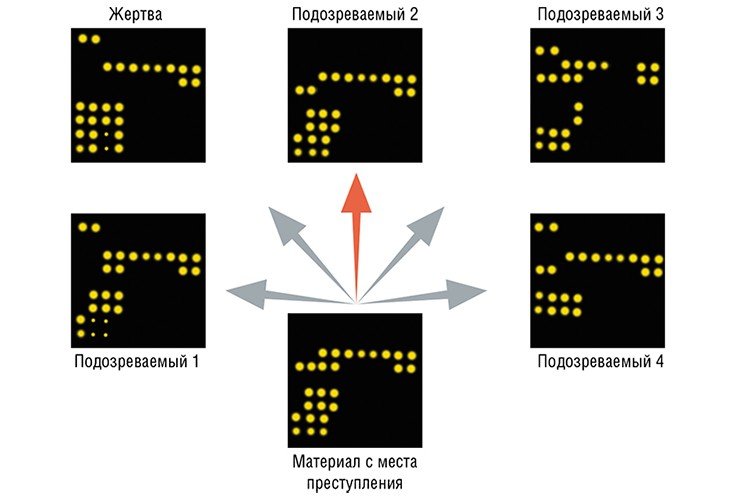
Биочипы могут найти практическое применение и в области, весьма далекой от медицины, а именно в судебной практике: для идентификации и опознания личности. В этом случае при проведении анализа используются нуклеотидные последовательности самых изменчивых участков ДНК митоходрий человека.
Наряду с ДНК-микрочипами, широкую известность приобрели белковые микрочипы, роль молекул-зондов в которых играют пептиды или целые белки. С помощью таких микрочипов можно исследовать взаимодействия белок-белок, белок-ДНК и т. п. Чаще всего конструируются белковые микрочипы, содержащие антитела, которые служат для специфической диагностики патогенов.
Кроме того, существуют и другие виды микрочипов: химические микрочипы, которые включают в себя настоящие комбинаторные «библиотеки» небольших химических соединений: благодаря им можно проводить одновременный скрининг тысяч потенциальных лекарственных средств; микрочипы, которые содержат образцы биологической ткани и используются для одновременного анализа тысяч образцов тканей: они применяются при определении содержания белков в здоровых и патологически измененных тканях, а также при оценке потенциальных мишеней для лекарственных препаратов.
Как же можно оценить внедрение биочипов в научную и медицинскую практику в целом? Безусловно, развитие новых технологий приведет (и уже приводит) к небывалому качественному скачку в этих областях.
И неудивительно: ведь эти миниатюрные устройства, содержащие в своем составе миллионы спотов с самыми разными молекулами-анализаторами, в принципе способны одновременно отслеживать работу всех генов человека. Их использование открывает широкие горизонты для исследований, направленных на более глубокое понимание основ функционирования организмов в нормальном и патологическом состояниях, а также на создание принципиально новых лекарств. Наше здоровье и здоровье будущих поколений во многом является «делом техники» — и оптимизм вызывает тот факт, что новые технологии становятся доступными уже сегодня.
* Олигонуклеотиды — относительно короткие (длиной несколько десятков нуклеотидов) фрагменты ДНК.