Найден новый, эпигенетический фактор набора избыточного веса у женщин
В наши дни избыточный вес – серьезная проблема для множества людей. И не только эстетическая: ожирение – это повышенный риск развития сердечно-сосудистых болезней, сахарного диабета и рака. Недавно ученые нашли еще один генетический механизм, способствующий набору и сохранению избыточного веса, и узнали, как его можно нейтрализовать
По данным ВОЗ, в европейском регионе избыточный вес имеют уже двое из троих взрослых людей, но что определяет склонность к его набору? Часто говорят: чтобы похудеть, надо просто меньше есть. Однако причиной ожирения может быть не только образ жизни, неспособность «взять себя в руки», но и наследственная склонность к запасанию высокоэнергетических субстратов. Это доказывают наблюдения за однояйцевыми (идентичными) близнецами: даже у тех, кто был воспитан в разных семьях, сходство индекса массы тела составляет 40–70 %.
На сегодня известно несколько генетических вариантов, влияющих на риск развития ожирения, однако они отвечают лишь за четверть изменчивости массы тела в популяции. Это означает, что существуют еще какие-то дополнительные факторы, влияющие на склонность человека к набору избыточного веса. И сейчас появляется все больше данных, что этим фактором могут быть эпигенетические (надгеномные) изменения.
Основной эпигенетический механизм регуляции работы генов – метилирование (присоединение метильной группы -CH3) определенных участков молекулы ДНК. Метильная группа блокирует считывание с ДНК генетической информации, и ген «замолкает»
Исследования, подтверждающие связь эпигенетической регуляции и массы организма, проводились в основном на животных и растениях. Но недавно были получены предварительные данные для человека, связывающие эпигенетические изменения (метилирование) одного из генов с набором лишнего веса.
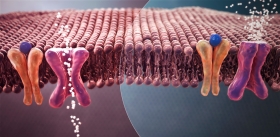
Речь идет о гене, кодирующем белок проопиомеланокортин (POMC), который играет ключевую роль в регуляции чувства сытости. Синтезируется этот сложный полипептид под действием другого гормона – лептина, секретируемого клетками жировой ткани. Лептин активирует расположенные в мозге (в дугообразном ядре гипоталамуса) нейроны, производящие РОМС, который затем расщепляется с образованием гормонально активных продуктов. Эти соединения активируют рецептор меланокортина-4 (MC4R) в паравентрикулярном ядре гипоталамуса, таким образом регулируя чувство сытости и модулируя расход энергии.
Большинство выявленных мутаций в генах, приводящих к развитию ожирения, как раз и связаны с генами, участвующими в передаче сигналов молекулярного пути «лептин – меланокортин». Генетические дефекты в этом каскаде приводят к тяжелому перееданию и раннему ожирению.
Недавно при исследовании эпигенетического статуса гена POMC у более чем 1100 человек было обнаружено, что у тучных женщин он гиперметилирован по сравнению с женщинами с нормальным весом. Низкая активность такого гена увеличивала риск набора избыточного веса примерно на 44 %.
Почему такой эффект проявляется только у женщин, пока непонятно. Ученые предполагают, что это может быть связано с гормональными особенностями и работой регуляторных микроРНК. Если же оценивать этот эффект в целом, то он оказывается сравним с эффектами других известных генетических факторов набора избыточного веса.
При исследовании уровня метилирования этого гена у однояйцевых и разнояйцевых близнецов оказалось, что у первых он был практически одинаковый. Это означает, что такие эпигенетические изменения происходят на очень ранней стадии развития, до того как оплодотворенная яйцеклетка разделяется на два эмбриона.
Есть ли способы повлиять на процесс метилирования генов? Считается, что уровень метилирования связан с наличием в организме источников метильных групп, таких как бетаин, метионин и фолиевая кислота, поступающих с пищей. По другим данным, система метилирования довольно стабильна, и клетки компенсируют небольшие колебания в «поставках» этих соединений. Другое дело, что эпигенетическая изменчивость в значительной степени формируется случайным образом. Так что пока, по крайней мере, повлиять на уровень метилирования гена POMC невозможно.
Ученые подошли к проблеме с другой стороны. Так как гиперметилирование гена POMC может снижать стимуляцию MC4R, то надо воздействовать именно на это звено молекулярного пути «лептин – меланокортин». Для этого использовали одобренный к применению препарат сетмеланотид – агонист MC4R, способствующий его активации. Сетмеланотид обычно используют для подавления чувства голода у пациентов с ожирением и мутацией гена POMC.
Эффективность этого препарата при гиперметилированном POMC была подтверждена в эксперименте, в котором участвовали четыре женщины и один мужчина с синдромом Кляйнфельтера, т. е. с дополнительной X-хромосомой. Все они на фоне приема препарата в течение нескольких месяцев испытывали более слабое чувство голода, чем обычно, а к концу эксперимента потеряли в среднем 7 кг (около 5 % веса).
Теперь нужны дальнейшие исследования, чтобы подтвердить эффективность и безопасность приема сетмеланотида в течение более длительного времени.
Фото: https://openclipart.org