Стресс будущей матери грозит ее ребенку психическими расстройствами
До XIX в. врожденные уродства, дефекты психики и даже криминальные наклонности детей вменялись почти исключительно в вину матери – ее неправильному питанию, плохому эмоциональному состоянию и социальному окружению во время беременности. Сейчас мы знаем о наследственности неизмеримо больше, однако до сих пор не всегда понимаем, как состояние беременной женщины отражается на здоровье ее будущего ребенка, в том числе психическом. Недавно американские исследователи проверили одну из гипотез, лежащих в основе формирования у детей расстройств аутистического спектра.
Поразительно, но только пятая часть человеческих зародышей, образовавшихся в результате слияния яйцеклетки и сперматозоида, имеет шанс благополучно завершить период внутриутробного развития. Большая часть эмбрионов гибнет на ранней стадии из-за хромосомных мутаций и других нарушений, другие – при имплантации в стенку матки и т. п. И все-таки каждый пятый успешно дойдет до «финиша» – но вот с какими показателями?
Нормальная беременность длится плюс-минус 273 дня, и все это время на организм женщины (а через него – и на будущего ребенка) будут воздействовать самые разные факторы – генетические, социально-экономические, окружающей среды, образа жизни, сплетаясь в сложную и до сих пор еще неясную общую картину. Но каждый новый научный результат «высвечивает» в этой картине еще один фрагмент.
Прорыв в понимании феномена взаимодействия беременной матери и будущего ребенка был связан с открытием эпигенетических механизмов модификации ДНК, которые влияют на активность генов, не меняя саму генную структуру. Оказалась, что такие изменения также могут наследоваться и увеличивать у ребенка риск развития ожирения и сердечно-сосудистых болезней, понижать стрессоустойчивость и даже приводить к развитию сахарного диабета.
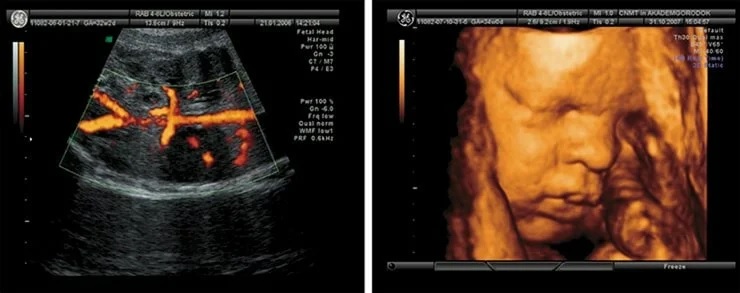
В последние годы активно ведутся исследования микробиома – сообществ микроорганизмов, обитающих в нашем теле и выполняющих целый спектр разнообразных функций, от переваривания пищи до поддержания иммунитета. Бактерии, живущие в кишечнике, могут влиять даже на наше поведение – такие связи опосредованы выделяемыми ими химическими соединениями. О важности подобных взаимосвязей говорит тот факт, что в случае детского аутизма индивидуальный подбор пищевого рациона в сочетании с коррекцией микрофлоры нередко оказывается даже более действенным, чем психотропные препараты.
Известно, что дети женщин, испытавших во время беременности серьезный психосоциальный стресс, более склонны к развитию депрессии, тревоги и расстройств аутистического спектра. Этот эффект подтвердили на моделях грызунов, однако его механизм остается неизвестным. Было высказано предположение, что в этом случае влияние матери является результатом взаимодействия «трех китов»: материнского кишечного микробиома, процесса воспаления и системы серотонина – «гормона счастья», участвующего в психических процессах.
Ранее ученые из Университета штата Огайо (США) на примере лабораторных мышей показали, что в результате дородового стресса кишечный микробиом меняется как у матери, так и потомства, при этом у ребенка формируются «неправильные» поведенческие реакции.
В новом эксперименте ученые попытались оценить роль, которую играют в этих взаимодействиях хемокины (хемотаксические цитокины) – сигнальные белки, которые регулируют миграции клеток иммунной системы. В данном случае они отслеживали хемокин CCL2 – один из самых важных белков, осуществляющих контроль за выходом иммунных клеток из кроветворных органов и их продвижением к фокусам воспаления.
Исследовали подвергли беременных самок мышей стрессу (обездвиживанию) в период, соответствующий ключевым этапам развития нервной системы эмбрионов. Оказалось, что у обычных мышей стресс стимулирует воспалительные процессы, что выражается в повышении уровня CCL2 в плаценте и мозге эмбрионов. Кроме того, он повышает уровень серотонина в плаценте, что может вызывать нарушения развития нервной системы и, в дальнейшем, поведенческие изменения у новорожденных мышат.
Однако у животных, принудительно «лишенных» микробиома, а также у мышей с «выключенным» геном, кодирующим белок CCL2, подобные изменения, включая поведенческие, не наблюдались.
На основе этих данных исследователи попытались реконструировать причинно-следственные связи между внутриутробным стрессом и особенностями психики у детей. По их мнению, стресс беременной матери провоцирует воспалительный процесс в развивающемся мозге эмбриона, что вызывает целый ряд неблагоприятных последствий, начиная от прямого повреждения нейронов до изменения обмена серотонина. При этом «проводником» стресса выступает материнский микробиом, который тесно взаимодействует как с ее иммунной, так и с нервной системой.
К сожалению, дать практические рекомендации будущим матерям по результатам этой и других подобных работ нельзя. Универсального решения проблемы стресса на сегодня просто не существует, но мы можем учиться справляться с ним, используя для этого все возможности.
Фото: https://commons.wikimedia.org