Как убить раковые клетки и не вызвать «цитокиновый шторм»
Авторы революционной методики иммунотерапии рака с использованием Т-клеток в 2018 г. получили Нобелевскую премию. Выдающиеся результаты стали итогом осмысления того, что наша иммунная система играет главную роль в постоянной, пусть и невидимой борьбе организма со злокачественными клетками. Оказалось, что это природное свойство иммунитета можно искусственно усилить и использовать, когда опухоль оказывается сильнее природных защитных механизмов. Хотя далеко не все проблемы на этом пути уже решены
Иммунная система здорового человека умеет обнаруживать и уничтожать мутировавшие клетки, способные превратиться в раковые – это входит в ее прямые «обязанности». И первые попытки активировать иммунитет для борьбы с этой болезнью были предприняты еще в начале прошлого века. Для этого использовались «убитые» патогенные бактерии (как при вакцинации), и в некоторых случаях опухоли полностью исчезали.
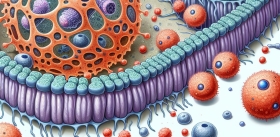
Один из современных методов активации иммунитета при иммунотерапии рака – это введение в организм больного генетически модифицированных Т-лимфоцитов (CAR T-клеток), способных распознавать клетки конкретной опухоли у конкретного пациента. Такие терапевтические лимфоциты получают из Т-клеток, взятых от самого больного. После введения уже модифицированных Т-клеток в организм пациента они начинают активно атаковать опухоль. Первоначально этот метод был направлен против злокачественных заболеваний кроветворной системы, но сейчас его пытаются использовать и для лечения обычных «твердых» опухолей.
Этот на первый взгляд простой, но эффективный метод, к сожалению, может иметь серьезные побочные эффекты. Дело в том, что дополнительные иммунные клетки вырабатывают избыточное количество биологически активных молекул – цитокинов, которые вызывают сильнейшую воспалительную реакцию с разнообразными симптомами, от высокой температуры до недостаточности органов. У многих пациентов такой «цитокиновый шторм» может приводить к тяжелому, угрожающему жизни состоянию, к тому же снижать противораковую эффективность терапии.
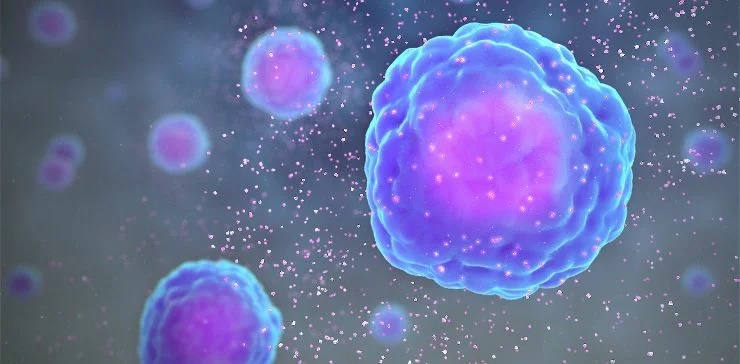
Недавно группа китайских ученых изучила «в пробирке» процесс уничтожения раковых клеток CAR T-клетками. Оказалось, что при этом модифицированные лимфоциты начинают выделять в окружающую среду в три-четыре раза больше белков перфорина и гранзима B, ответственных за образование пор в клеточной мембране. Формирование «дыр» в мембранах опухолевых клетках способствует их гибели путем пироптоза – одного из видов запрограммированной некротической гибели клетки, при котором после разрушения мембраны все содержимое клетки «вываливается» наружу. При этом высвобождаются и молекулы, активирующие иммунные клетки макрофаги, которые и производят вещества, вызывающие воспаление. Этот механизм был подтвержден в экспериментах на мышах, у которых был смоделирован синдромом высвобождения цитокинов в результате CAR T-клеточной терапии.
Чтобы снять негативные последствия иммунотерапии, можно попробовать так модифицировать T-клетки, чтобы они вызывали более щадящий для окружения тип запрограммированной клеточной смерти – апоптоз, при котором не происходит выброса иммуногенных и токсичных молекул. Есть и другие варианты, но все это – дело будущего. Пока же пациентам, получающим CAR T-клеточную терапию, остается надеяться на лучшее.
Фото: https://commons.wikimedia.org и https://commons.wikimedia.org