«Обученные» иммунные клетки-киллеры спасли больную раком груди в терминальной стадии
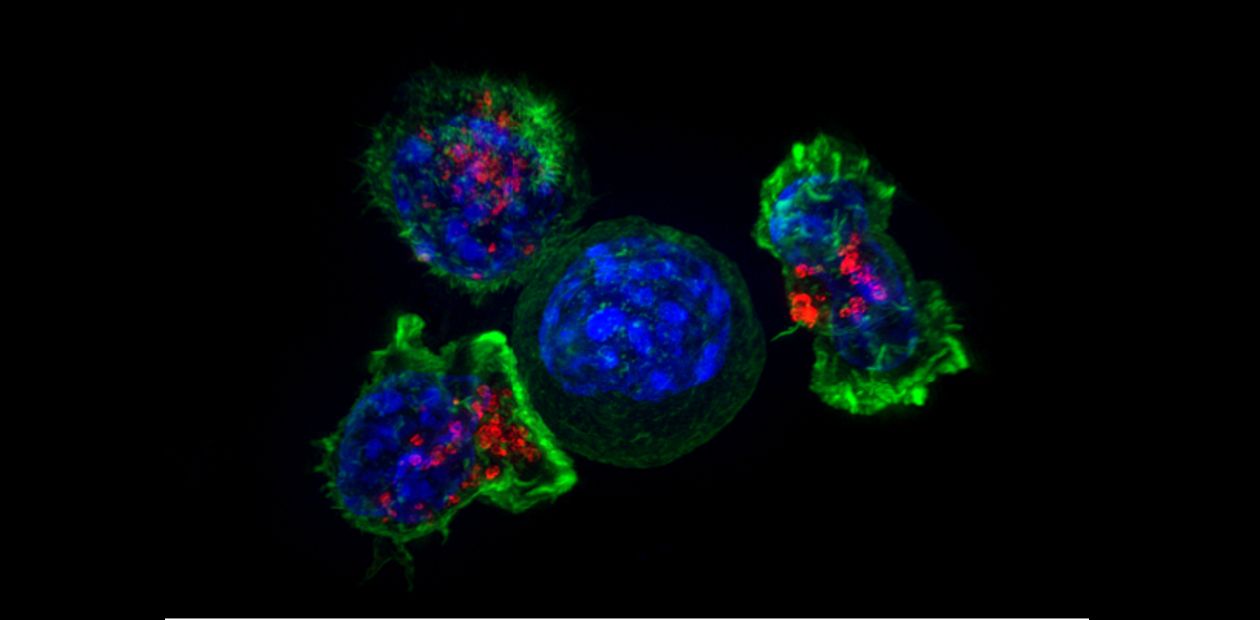
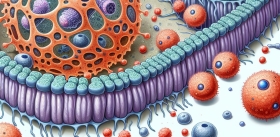
Чтобы понять суть метода иммунотерапии рака, сначала немного ликбеза. Главными клетками иммунной системы являются лимфоциты, которые вырабатывают белки-антитела против антигенов («чужеродных» молекул, в том числе на клеточных мембранах), обеспечивают контактное взаимодействие с патологическими клетками и вообще «мастера на все руки». Центральными «игроками» противоопухолевого иммунитета являются цитотоксические Т-лимфоциты, которые недаром называют еще Т-киллерами, а также особые дендритные клетки, которые «показывают» чужеродный антиген Т-лимфоцитам и таким образом активируют и направляют их деятельность.
Первые попытки использовать Т-лимфоциты как инструмент противораковой терапии начались еще в 1980-х гг., когда эти клетки научились культивировать вне организма. Т-лимфоциты, инфильтрирующие опухоль, выделяли из опухолевой ткани, размножали и вводили обратно пациенту. Таким образом удавалось добиться серьезных улучшений у больных меланомой. Однако в силу трудоемкости метода и побочных эффектов, связанных с сопутствующим введением высоких доз ростовых факторов, этот метод применялся лишь в случае, когда иных способов лечения не существовало (например, при метастатической меланоме – наиболее агрессивной стадии рака кожи).
Современные методики позволяют избирательно нацеливать Т-лимфоциты на опухолевые клетки благодаря генной модификации их поверхностных рецепторов. Однако до сих пор считалось, что такая терапия эффективна лишь в случае эпителиальных опухолей с высоким уровнем соматических мутаций (при меланоме, раке легких и мочевого пузыря), но не слишком результативна в отношении других распространенных видов рака эпителия, характеризующихся более низкой скоростью мутирования (рака желудочно-кишечного тракта, яичников, молочной железы).
Недавно в США были проведены клинические испытания иммунотерапевтического подхода к лечению рака молочной железы на 49-летней больной, которая фактически умирала, – опухоль оказалась устойчива сразу к нескольким видам химиотерапии. Ученые выделили из опухолевой ткани пациентки наследственный материал (ДНК и РНК), в котором было выявлено несколько десятков новых мутаций.
Параллельно из опухоли выделили инфильтрирующие ее Т-лимфоциты и другие иммунокомпетентные клетки, способные специфически взаимодействовать с антигенами, включая антиген-презентирующие дендритные клетки. Внутрь этих клеток поместили фрагменты матричной РНК, содержащие мутации, характерные для опухоли. Модифицированные дендритные клетки активировали цитотоксические Т-лимфоциты, среди которых были отобраны те, что наиболее активно реагировали на мутантные версии белков, кодируемых генами SLC3A2, KIAA0368, CADPS2 и CTSB. Эти лимфоциты, размноженные в большом количестве, были введены пациентке.
Через 1,5 месяца после введения «обученных» Т-клеток размер опухоли уменьшился наполовину, а спустя 22 месяца наблюдалась видимая полная регрессия не только опухоли, но и метастазов. Этот вдохновляющий результат показывает, что максимально персонализированная терапия, при которой иммунные клетки-киллеры прицельно «направлены» на опухоль с конкретным мутантным «профилем», может привести к долговременной ремиссии даже в безнадежном случае.
Фото: https://visualsonline.cancer.gov
Подготовила Мария Перепечаева